Clear Sky Science · tr
APOL1 plazma zarıh havuzları hızlı protein yıkımına direnç gösterir
Neden bir böbrek proteininin “kayboluş gösterisi” önemli?
Yakın Afrika kökenli kişilerde görülen ağır böbrek hastalıklarının büyük bir kısmı tek bir genin, APOL1’in iki varyantına bağlanmıştır. Yine de bilim insanları bu genin çoğu taşıyıcıya zarar vermeden böbrek hücrelerine nasıl zarar verdiğini tam olarak açıklamakta zorlanıyor. Bu çalışma, basit görünen ama büyük sonuçları olan bir soruyu soruyor: APOL1 proteini hücre içinde üretildikten sonra ne kadar süre kalıyor ve nerede en kararlı? Cevaplar şaşırtıcı bir ikili kişilik ortaya koyuyor—APOL1 hücre içinde hızla yok edilirken, hücrenin dış yüzeyine gömüldüğünde inatla stabil kalıyor; bu da gelecekteki tedavilere yol gösterebilecek bir ipucu sunuyor.
Çifte kenarlı risk geni
APOL1 geni belirli parazitlere karşı insanları korumaya yardımcı olur; bu evrimsel avantaj, G1 ve G2 adı verilen risk varyantlarının Afrika nüfuslarında yaygın olmasını muhtemelen açıklar. Ne yazık ki bu varyantların iki kopyasını miras alan kişiler APOL1 kaynaklı böbrek hastalıkları olarak gruplandırılan bozukluklar için belirgin biçimde artmış bir riskle karşılaşır. Önceki çalışmalar, APOL1 seviyeleri yükseldiğinde—çoğunlukla iltihabi yanıta bağlı olarak—proteinin özellikle podositler gibi hassas böbrek filtreleme hücrelerinde toksik hale gelebildiğini göstermişti. Ancak çoğu çalışma APOL1’i neyin açtığına odaklandı. Hücrelerin onu kapatıp örneğin proteini parçalayarak nasıl yok ettiği çok daha az bilinmektedir.
Hücre içindeki kırılgan proteini izlemek
APOL1’in stabilitesini incelemek için araştırmacılar insan hücre hatlarını floresan etiketli APOL1 ve en yakın akrabası APOL2 varyantlarını üretecek şekilde tasarladılar. Bu, Western blot, mikroskopi ve akım sitometrisi kullanarak her bir proteinin farklı koşullar altında ne kadar biriktiğini veya kaybolduğunu izlemesini sağladı. Hücrenin ana protein öğütme makinası olan proteazomu engellediler ve ayrı olarak yeni protein üretimini durdurdular. Proteazomlar inhibe edildiğinde APOL1 seviyeleri hızla yükseldi; bu, normalde hızlı bir şekilde parçalandığını gösterdi. Yeni protein sentezi durdurulduğunda APOL1 seviyeleri hızla düştü. Buna karşılık, APOL2 her iki işlem altında neredeyse değişmedi ve çok daha kararlı bir protein olduğunu ortaya koydu. Önemli olarak, APOL1’in yüksek dönüşüm hızı normal versiyon (G0) ile böbrek risk versiyonları (G1 ve G2) arasında aynıydı ve membranlarda yerleşme biçimleri farklı olan birkaç doğal APOL1 formunda da gözlendi.
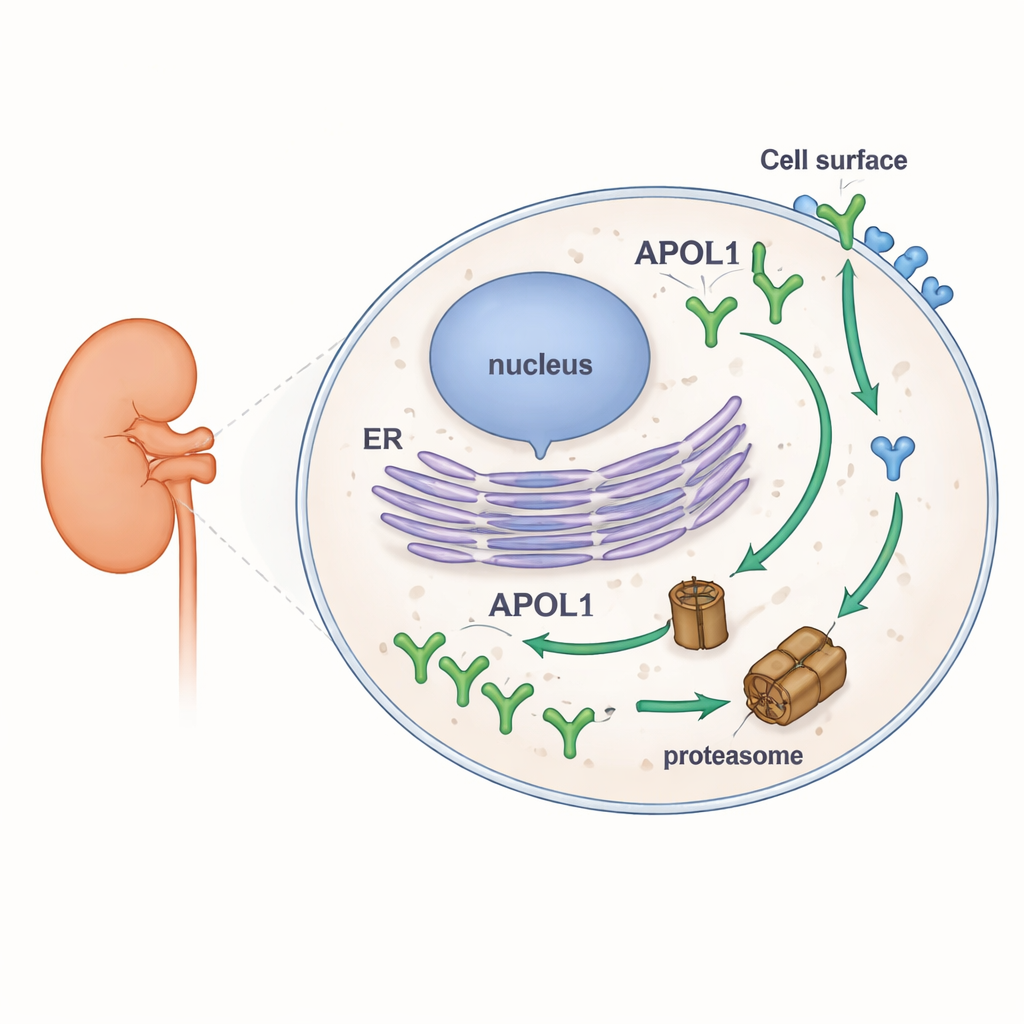
Sıralama ipuçları ve iki mahallenin hikâyesi
Proteinin yapısına inen ekip, APOL1 ve APOL2’yi intrinsically disordered regions (içsel olarak yapılandırılmamış bölgeler) olarak bilinen gevşek, yapılandırılmamış segmentler açısından bilgisayar araçlarıyla taradı. Bu tür bölgeler sıklıkla proteazom için “beni ye” sinyalleri olarak işlev görür. APOL1 içinde APOL2’de büyük ölçüde bulunmayan iki güçlü aday bölge tespit ettiler. APOL1’in özgün ön ucunun kırılganlığına katkıda bulunup bulunmadığını test etmek için hibritler oluşturdular: ilk 59 amino asidi eksik kısaltılmış bir APOL1 ve o APOL1 segmentini taşıyan bir APOL2 chimera. APOL1’in N-terminal parçasını APOL2’ye eklemek APOL2’yi daha hızlı parçalanır hale getirirken, kısaltılmış APOL1 kararsız kaldı; bu, APOL1’in hızlı yıkımını teşvik eden birden fazla bölüm olduğunu düşündürüyor. Birlikte, bu sonuçlar APOL1’in alışılmadık esnek segmentlerini hızlı dönüşümüne bağlarken, bu davranışı özellikle hastalık oluşturan varyantlara bağlamıyor.
Hücre yüzeyinde inatçı protein
Yazarların hücre içindeki APOL1 ile hücre yüzeyindeki APOL1’i ayırdıklarında ortaya çıkan en çarpıcı bulgu bu oldu. Sadece dışa maruz kalan APOL1 kısmını tanıyan antikorları kullanarak yüzey seviyelerini toplam seviyelerden ayrı olarak ölçtüler. Hücre içinde APOL1 beklendiği gibi davrandı: proteazomlar engellendiğinde birikti ve yeni sentez durdurulduğunda hızla kayboldu. Ancak yüzey APOL1 herhangi bir durumda neredeyse hiç değişmedi. APOL1 molekülleri plazma membranına ulaştığında, hızlı yıkıma karşı son derece dirençli oldukları ortaya çıktı. Dahası, risk varyantları toplam APOL1’den daha az üretseler bile, yüzey seviyeleri benzerdi. Bu, riskli ve normal APOL1’in hücre içinde benzer oranlarda temizlendiğini, ancak iyon kanalları oluşturdukları ve toksisiteyi tetikledikleri düşünülen membrana gömülü havuzların tüm varyantlarda korunduğunu düşündürmektedir.
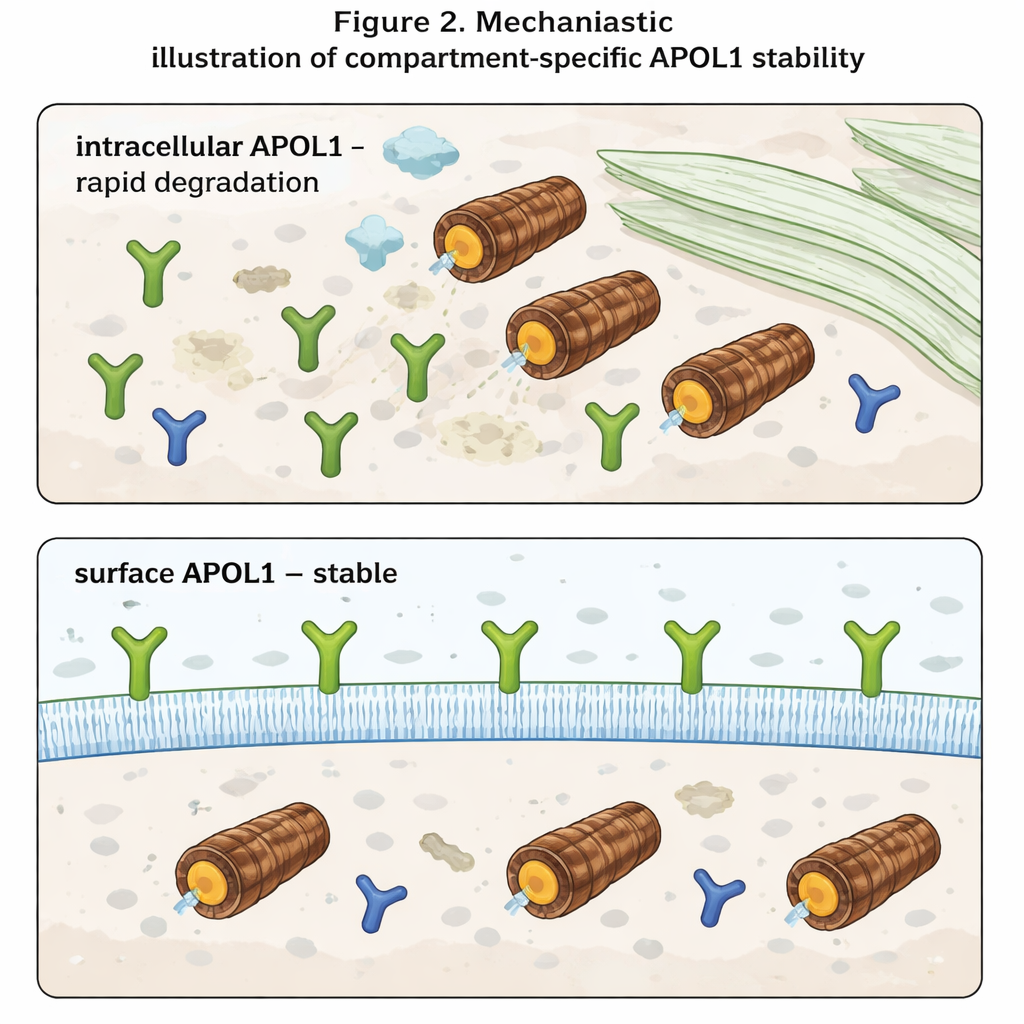
Gelecekteki tedaviler için ne anlama geliyor
Uzman olmayanlar için çıkarılacak ana mesaj, APOL1’in bulunduğu yere bağlı olarak çok farklı davrandığıdır. Hücre içinde kısa ömürlü bir protein olup, hızlıca tanınıp yok edilir. Hücre yüzeyinde ise uzun ömürlü ve nispeten korunmuş hale gelir; hatta hücrenin yıkım mekanizması değişse bile. Hastalığın yüzeydeki APOL1 kanallarının sodyum ve potasyum gibi iyonların dengesini bozduğunda ortaya çıktığı düşünüldüğünden, tedaviler muhtemelen toplam APOL1 seviyelerinden çok ne kadarının plazma membranına ulaştığına ve orada ne kadar kaldığına odaklanmalı. APOL1’in yüzeye taşınmasını azaltan veya yüzey havuzunu seçici olarak kararsızlaştıran stratejiler, teoride genin faydalı bağışıklık işlevlerini tamamen engellemeden böbrek hasarını hafifletebilir.
Atıf: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Anahtar kelimeler: APOL1, böbrek hastalığı, protein yıkımı, plazma membranı, proteazom