Clear Sky Science · tr
İnsan histon deasetilaz 5’in katalitik bölgesinin in vitro karakterizasyonu
DNA paketlenmemizdeki küçük anahtarların neden önemi var
Her hücrenin içinde DNA’mız, makaralara benzeyen proteinlerin etrafına sarılmıştır; bu, metrelerce genetik materyalin mikroskobik bir alana sığmasına yardımcı olur. Bir genin açık mı kapalı mı olduğu sıklıkla bu makaralardaki küçük kimyasal etiketlere bağlıdır. Bu çalışma, kalp hastalıkları, beyin bozuklukları, kanser ve daha fazlasıyla ilişkilendirilen HDAC5 adlı belirli bir protein “anahtarına” odaklanır. HDAC5’in moleküler düzeyde nasıl çalıştığını anlamak, araştırmacıların daha az yan etkiye sahip, daha hassas ilaçların geliştirilmesine zemin hazırlamasını umuyor.
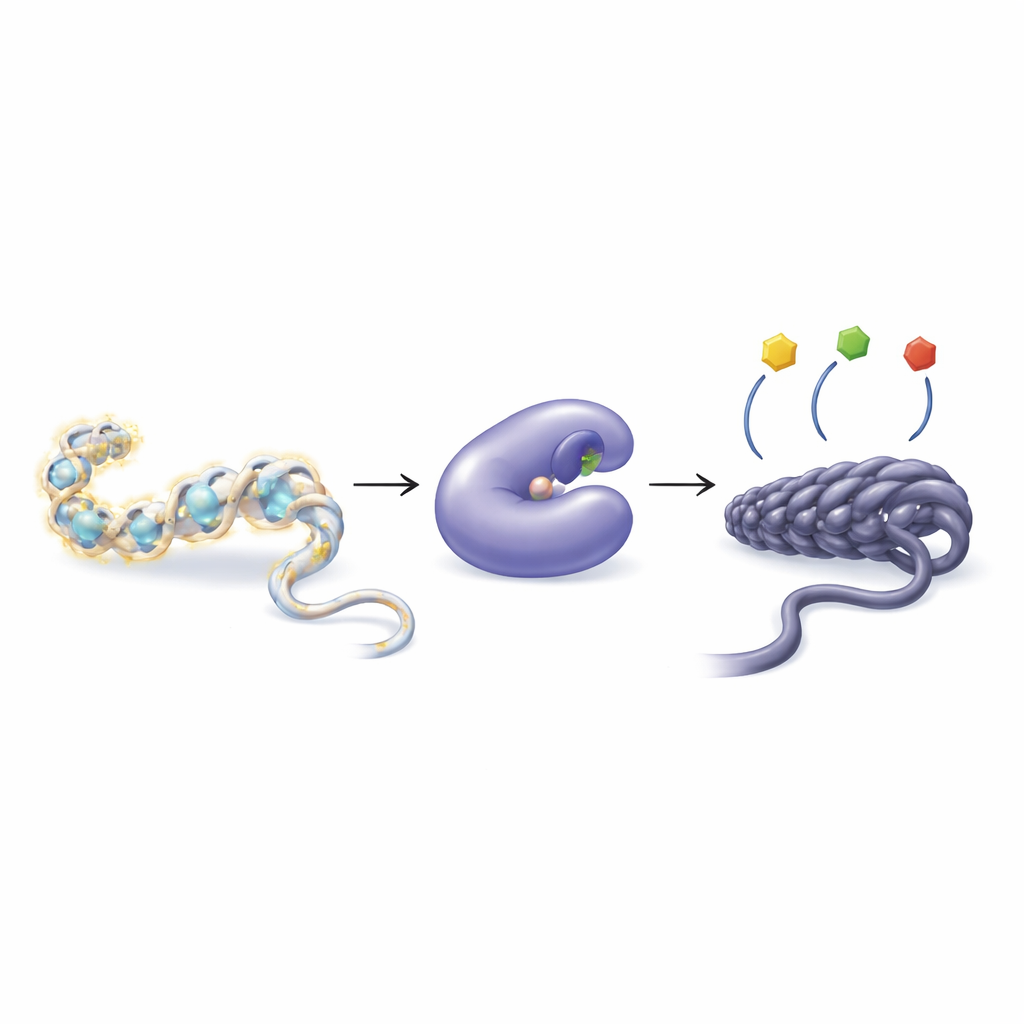
Hücreler genleri küçük kimyasal etiketlerle nasıl ayarlar
DNA’mız serbestçe yüzmez; histon adı verilen proteinlerin etrafına sarılarak kromatin adı verilen yapıyı oluşturur. Hücreler, kromatini gevşetmek veya sıkılaştırmak için histon kuyruklarından asetil grupları gibi küçük kimyasal grupları ekleyebilir veya çıkarabilir. Daha gevşek paketleme genlerin okunmasını kolaylaştırır; daha sıkı paketleme genleri sessize alma eğilimindedir. Bu dengeyi iki enzim grubu yönetir: histon asetil transferazlar asetil gruplarını eklerken, histon deasetilazlar (HDAC’lar) bunları çıkarır. Bu dengenin bozulması, kanser, kalp sorunları, kas kaybı ve bağışıklık bozuklukları dahil geniş bir hastalık yelpazesine katkıda bulunabilir.
HDAC5 neden umut vaat ediyor ama zorlu bir ilaç hedefi
HDAC’lar birkaç sınıfa ayrılan geniş bir enzim ailesi oluşturur. Günümüzde klinikte kullanılan birçok ilaç birçok HDAC tipini aynı anda engeller; bu da önemli normal işlevleri kapatıp güçlü yan etkilere yol açabilir. Sınıf IIa HDAC’lar, özellikle beyin, kalp ve iskelet kası gibi belirli dokularda zengin olmaları ve anahtar gen ağlarını düzenlemek için diğer proteinlerle ortaklık kurmaları nedeniyle öne çıkar. HDAC5 sık sık bir köprü görevi görür; kromatini sıkılaştırmak ve bazı genleri susturmak için yüksek aktiviteli bir ortak enzim (HDAC3) getirir. Bu odaklanmış rolleri nedeniyle HDAC5 daha seçici ilaçlar için çekici bir hedef olarak görülür, ancak ayrıntılı biyokimyasal verilerin eksikliği ve aktif çekirdeğinin yüksek çözünürlüklü bir yapısının olmaması rasyonel ilaç tasarımını zorlaştırmıştır.
HDAC5’i deney tüpünde yeniden kurmak
Bu eksikliği ele almak için araştırmacılar insan HDAC5’in yalnızca kimyasal reaksiyonu gerçekleştiren katalitik çekirdeğini bakterilerde ürettiler, saflaştırdılar ve çözeltide kararlı, tek birimlik bir protein oluşturduğunu doğruladılar. Ardından farklı tuz düzeyleri ve asitlik altında nasıl çalıştığını test ettiler. HDAC5’in aktivitesi geniş bir tuz aralığında dayanıklı kaldı ve birçok hücrenin içindekine benzer şekilde hafif bazik koşullarda zirve yaptı. Özel floresan test molekülleri kullanarak, doğal HDAC5 formunun sınıf IIa enzimleri sorgulamak için yaygın olarak kullanılan belirli bir substrat türünü tanıdığını buldular. İlgili HDAC’ler üzerine önceki çalışmalardan yola çıkarak kritik bir noktada tek bir amino asidi (histidin) tirozin ile değiştirdiler. Dikkate değer şekilde, bu küçük değişiklik mutant HDAC5’in her iki test substratını da verimli şekilde işlemesine izin verdi; bu da aktif bölgedeki tek bir kalıntının enzimin kimyasal tercihlerini nasıl yönlendirdiğini ortaya koydu.
İki yeni ilaç adayını test etmek ve karşılaştırmak
Ekip daha sonra NT160 ve FFK24 olarak bilinen iki deneysel HDAC5 engelleyici molekülü inceledi. Bu bileşikler, eski hidroksamat bazlı ilaçlarda görülen bazı toksisite ve zayıf seçicilikten kaçınan daha yeni bir çinko bağlayıcı grup kullanır. Her bir inhibitörün kontrollü reaksiyonlarda HDAC5’i ne kadar yavaşlattığını ölçerek yazarlar nanomolar aralığında son derece düşük inhibisyon sabitleri belirlediler; bu, her iki bileşiğin de enzime sıkıca bağlandığı anlamına gelir. NT160 tutarlı şekilde FFK24’e göre yaklaşık on kat daha güçlü bağlandı. Bunun nedenini anlamak için araştırmacılar HDAC5’in çekirdeği için AlphaFold tarafından tahmin edilmiş bir yapıyı kullanarak bilgisayar tabanlı yerleştirme (docking) yaptılar. Her iki inhibitörün de aktif cep içine derinlemesine yerleşen ve metal iyonla temas kuran ortak bir baş bölgesi vardı, ancak NT160’ın kuyruğu cepteki belirli amino asitlerle ekstra stabilleştirici temaslar kurdu. Bu ek etkileşimler muhtemelen onun daha yüksek etkinliğini açıklar.
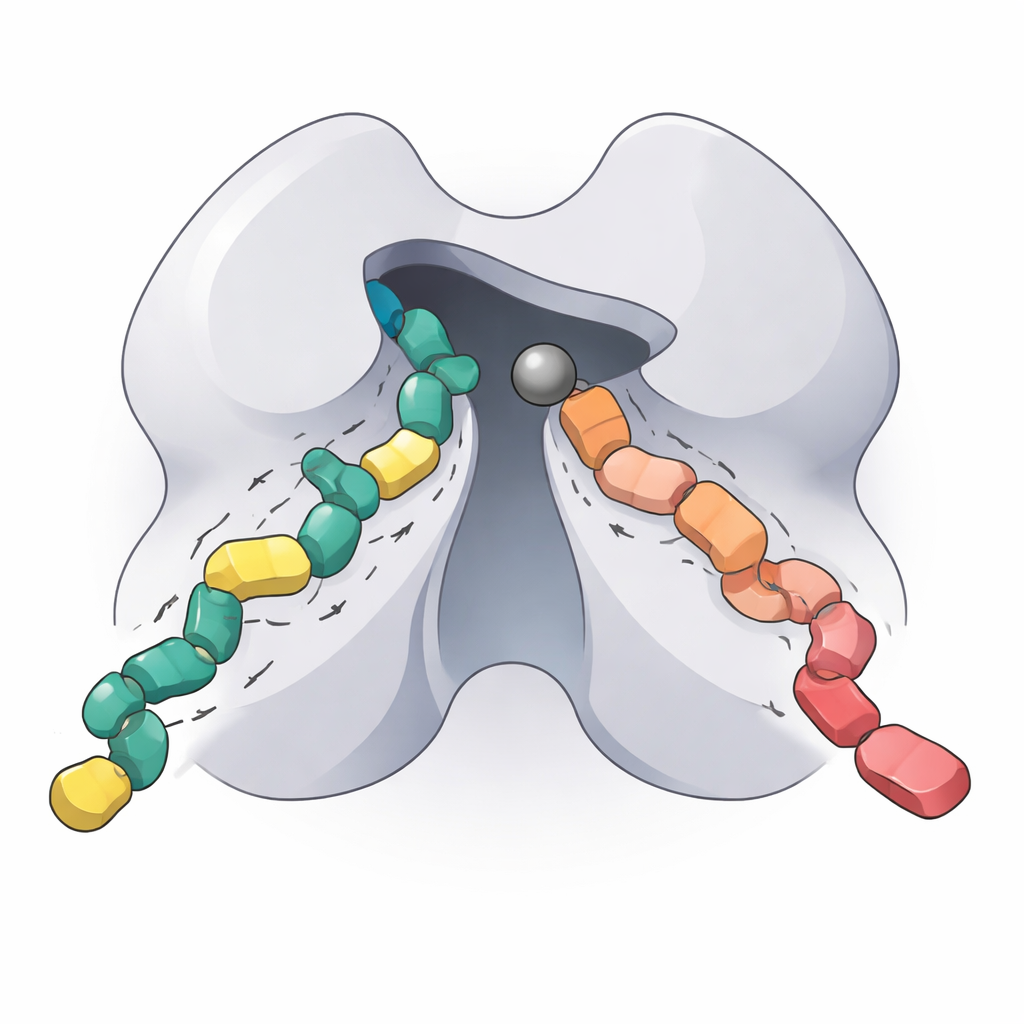
Gelecekteki hedefe yönelik terapiler için anlamı
HDAC5’in çalışan çekirdeğini yeniden oluşturup, optimal çalışma koşullarını haritalandırıp, tek bir amino asit değişikliğinin davranışını nasıl değiştirdiğini çözüp ve iki yeni nesil inhibitörün bağlanmasını nicelendirerek bu çalışma daha önce yeterince tanımlanmamış önemli bir enzimin ayrıntılı bir biyokimyasal “parmak izini” sunuyor. Uzman olmayanlar için ana çıkarım, HDAC5’in belirli genlerin açık mı kapalı mı olacağını kontrol etmeye yardımcı olduğu ve bu anahtarın hassas şekilde ayarlanmasının kalp hastalığı, nörodejenerasyon, kanser ve bağışıklık bozukluklarının tedavisinde değerli olabileceğidir. Burada sunulan yeni bulgular ve araçlar, araştırmacıların ihtiyaç duyulan yerde etki gösteren ve vücudun diğer yerlerinde istenmeyen etkileri en aza indiren HDAC5 ve sınıf IIa-seçici ilaçlar tasarlamasına yardımcı olmalıdır.
Atıf: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Anahtar kelimeler: histon deasetilaz 5, epigenetik düzenleme, HDAC inhibitörleri, hedefe yönelik kanser terapisi, kromatin yapısı