Clear Sky Science · tr
EGF bağlanma bölgesinin CRISPR/Cas9 ile düzenlenmesini takiben EGFR aktivitesindeki değişiklikler
Neden Bir Kanser Sinyalinin Yeniden Yönlendirilmesi Önemli
Rahim ağzı kanseri sıklıkla epidermal büyüme faktörü reseptörü (EGFR) adını taşıyan güçlü bir büyüme anahtarına bağımlıdır. Birçok tümörde bu reseptörlerin sayısı çok yüksektir, ancak bunları kapatmayı hedefleyen ilaçlar yalnızca bir hasta bölümüne yardımcı olmuştur. Bu çalışma, tedavi açısından büyük çıkarımları olan temel bir soruyu sordu: reseptörü tamamen ortadan kaldırmadan EGFR’nin favori büyüme sinyali epidermal büyüme faktörünü (EGF) yakalama yeteneğini kaldırırsanız ne olur?
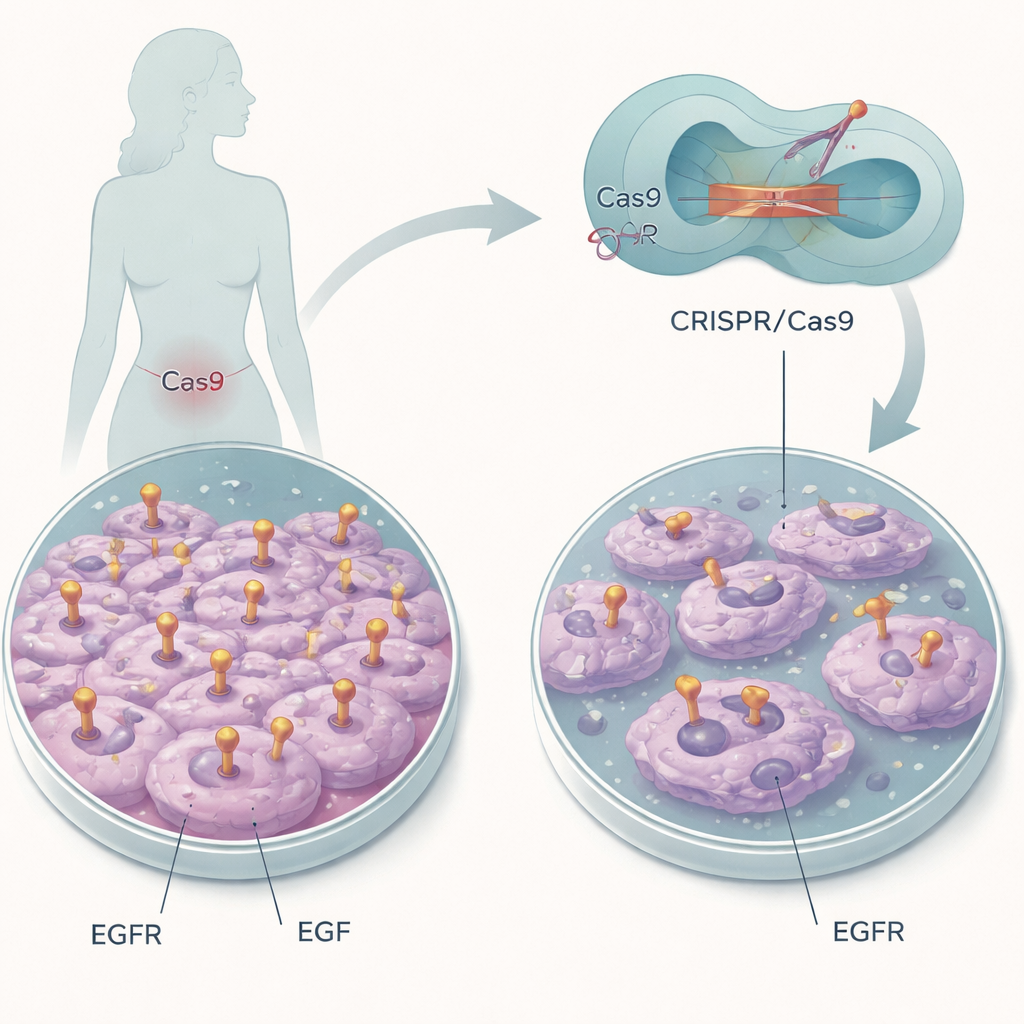
Moleküler Bir "Açık Anahtarını" Kapatmak
Araştırmacılar, büyük miktarda normal EGFR taşıyan bir rahim ağzı kanseri hücre hattına odaklandı. Gen yok etmek yerine, CRISPR/Cas9 genom düzenlemeyi bir moleküler bisturi gibi kullanarak EGFR’nin EGF bağlama cebindeki yalnızca birkaç aminoasidi değiştirdiler. L14 ve Y45 olarak adlandırılan iki özel pozisyon, EGF’nin reseptöre kenetlenmesine yardımcı olur. Bu yapı taşlarını farklıleriyle ikame ederek ekip, EGFR’yi varlığını korurken EGF’ye karşı kör yapmak; böylece bu tek etkileşimin kanser hücresi davranışındaki rolünü izole etmeyi amaçladı.
Tasarımcı Kanser Hücre Hatları Oluşturmak
İlk adımda ekip, bu mutasyonları normal veya değiştirilmiş EGFR’yi geçici olarak üreten plazmidleri kullanarak hücrelerde test etti. Floresan etiketli EGF, tüm mutant formların normal reseptöre kıyasla çok daha az ligand bağladığını gösterdi; özellikle hem L14 hem de Y45 birlikte değiştirildiğinde bağlanma büyük ölçüde azaldı. Araştırmacılar daha sonra bu değişiklikleri CRISPR/Cas9 ile doğrudan kanser hücresi genomuna tanıttı ve birkaç yeni hücre klonu ürettiler. Bazı klonlar tek bir mutasyon taşıyordu, diğerleri çift mutasyonu bir EGFR kopyasında ve diğerinde inaktive edici değişiklikleri taşıyordu. Ortaya çıkan protein şekillerinin bilgisayar modelleri, bu değişikliklerin bağlanma bölgesini yeterince bozduğunu; EGF kenetlenmesini zayıflattığını veya ortadan kaldırdığını gösterdi ve bu sonuçlar bağlanma testleriyle tutarlıydı.
Reseptör Hareket Ediyor Ama Hücreler Hayatta Kalıyor
Ayrıntılı görüntüleme, düzenlenmiş reseptörlerin hücre içinde çok farklı davrandığını ortaya koydu. Düzenlenmemiş kanser hücrelerinde EGFR hücre yüzeyinde oturur, EGF’yi yakalar ve ardından fosforilasyonla kimyasal olarak aktive olurken içeriye doğru hareket eder. Çift mutasyonu taşıyan klonlarda EGF bağlanması neredeyse tamamen ortadan kalktı ve EGFR artık zar üzerinde gözlenmedi; bunun yerine geriye kalan küçük miktardaki reseptör hücrenin iç kısmında birikti. Tek bir Y45 değişimi bile bağlanmayı büyük ölçüde azalttı ve toplam EGFR düzeylerini düşürdü. Yine de, bu ders kitabı EGF–EGFR sinyal yolunun bozulmasına rağmen kanser hücreleri kültürde canlı kalmaya ve yalnızca mütevazı hücre döngüsü değişiklikleri ile çoğalmaya devam etti.
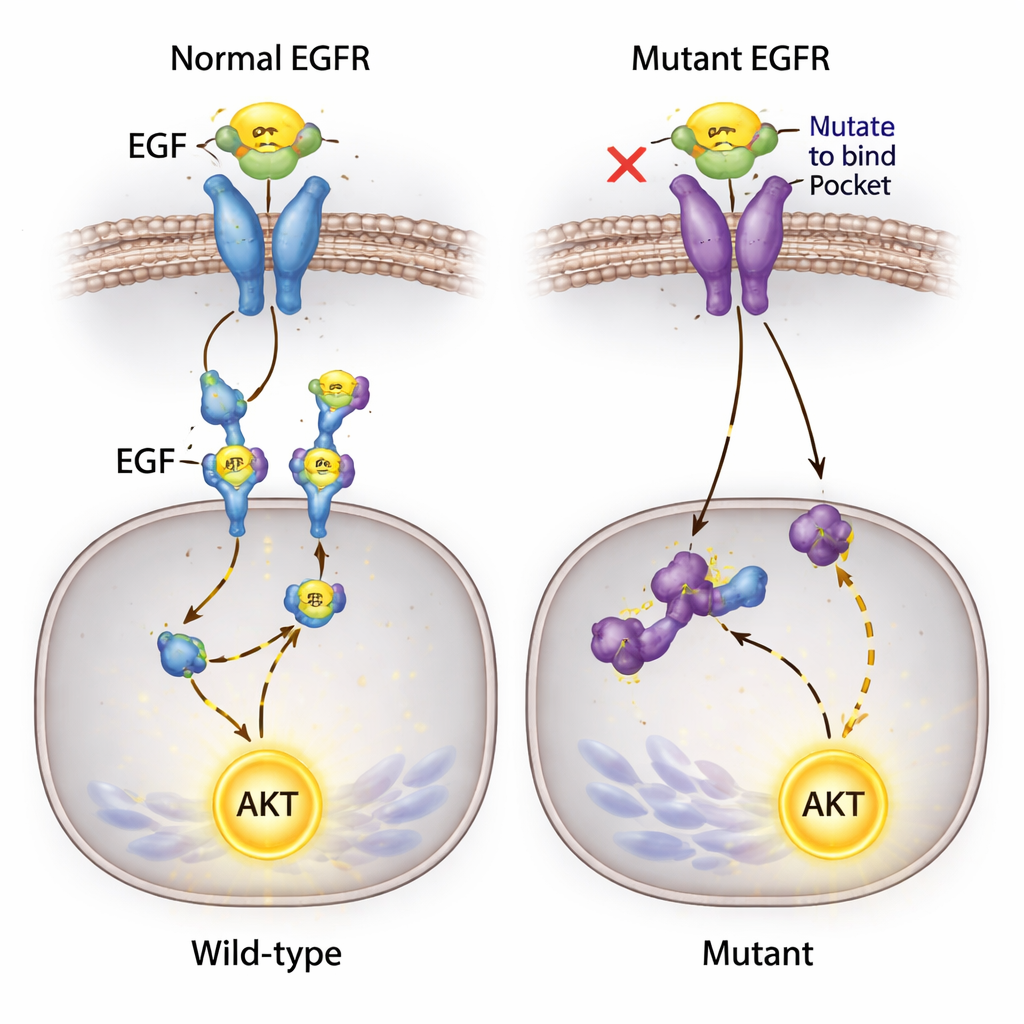
Sürmekten Vazgeçmeyen Beklenmedik Bir Sinyal
En şaşırtıcı bulgulardan biri, genellikle EGFR’nin aşağısında aktive olan hücre hayatta kalmasını destekleyen kilit bir protein olan AKT ile ilgiliydi. Araştırmacılar EGF–EGFR bağlanmasının bu yolu susturacağını bekliyordu. Bunun yerine ortama EGF eklediklerinde, AKT tüm hücre hatlarında güçlü biçimde aktive oldu—EGF’nin artık EGFR’ye bağlanamadığı ve reseptör fosforilasyonunun tespit edilemediği hücreler de dahil. Bu hücrelerin bilinen bir başka sinyal geninde, PIK3CA’da bir mutasyon taşıması nedeniyle ekip, EGF’nin AKT aktivasyonuna başka yüzey proteinleri veya arka plan mutasyonları aracılığıyla alternatif yollarla beslenmesine ve düzenlenmiş EGFR’yi devre dışı bırakarak atlatmasına izin veren yollar olabileceğinden şüpheleniyor.
Gizli Genetik Değişiklikler ve Gelecek Tedaviler
CRISPR’in yaygın istenmeyen düzenlemelere yol açmadığından emin olmak için bilim insanları yeni hücre hatlarının tüm genomlarını diziledi. İstenen EGFR mutasyonlarının mevcut olduğunu doğruladılar ve CRISPR kılavuzları için öngörülen hedef dışı bölgelerde kesiklere dair kanıt bulamadılar. Bununla birlikte genoma dağılmış birçok spontan mutasyon tespit ettiler; bunların bazıları hücrelerin davranışını etkileyebilir. Bu durum, CRISPR hedef adrese isabet etse bile kanser hücrelerinin doğal olarak istikrarsız DNA’sının deneysel sonuçların yorumunu ve hassas gen tabanlı tedavilerin tasarımını karmaşıklaştırabileceğini vurguluyor.
Hastalar İçin Anlamı Nedir
Halk için alınacak mesaj şudur: EGF ile EGFR arasındaki tokalaşmayı—atomik düzeyde çok hassas biçimde olsa bile—sadece engellemek, kanser hücrelerinin otomatik olarak “büyü ve hayatta kal” komutlarını almalarını durdurmaz. Çalışma, kanser hücrelerinin AKT aktivasyonu gibi anahtar sinyalleri bloke edilmiş bir reseptör etrafından yeniden yönlendirebileceğini ve CRISPR düzenlemesinin bu tür istikrarsız genomlarda dikkatle değerlendirilmesi gerektiğini gösteriyor. Bu tasarlanmış hücre hatları şimdi EGFR bağımlı tümörleri sürdüren yedek yolları araştırmak için güçlü bir laboratuvar modeli sağlıyor; bu bilgi nihayetinde hem EGFR’yi hem de onun gizli suç ortaklarını hedefleyen kombinasyon tedavilerine yol açabilir.
Atıf: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Anahtar kelimeler: EGFR, rahim ağzı kanseri, CRISPR, EGF sinyal iletimi, AKT yolu