Clear Sky Science · tr
Gen kopya sayısı artışı IFI30 aşırı ifadesini ve koordine bağışıklık aktivasyonunu tetikliyor; mide adenokarsinomunda yeni bir tanısal ve terapötik hedef tanımlanıyor
Neden bir mide proteini önem taşıyor
Mide kanseri, sıklıkla geç evrede tespit edilmesi ve tedavisinin zor olması nedeniyle dünyanın en ölümcül kanserlerinden biridir. Bu çalışma, bağışıklık sisteminin tehditleri tanımasına yardımcı olan hücrelerde bulunan ve az bilinen IFI30 adlı bir proteine odaklanıyor. Araştırmacılar, mide tümörlerinde IFI30’un nasıl değiştirildiğini ve vücudun savunmasını nasıl şekillendirdiğini izleyerek, bunun daha erken tanı ve daha etkili, kişiselleştirilmiş tedavi seçimleri için güçlü bir araç olabileceğini öne sürüyorlar.
Mide tümörlerinde gizli bir sinyal
Ekip önce basit bir soru sordu: IFI30 sağlıklı ve kanseröz mide dokusunda farklı düzeylerde mi bulunuyor? Binlerce örneğin gen aktivitesini birleştiren büyük halka açık veri kümelerini kullanarak, IFI30’un normal mide mukozasına kıyasla—midenin en yaygın kanser türü olan mide adenokarsinomunda—tutarlı biçimde çok daha yüksek olduğunu buldular. Bu bulgu, bağımsız hasta grupları ve hem RNA hem de protein düzeylerinde doğrulandı. Yazarlar IFI30’un tek başına tümör dokusunu sağlıklı dokudan ayırt etmedeki performansını değerlendirdiklerinde sonuç çarpıcıydı: tek bir belirteç için mükemmel sayılan 0,92’lik bir tanısal doğruluk (AUC). Mikroskop görüntüleri ayrıca IFI30’u, antijenlerin bağışıklık tanıması için işlendiği hücre içi geri dönüşüm sisteminin içinde konumlandırdı.
IFI30’u yükselten DNA değişiklikleri
Sonraki adımda araştırmacılar, IFI30’un bu tümörlerde neden bu kadar yükseldiğine baktılar. The Cancer Genome Atlas’tan kanser genomlarını taradıklarında, IFI30 geninin fazla kopyalarının—kopya sayısı amplifikasyonları olarak bilinen—aşırı ifadesinin ana sürükleyicisi olduğunu buldular. IFI30 amplifikasyonu olan tümörler genelde daha yüksek genom kararsızlığı gösteriyor ve sıklıkla TP53 ve PIK3CA gibi iyi bilinen kanser mutasyonlarını taşıyordu. IFI30 kopya sayısı arttıkça RNA düzeylerinin de yükselmesi, yapısal DNA değişiklikleri ile bu proteinin artan üretimi arasında doğrudan bir bağlantı olduğunu düşündürüyor. Bu, IFI30’u pasif bir gözlemci değil, daha agresif tümör biyolojisinin bir parçası olarak resmediyor.
Tümör etrafında bağışıklık etkileşimi
IFI30 antijenleri T hücrelerine "isteme posterleri" olarak sunan materyalin işlenmesinde yer aldığı için ekip, bunun tümör mikroçevresinde tam olarak nerede yer aldığını araştırdı. Tek hücre dizilemesi, genleri bireysel hücrelerde okuyan yöntem, IFI30’un özellikle dendritik hücrelerde, makrofajlarda ve CD8 T hücrelerinde—anti-tümör bağışıklığını başlatan ve sürdüren kilit oyuncularda—zenginleştiğini gösterdi. Ağ analizleri, IFI30 açısından zengin bağışıklık hücreleri ile çevreleyen tümör ve destek hücreleri arasında yoğun iletişim ortaya koydu. Yüksek IFI30’a sahip tümörler antijen sunumu, iltihap sinyalleri ve bağışıklık hücrelerini çeken ve organize eden haberleşme molekülleriyle ilişkili yolların güçlü şekilde aktive olduğunu gösterdi. Aynı zamanda, bu tümörler hücre döngüsünde hızlanma, doku yeniden düzenlenmesi ve düşük oksijene uyum gibi invazyon ve stres özellikleri sergileyerek IFI30’un kanser içinde saldırı ve savunmanın kesişim noktasındaki rolünü vurguladı.
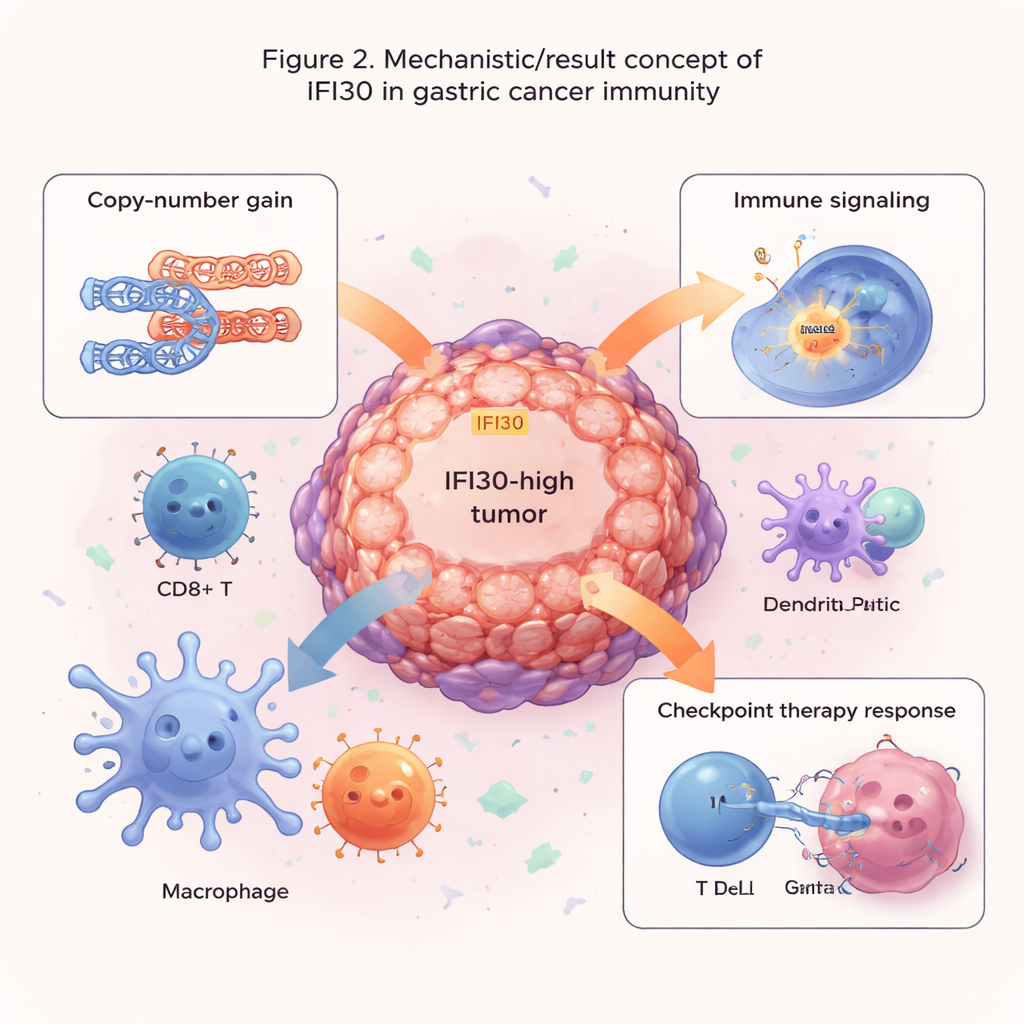
İlaç seçimi ve immünoterapi için ipuçları
Yazarlar daha sonra IFI30’un tümörlerin tedaviye nasıl yanıt verdiğini öngörmede yardımcı olup olmayacağını sordular. IFI30 düzeylerini büyük ilaç yanıtı veri kümeleriyle eşleştirerek, IFI30 yüksek tümörlerin hücre bölünmesini hedefleyen bazı ilaçlara veya yaygın bir büyüme yoluna (MAPK) yönelik ilaçlara karşı dirençli olma eğiliminde olduğunu, ancak EGFR ve PI3K/AKT sinyalini bloke eden ilaçlara karşı daha hassas göründüğünü buldular. Önemli olarak, IFI30 düzeyleri T hücreleri üzerinde önemli bir fren olan ve günümüzün kontrol noktası inhibitörleri tarafından hedeflenen PD-L1 ile yakından izledi. Birkaç immünoterapi çalışmasında, tümörleri daha yüksek IFI30 ekspresyonuna sahip olan hastalar düşük düzeydekilere kıyasla kontrol noktası blokajına daha yüksek yanıt gösterme eğilimindeydi. IFI30 tabanlı bir skor, tümör mutasyon yükü ve yalnızca PD-L1 gibi yerleşik ölçütleri geride bıraktı ve özellikle immünoterapilere daha iyi yanıt verdiği bilinen yüksek mikrosatellit instabilitesi taşıyan tümörlerde zenginleşti.
Laboratuvardan olası yeni hedefe
IFI30’un sadece bir belirteç mi yoksa kanser büyümesini de destekleyen bir etken mi olduğunu test etmek için ekip genetik araçlarla mide kanseri hücre hatlarında düzeylerini azalttı. IFI30 baskılandığında kanser hücreleri daha yavaş büyüdü; bu da tümör proliferasyonunun sürdürülmesinde doğrudan bir rolü işaret ediyor. Bir arada ele alındığında veriler, IFI30’un hem bağışıklık aktivitesinin bir göstergesi hem de kötü huylu davranışlara katkıda bulunan bir faktör olduğunu öne sürüyor. Hastalar için bu, basit bir IFI30 ölçümünün bir gün doktorların mide kanserini daha güvenilir tespit etmesine, hangi hastaların belirli hedefe yönelik ilaçlardan veya immünoterapilerden fayda sağlayacağını önceden tahmin etmesine ve belki de IFI30’un tümör teşvik edici etkilerini doğrudan veya dolaylı olarak engelleyen yeni tedavilere yol göstermesine yardımcı olabileceği anlamına geliyor.
Atıf: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Anahtar kelimeler: mide kanseri, IFI30, biyobelirteç, tümör immünitesi, immünoterapi