Clear Sky Science · tr
Ayrışmış biotin ligaz yaklaşımı, oligomerik alfa-sinükleine bağlı proteinleri agregasyon sırasında ortaya çıkarıyor
Neden birikmiş beyin proteinleri önemli
Parkinson hastalığı ve ilişkili durumlarda, normalde yardımcı olan bir beyin proteini olan alfa‑sinüklein, Lewy cisimcikleri olarak bilinen yapışkan birikintilere dönüşebilir. Bu birikintiler semptomlardan onlarca yıl önce ortaya çıkar ve otopside görülen ayırt edici bir özellik olmalarına rağmen, alfa‑sinükleini zararsız bir durumdan tehlikeli agregatlara iten diğer hangi proteinlerin rol oynadığını hâlâ bilmiyoruz. Bu çalışma, alfa‑sinüklein tek moleküllerden küçük kümelere geçerken yakınında hangi proteinlerin bulunduğunu haritalamak için zekice bir moleküler “yakınlık etiketi” kullanarak hastalığın nasıl başladığına ve hangi yolakların yavaşlatma veya önleme için hedeflenebileceğine dair yeni ipuçları sunuyor.
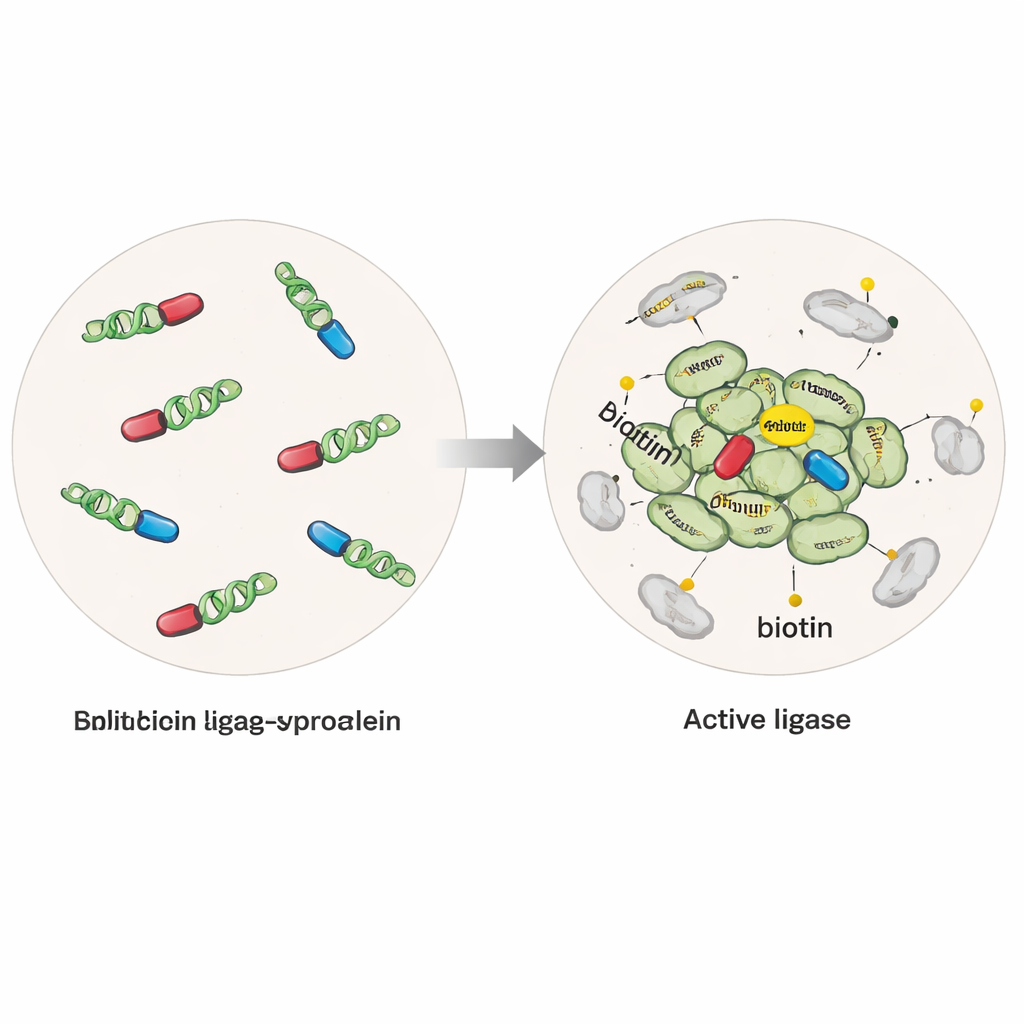
Komşuları aydınlatan moleküler bir “etiket”
Araştırmacılar, alfa‑sinükleini, birkaç milyarıncı metre içindeki herhangi bir proteine küçük bir biotin etiketi ekleyebilen modifiye bir enzimle füzyon halinde üretecek şekilde insan hücrelerini genetik olarak tasarladılar. Bir versiyonunda enzim sağlam ve aktiftı; alfa‑sinüklein bulunduğu her zaman tek moleküllerin yanı sıra kümelerin yakınındaki proteinleri yakalıyordu. İkinci, daha seçici “ayrılmış” versiyonda ise enzim iki inaktif yarıya bölünmüştü ve her yarı ayrı bir alfa‑sinüklein molekülüne bağlanmıştı. Yalnızca alfa‑sinüklein molekülleri multimere veya oligomere dönüşüp bir araya geldiğinde yarılar tekrar birleşip aktif bir enzim oluşturuyor ve etiketlemeyi özellikle bu erken agregatlar etrafında başlatıyordu. Saflaştırılmış alfa‑sinüklein fibrillerini hücrelere ekleyerek ekip, hastalığa benzeyen agregasyonu de tetikleyip normal ve patolojik durumları karşılaştırabildi.
Yakın proteinlerin bir haritasını oluşturmak
Etiketlemeye zaman tanıdıktan sonra ekip, tüm biotinle işaretlenmiş proteinleri çekti ve bunları kütle spektrometrisi kullanarak tanımladı; bu teknik proteinleri yüksek doğrulukla tartıp sayıyor. Tüm koşullar boyunca 1.277 farklı protein bulundu ve dikkatli filtrelemeden sonra alfa‑sinüklein yakınında gerçek olma olasılığı yüksek 581 proteine indirildi. Sağlam ve ayrılmış enzim sistemlerini karşılaştırarak, ağırlıklı olarak tek moleküllerle ilişki kuran proteinleri multimeleri tercih edenlerden ayırabildiler. Ayrıca agregasyon tetiklendiğinde alfa‑sinükleinin yerel protein ortamının nasıl değiştiğini görmek için fibril eklenen ve eklenmeyen hücreleri karşılaştırdılar.
Kümelere çekilen ana hücresel yolaklar
Ortaya çıkan etkileşim ağı taslağı birkaç ana biyolojik temayı işaret ediyor. Normal koşullarda, multimerik alfa‑sinüklein birçok membran‑taşıma proteini ve proteinleri modifiye eden enzimlerin yakınında yer alıyordu—bu, sinaptik veziküllerin yönetimi ve protein kalite kontrolünün sürdürülmesine yardımcı olma önerilen rolüyle uyumlu. PAK4, RIPK2 ve MAP4K4 gibi bazı fosfat grubu ekleyen kinazlar sağlıklı multimerlerin yakınında zenginleşmiş görünürken, agregatlar oluştuğunda temaslarını kaybediyormuş gibi görünüyordu; bu, bu ilişkilerin bozulmasının hastalıkla ilişkili form lehine olabileceğine işaret ediyor. Ekip ayrıca insülin benzeri büyüme faktörü sinyaline bağlı proteinleri tespit etti; bu, insülin direnci ile Parkinson hastalığı arasındaki klinik bağlantıları destekliyor ve agregasyonun 14‑3‑3 şaperon ailesi ve hücresel yıkım yolaklarının belirli bileşenleri gibi hasarlı proteinlerin bertaraf edilmesine dahil olan proteinleri işe kattığını buldu.
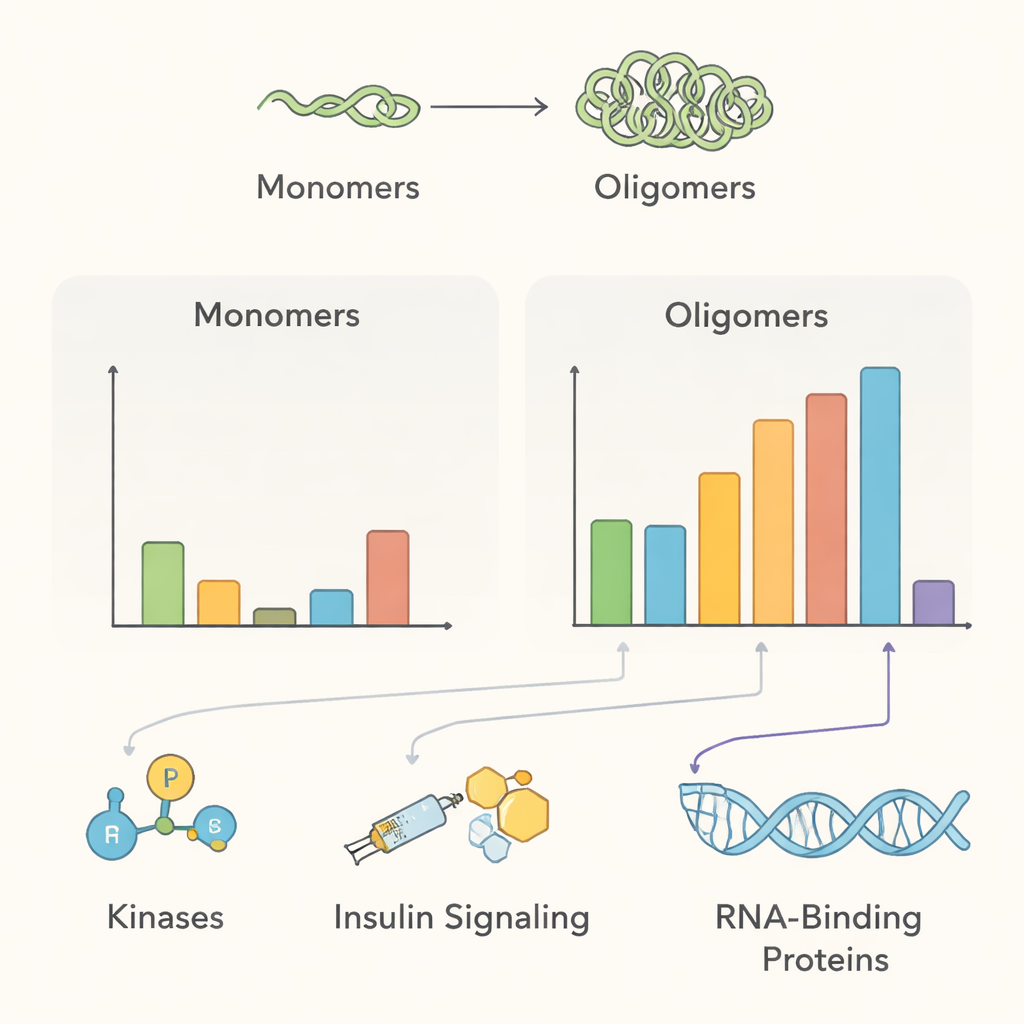
Diğer beyin bozukluklarına beklenmedik köprüler
Parkinson hastalığının ötesinde, veriler amyotrofik lateral skleroz (ALS) ve frontotemporal demans (FTD) ile şaşırtıcı bir bağlantıyı vurguluyor. O koşullarda yanlış yer değiştiren ve agregasyon gösteren bir RNA‑bağlayıcı protein olan FUS, normal ve agregasyon tarafından tetiklenen koşullar altında multimerik alfa‑sinükleinin yakınında görünüyordu. Diğer RNA ile ilişkili proteinler de alfa‑sinüklein agregasyonu sırasında yakınlıklarını değiştirdi. Bu bulgular, küçük alfa‑sinüklein birleşimlerinin RNA işlemleyen proteinleri hücre içinde yanlış yere hapsedebileceği olasılığını gündeme getiriyor; bu da Lewy cisimciği hastalıklarının biyolojisini ALS ve FTD ile potansiyel olarak ilişkilendirebilir, ancak doğrudan fiziksel etkileşimlerin hâlâ doğrulanması gerekiyor.
Hastalığı anlamak için anlamı
Uzman olmayanlar için ana çıkarım, bu çalışmanın alfa‑sinüklein normal bir yardımcıdan zararlı bir kümeye dönüşürken onunla birlikte seyahat eden proteinlerin erken aşama bir “iletişim listesi”ni sağladığıdır. Çalışma, belirli kinazlar veya kalite kontrol enzimleriyle olan koruyucu ilişkilerin kaybının, yeni toksik ortaklar edinmek kadar önemli olabileceğini öne sürüyor. Deneyler basitleştirilmiş bir hücre modelinde yapıldığı ve henüz nedensellik kanıtlamadığı halde, nöronlar ve beyin dokusunda gelecekteki testler için somut adaylar ve yolakları öne çıkarıyor. Uzun vadede, değişen bu protein mahallelerini haritalamak koruyucu etkileşimleri yeniden kurma, insülinle ilişkili sinyali destekleme veya RNA‑bağlayıcı proteinlerin yakalanmasını önleme stratejilerine yol gösterebilir ve moleküler düzeydeki ince değişikliklerden tam gelişmiş Lewy cisimciği hastalıklarına geçişi yavaşlatma potansiyeli taşıyabilir.
Atıf: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Anahtar kelimeler: alfa-sinüklein, Lewy cisimciği hastalığı, protein agregasyonu, yakınlık proteomikleri, Parkinson hastalığı