Clear Sky Science · tr
Atım Frekanslı Düşük Frekanslı Darbeli elektromanyetik alanın (PEMF) mitokondrilerle etkileşimi
Nazik Alanlar ve Hücrenin Güç Merkezleri
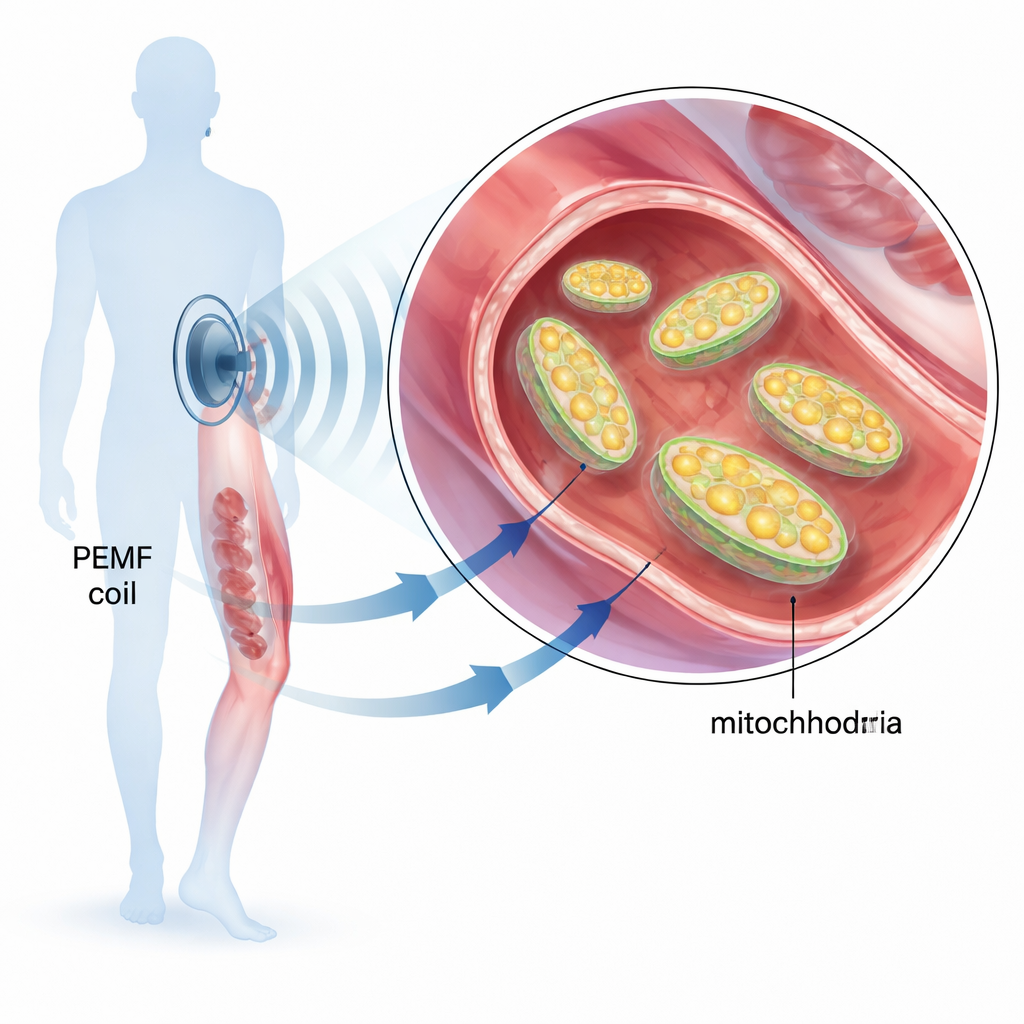
Darbeli elektromanyetik alan (PEMF) tedavisi, kırıkların kaynamasına yardım etmek, eklem ağrısını hafifletmek ve ameliyat sonrası iyileşmeyi hızlandırmak için kliniklerde zaten kullanılıyor. Yine de bu nazik, düşük frekanslı alanların vücudumuz içinde nasıl etki ettiğini tam olarak anlamış değiliz. Bu çalışma basit ama önemli bir soruyu gündeme getiriyor: PEMF sinyalleri doğrudan hücrelerimizin içindeki, enerjimizin çoğunu üreten küçük güç santralleri olan mitokondrileri etkiliyor mu, etkiliyorsa nasıl?
Mitokondrilerin Günlük Sağlık İçin Önemi
Mitokondriler, yiyecek ve oksijeni ATP molekülüne dönüştürür; ATP hücrelerin evrensel “enerji birimi”dir. Mitokondriler aksadığında dokular daha yavaş iyileşir, kaslar daha çabuk yorulur ve zayıf metabolizma ile ilişkili hastalıklar kötüleşebilir. Önceki araştırmalar PEMF tedavilerinin enerji metabolizmasını iyileştirebileceğine ve doku onarımını destekleyebileceğine işaret ettiğinden, yazarlar belirli bir PEMF cihazının mitokondriyal aktiviteyi ayarlayıp ayarlayamayacağını incelediler. Bunun için iyi tanımlanmış bir manyetik sinyal kullandılar: düşük giriş enerjili, 30 kHz’lik sinüs dalgasının milisaniye uzunluğunda kısa darbeleri; bunları kültürdeki kas hücrelerine, sıçan dokularına ve saflaştırılmış mitokondrilere uyguladılar.
Canlı Hücrelerin İçine Daha Yakından Bakmak
Laboratuvarda yetiştirilen insan kas hücrelerinde ekip PEMF maruziyetinden sonra üç ana göstergeyi ölçtü: mitokondri iç zarındaki elektrik potansiyeli (küçük bir pil gibi), reaktif oksijen türleri düzeyleri (yüksek düzeyler zararlı olabilir) ve mitokondriyal solunumu geçici olarak engelleyebilen bir gaz olan azot monoksit. Tedaviden yaklaşık 90 dakika sonra mitokondri zar potansiyeli hafifçe azaldı; azot monoksit seviyeleri düştü; reaktif oksijen türleri artmadı. Zar potansiyelindeki küçük düşüş ya hasaret ya da ATP üretiminin daha yoğun çalıştığının bir işareti olabilir. Hücrelerde stres belirtisi görülmediğinden, yazarlar mitokondrilerin muhtemelen biraz daha hızlı çalıştığını ve iç zarlarındaki voltajı daha fazla kullandığını düşündüler.
Mitokondrilerin Nefes Alma Şeklini Test Etmek
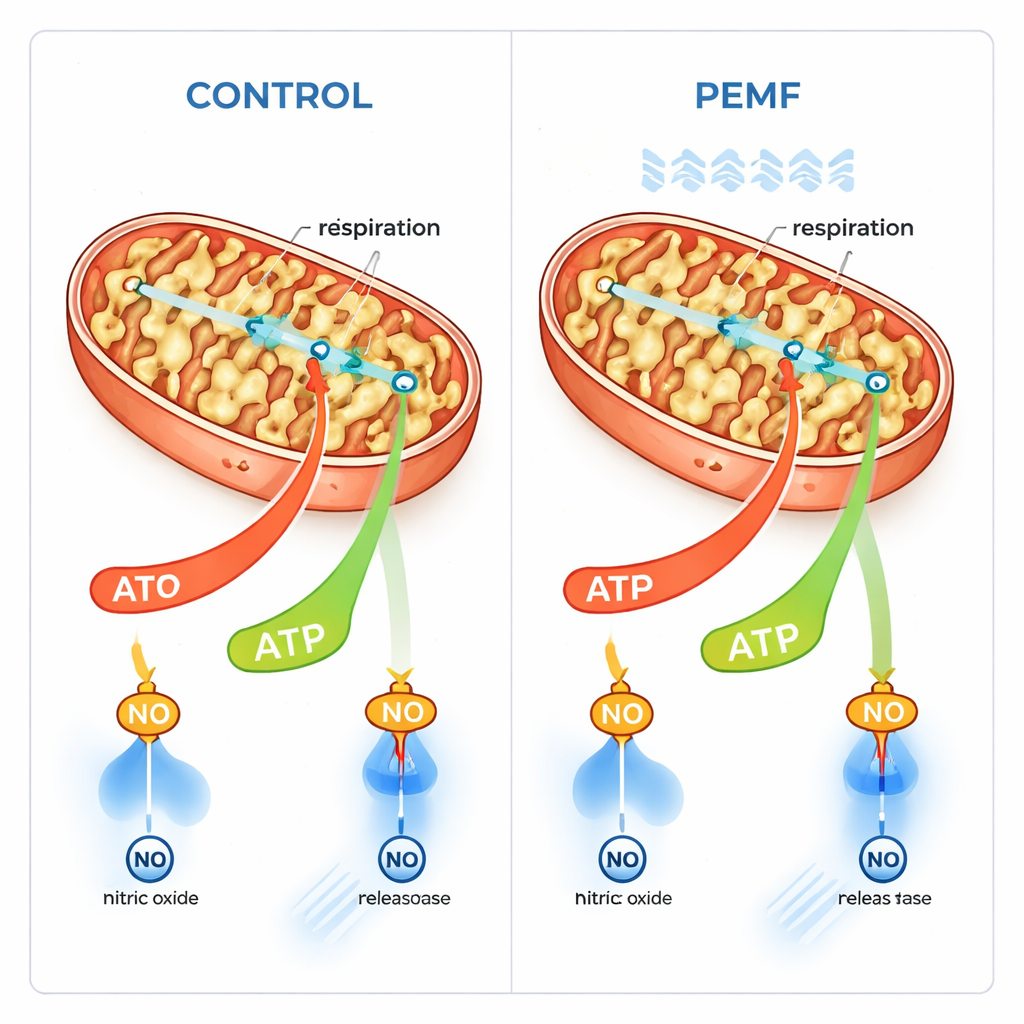
Bu fikri daha doğrudan sınamak için araştırmacılar, mitokondrilere farklı yakıtları hassas şekilde verip oksijen kullanımını ölçebilmeleri için dış hücre zarını nazikçe delinerek geçirgen hale getirdiler. PEMF sonrası özellikle glutamat varlığında, ATP üretimine bağlı solunumda daha yüksek bir eğilim gözlemlediler. Çok sayıda örnek üzerinde yapılan istatistiksel analiz, PEMF maruziyeti ile yakıt seçiminin mitokondrilerin oksijen tüketme hızını anlamlı şekilde şekillendirdiğini gösterdi. Önemli olarak, PEMF’nin hücrelere veya mitokondrilere zarar verdiğine dair hiçbir belirti yoktu. Bunun yerine alanlar, oksijen kullanımının ATP üretimiyle sıkı bağ içinde olduğu “bağlı” solunum modunu seçici olarak uyarmış gibi görünüyordu; gereksiz, bağlanmamış yakıt yakımını artırmadan.
İnflamasyon, Azot Monoksit ve Mavi Işıktan Gelen Bir Sürpriz
Azot monoksit inflamasyon sırasında birikebilir ve mitokondriyal solunumdaki kilit bir adımı bloke edebilir; bu yüzden ekip, PEMF’nin böyle bir inhibisyondan sonra mitokondrilerin toparlanmasına yardımcı olup olmayacağını sorguladı. Kas ve karaciğer doku homojenatlarına ve izole karaciğer mitokondrilerine kimyasal bir azot monoksit verici eklediler; bu, solunumu güçlü biçimde yavaşlattı. Bu koşullar altında, mitokondriler yüksek yoğunlukta olsa bile PEMF mitokondriyal fonksiyonu geri getirmedi. Bloğun tamamen geri çevrilebilir olup olmadığını görmek için, azot‑monoksit‑ile inhibe edilmiş mitokondrilere bilinen şekilde azot monoksiti bağlandığı yerden sökebilen bir yöntemle mavi ışık tuttular. Mavi ışık solunumu kısmen kurtardı; bu sistemin toparlanabileceğini doğruladı, fakat PEMF ekstra bir fayda sağlamadı. Bu, PEMF’nin olumlu etkilerinin inflamasyon benzeri koşullarda azot monoksidi gidermesinden kaynaklanmadığını gösterdi.
Zarlı Kapılar ve Enerji Akışı
Hücreleri elektrik devrelerine benzeten yazarlar, PEMF’nin esasen biyolojik zarlar üzerinde etkili olabileceğini öne sürüyor. Mitokondriler, enerjiyle ilgili moleküllerin içeri ve dışarı geçişine izin veren VDAC adlı anahtar bir geçit proteini içeren bir dış zarla sarılıdır. İç zarın çok yüksek voltajının aksine dış zar daha küçük ve daha kolay etkilenebilir bir voltaja sahiptir. Yazarlar, PEMF’nin bu dış zar potansiyelini ince şekilde değiştirerek VDAC kapılarının açık kalma sıklığını kaydırabileceğini ve böylece yakıt ile tüketilmiş ATP’nin zar boyunca akışını kolaylaştırabileceğini öneriyor. Bu, elektron taşıma makinesinin maksimum kapasitesini değiştirmeden bağlı, ATP üreten solunum modunu doğal olarak artırır.
Gelecek Terapiler İçin Anlamı
Genel olarak çalışma, bu tip PEMF’nin mitokondrilere zararlı olduğuna dair kanıt bulmuyor. Aksine, PEMF mitokondriyal solunumun ATP üreten kısmını nazikçe güçlendirirken maksimum solunum kapasitesini ve oksidatif stresi değişmeden bırakıyor. Ancak yüksek azot monoksiti ile bloke edilmiş mitokondrileri kurtarmıyor; bu da inflamasyonlu dokulardaki faydalarının başka yollardan kaynaklanmak zorunda olduğunu gösteriyor. Hastalar ve klinisyenler için bu sonuçlar, özenle ayarlanmış elektromanyetik alanların hücrenin güç merkezlerini daha verimli, enerji üreten bir duruma doğru yönlendirebileceği fikrini destekliyor—kemik onarımı, yara bakımı ve ameliyat sonrası iyileşme gibi alanlarda bildirilen bazı iyileştirici etkiler için makul, mekanistik bir açıklama sunuyor.
Atıf: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Anahtar kelimeler: darbeli elektromanyetik alan tedavisi, mitokondri, hücresel enerji, azot monoksit, ATP üretimi