Clear Sky Science · tr
GJB2 c.109G > A mutasyonu, IFI27 aracılı mitokondriyal apoptoz yolunu aktive ederek kalıtsal non-sendromik işitme kaybına yol açıyor
Çocukların geleceği için küçük kulak hücreleri neden önemli
Doğumda var olan işitme kaybı dünya çapında milyonlarca çocuğu etkiler ve sıklıkla konuşmayı öğrenme, okul başarısı ve başkalarıyla bağlantı kurma biçimlerini belirler. En yaygın genetik nedenlerden biri GJB2 adlı gendir, ancak bu gendeki değişikliklerin iç kulağa nasıl zarar verdiği tam olarak anlaşılmamıştır. Bu çalışma, zebrafish ve insan hücreleri kullanarak GJB2’deki tek bir DNA değişikliğinden hassas ses algılayıcı hücrelerin ölümüne kadar giden olay zincirini izliyor ve gelecekteki tedaviler için potansiyel bir hedef olarak IFI27 adlı yeni bir moleküle işaret ediyor.
Çocukluk dönemindeki sessizliğin arkasındaki yaygın gen değişikliği
Araştırmacılar, Çin’in Fujian Eyaleti’nde kalıtsal işitme kaybından şüphelenilen 1.199 çocuğun kan örneklerini tarayarak işe başladı. Birkaç iyi bilinen işitme sağırlık genine odaklandılar ve tespit edilen değişikliklerin %85’inin GJB2’de olduğunu buldular. Bunlar arasında c.109G>A (p.Val37Ile olarak da bilinir) adlı özgül bir değişiklik en sık görüleniydi. Bu varyant genel nüfusta nispeten yaygın olmasına rağmen işitme kaybı olan kişilerde güçlü şekilde zenginleşmiş olarak bulundu; bu da onun diğer tıbbi sorunlar eşlik etmeden görülen non-sendromik işitme kaybında önemli bir rol oynadığını düşündürüyor.
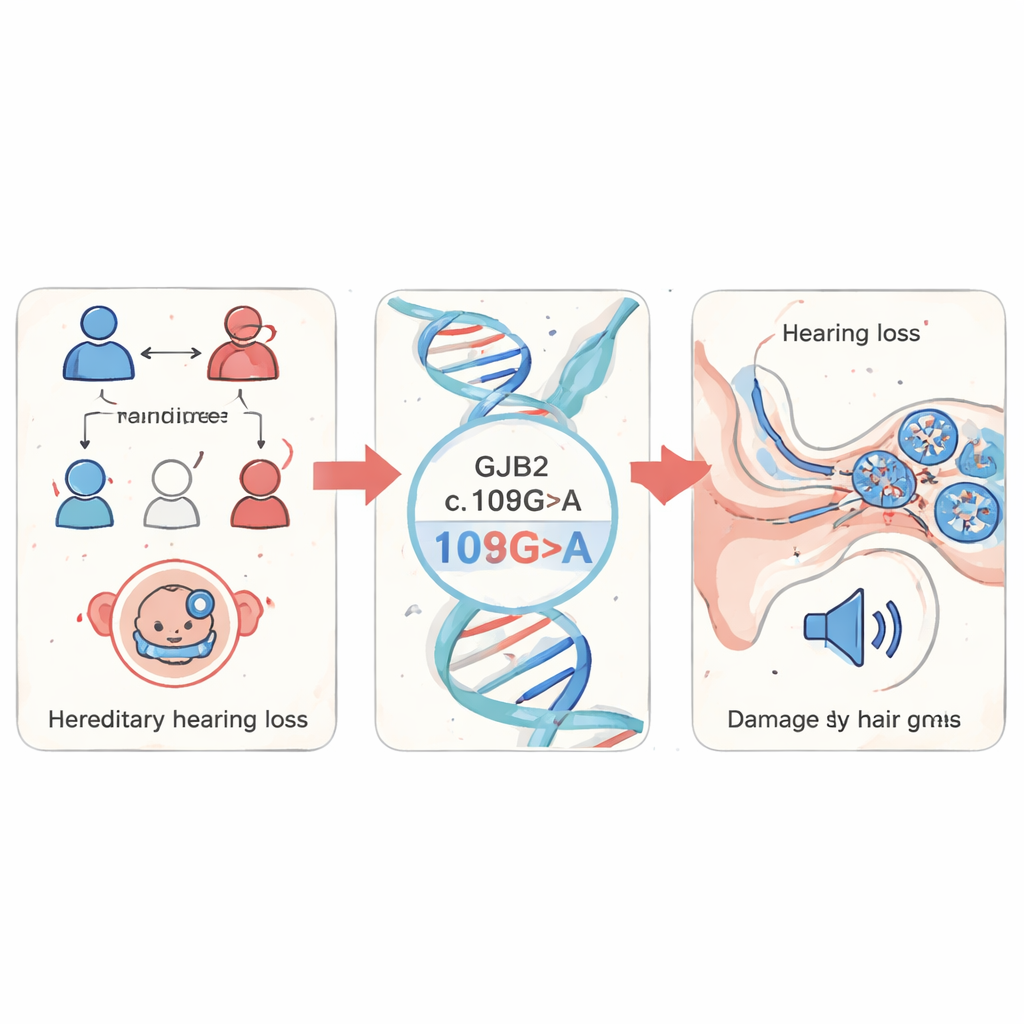
Şeffaf bir balıkta hasarı izlemek
Bu mutasyonun canlı bir organizmada ne yaptığını görmek için ekip, embriyoları şeffaf olan ve birçok gen ile kulak yapısı insanlarla ortak olan küçük bir tatlı su balığı olan zebrafish’e yöneldi. Zebrafish embriyolarını normal insan GJB2 veya c.109G>A mutant versiyonunu üretecek şekilde mühendislik ile değiştirdiler ve ayrıca balığın kendi gjb2 genini azaltmak için “knockdown” yaklaşımı kullandılar. Mutant veya azaltılmış gen taşıyan embriyolar büyüme gecikmesi, kıvrık kuyruklar ve kalp çevresinde şişme gibi gelişimin aksadığına işaret eden belirtiler gösterdi. En önemlisi, iç kulakları belirgin şekilde anormaldi: otolitler daha küçük ve birbirinden daha uzak, sıvı dolu kohlear bölge ise küçülmüştü. Bilim insanları mutantla birlikte normal GJB2 eklediklerinde, bu yapısal sorunların birçoğu düzeldi; bu da kusurları sürükleyen etkenin mutasyonun kendisi olduğunu gösterdi.
Arızalı kulaklardan zayıf işitme davranışına
İşitme, ses titreşimlerini sinir sinyallerine çeviren küçük “tüy hücrelerine” bağlı olduğundan, ekip zebrafish’te bu hücreleri boyadı. GJB2 mutasyonu veya knockdown olan balıklarda hem iç kulakta hem de su hareketini algılayan vücut yüzeyinde çok daha az tüy hücre görüldü. Araştırmacılar daha sonra balıkların sese nasıl yanıt verdiğini test etti. Otomatik bir izleme sistemi kullanarak, 5 günlük larvaların kısa ses patlamalarına maruz kaldıklarında ne kadar uzağa ve ne kadar hızlı yüzdüklerini ölçtüler. Normal ve vahşi tip GJB2 balıkları daha fazla ve daha hızlı yüzerek tepki verirken, mutant ve knockdown balıkların davranışında neredeyse hiç değişiklik olmadı; bu da işitme bozukluğunu gösteriyor. Yine, normal GJB2 eklenmesi hem tüy hücresi sayısını hem de sesle tetiklenen hareketi kısmen geri getirdi.
Hücresel enerji santrallerinde ölümcü bir yol
Hücrelerin içinde neler olduğunu anlamak için bilim insanları normal zebrafish ile reduced gjb2’ye sahip olanların gen aktivitesini karşılaştırmak amacıyla RNA dizilemesi kullandı. “Mitokondriyal apoptoz yolu” ile ilişkili bir gen seti—hücrenin enerji fabrikalarına odaklanan kendi kendini yok etme rotası—güçlü şekilde aktive olmuştu. Özellikle IFI27 ailesinin birkaç üyesi ve Bax, sitokrom c, Apaf1 ve kaspazlar gibi iyi bilinen hücre ölümü elemanları öne çıktı. İnsan HEK293 hücrelerindeki takip deneyleri bu deseni doğruladı: mutant GJB2 taşıyan hücreler daha fazla reaktif oksijen türü (ROS, oksidatif stres biçimi) üretti, mitokondrilerden daha fazla sitokrom c salındı ve apoptoz proteinleri etkinleşti, bunun sonucunda hücre ölümü arttı. Araştırmacılar mutant geni taşıyan hücrelerde IFI27’yi susturduğunda ROS düzeyleri düştü, ölüm sinyalleri zayıfladı ve daha az hücre apoptoz yaşadı.
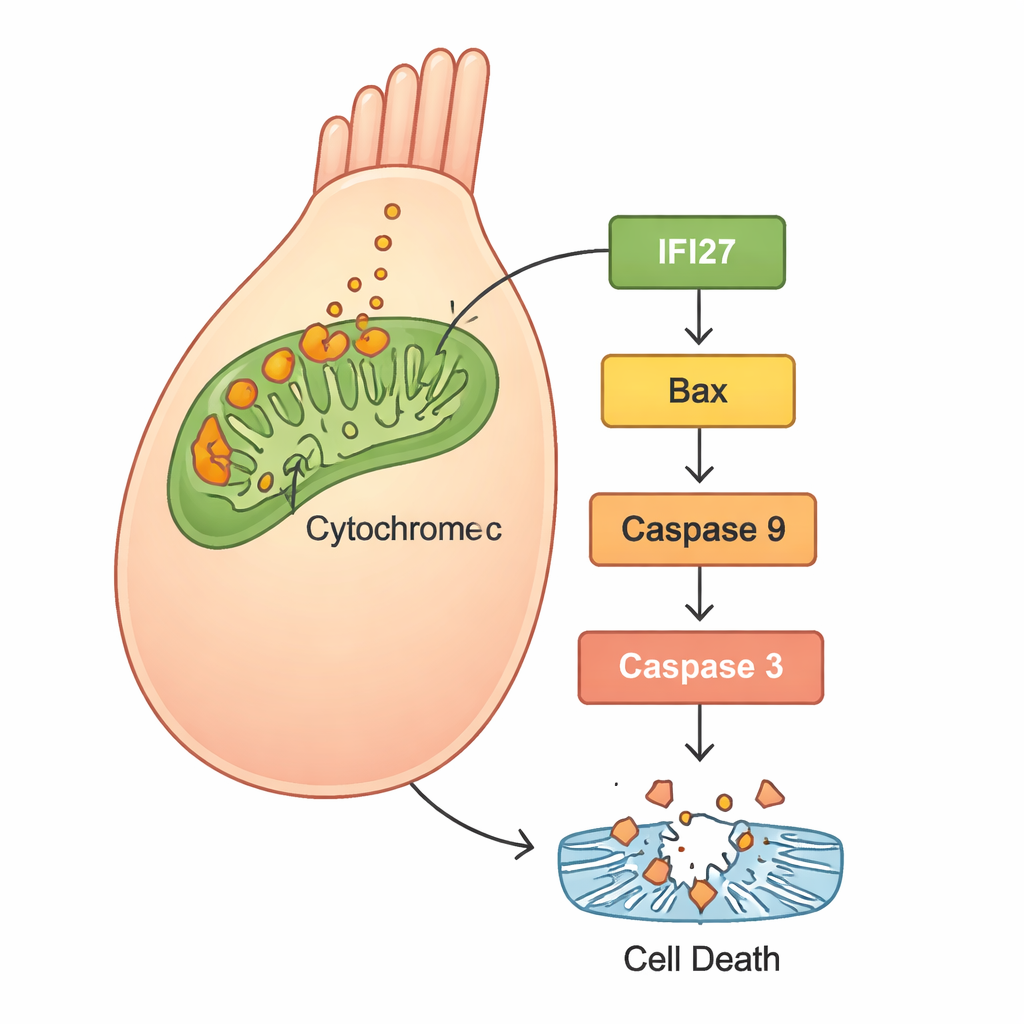
Gelecekteki tedaviler için bunun anlamı
Birlikte ele alındığında bulgular net bir hikaye öneriyor: GJB2 c.109G>A mutasyonu, hücresel iletişimi değiştirmesinin yanı sıra mitokondri içinde stres tetikleyerek normal iç kulak gelişimini ve işlevini bozuyor. Bu stres IFI27 ve ilgili genleri yükseltiyor, sitokrom c salınımına yol açıyor ve tüy hücrelerini programlı hücre ölümüne iten bir protein kaskadını aktive ediyor. Tüy hücreleri insanlarda kolaylıkla geri büyümediği için kayıpları kalıcı işitme kusurlarına yol açıyor. IFI27’yi azaltmanın insan hücrelerinde bu yıkıcı kaskadı hafiflettiğini göstermesi, IFI27’yi ilaçlar veya gen tabanlı tedaviler için umut verici bir hedef olarak öne çıkarıyor. Bu tür tedaviler hâlâ gelecekte ve büyük olasılıkla yaşamın çok erken döneminde verilmesi gerekecek olsa da, bu çalışma bir zamanlar gizemli olan bir gen mutasyonunu çocukluk sağırlığının potansiyel olarak önlenebilir bir nedeni haline getirebilecek somut bir moleküler yol haritası sunuyor.
Atıf: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
Anahtar kelimeler: genetik işitme kaybı, GJB2 mutasyonu, zebrafish modeli, mitokondriyal apoptoz, IFI27