Clear Sky Science · tr
İnsan epitelyal hücrelerinde yüksek saha bant genişliğinde terahertz dalgalarının termal olmayan etkisiyle DNA çift sarmal kırıkları yoluyla verimli apoptoz
Kanser Hücrelerini Yok Etmeye Dair Yeni Bir Işık
Kanser tedavileri sıklıkla ince bir çizgide yürür: tümör hücrelerini yok ederken sağlıklı doku veya bağışıklık sistemine ciddi zarar vermemelidir. Bu çalışma bu iş için sıra dışı bir aracı inceliyor—mikrodalga ile kızılötesi arasındaki görünmez ışık türü olan yoğun terahertz (THz) dalgaları. Araştırmacılar, dikkatle ayarlanmış yüksek saha THz darbelerinin dokuyu "pişirmeden" veya iltihaba yol açan dağınık hücre ölümü oluşturmak yerine kanser hücrelerini kontrollü biçimde "intihara" götürebileceğini gösteriyor.
Nazik Hücre Ölümünün Önemi
Birçok yaygın kanser terapisi hücreleri ölüme iter, ancak genellikle yan hasara yol açar. İlaçlar ve biyolojik ajanlar tümörler direnç geliştirdikçe etkinliğini kaybedebilir ve bağışıklık sistemini zayıflatabilir. X ışınları, radyoaktivite veya ısı kaynaklı ablasyon gibi fiziksel yöntemler çevredeki sağlıklı dokulara zarar verebilir ve sıklıkla nekroza—iltihap ve ağrı tetikleyen şiddetli bir hücre ölümü biçimi—yol açar. Hücrelerin sessizce kendi kendini parçaladığı, düzenli bir otoyıkım süreci olan apoptozu tetikleyen bir yöntem, özellikle cilde yakın tümörleri küçültmek için çok daha az travmatik bir yol sunabilir.
Terahertz Dalgalarının Meme Kanseri Hücreleriyle Buluşması
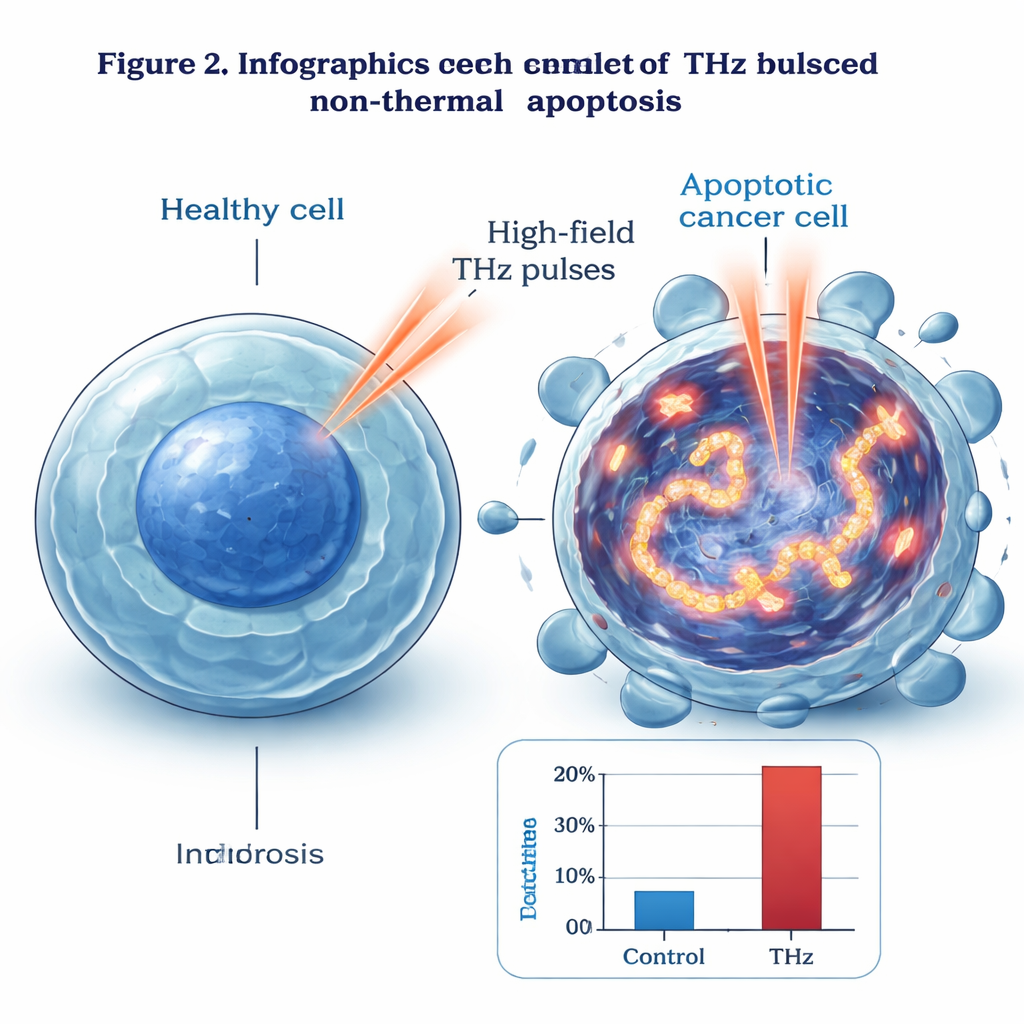
Çalışma ekibi laboratuvarda sıkça kullanılan bir epitelyal hücre türü olan insan meme kanseri hücreleri (MCF‑7) üzerinde yoğunlaştı. Bu hücreleri normal vücut sıcaklığında tutarak oldukça güçlü, bant genişliğinde THz darbelerine dört saate kadar maruz bıraktılar. Alan şiddetleri günlük cihazlardakinden çok daha yüksek, santimetre başına birkaç milyon volta ulaştı. Bu koşullar altında apoptoza giren hücre oranı maruz kalma süresiyle birlikte düzenli olarak arttı. Test edilen en yüksek THz yoğunluğunda neredeyse %99 oranında kanser hücresi apoptoza girerken, %1’den azı nekrozla öldü. Bu büyük ve temiz programlı hücre ölümü dalgası, THz darbelerinin hücreleri yalnızca ısıtmaktan daha fazlasını yaptığını gösteriyor.
Isıtma Dışı Etkiler ve Güvenli Sıcaklık Sınırları
Su THz radyasyonunu güçlü biçimde soğurduğundan, akla gelen endişe kazara ısınmadır. Bilim insanları ışınlama sırasında sıcaklık değişimlerini takip etmek için termal görüntüleme kullandılar. Orta yoğunlukta dört saat sonra bile kanser hücreleri yalnızca yaklaşık 3 °C ısındı ve nekroz %4’ün altında kaldı. Hücrelerin dört saat boyunca yalnızca ısıtıldığı ayrı kontrol deneyleri, 41 °C’nin altındaki sıcaklıklarda neredeyse hiç ölüm olmadığını, 43 °C’nin üzerinde ise nekrozda keskin bir artış görüldüğünü gösterdi. En yoğun THz ayarlarında bile araştırmacılar hücre sıcaklıklarını bu 43 °C eşiğinde ya da altında tuttular ve hâlâ minimum nekrozla neredeyse tam apoptoz gözlemlediler. Darbelerin tekrarlanma hızını düşürerek sıcaklığın kontrol altında tutulabileceğini ancak güçlü antitümör etkilerin korunabildiğini gösterdiler; bu da termal olmayan bir mekanizmanın devrede olduğunu vurguluyor.
DNA’yı Çalkalayarak Ölüm Genlerini Açmak
Mekanizmayı bulmak için ekip hücrenin içini inceledi. Elektron mikroskobunda THz uygulanmış hücreler apoptozun klasik erken belirtilerini gösterdi: yoğunlaşmış genetik materyal, değişmiş çekirdekler ve bütün dış zarlar. γ‑H2AX adlı floresan bir belirteç kullanılarak DNA’da yaygın çift zincir kırıkları tespit edildi—ışınlanmış hücrelerde bu hasar, işlem görmemiş veya hafif ısıtılmış kontrol gruplarına kıyasla çok daha sık rastlandı. Hasar deseni THz ışınının yoğunluk profiline uydu ve merkeze doğru güçlendi. Gen ve protein analizleri, GADD45B ve c‑Jun gibi stres ve hasara yanıt veren moleküllerin güçlü biçimde aktive olduğunu, oysa p53 ve birçok kaspaz dahil geleneksel hücre ölümü yollarının bilinen oyuncularında büyük değişimler olmadığını ortaya koydu. Yazarlar, yoğun THz alanlarının DNA’da şiddetli titreşimsel "rezonanslar" oluşturarak çift sarmalı fiziksel olarak zorlayıp kırıyor ve ardından p53 ve kaspaz bağımsız, ayrı bir apoptoz yolunu tetikliyor olabileceğini öneriyorlar.
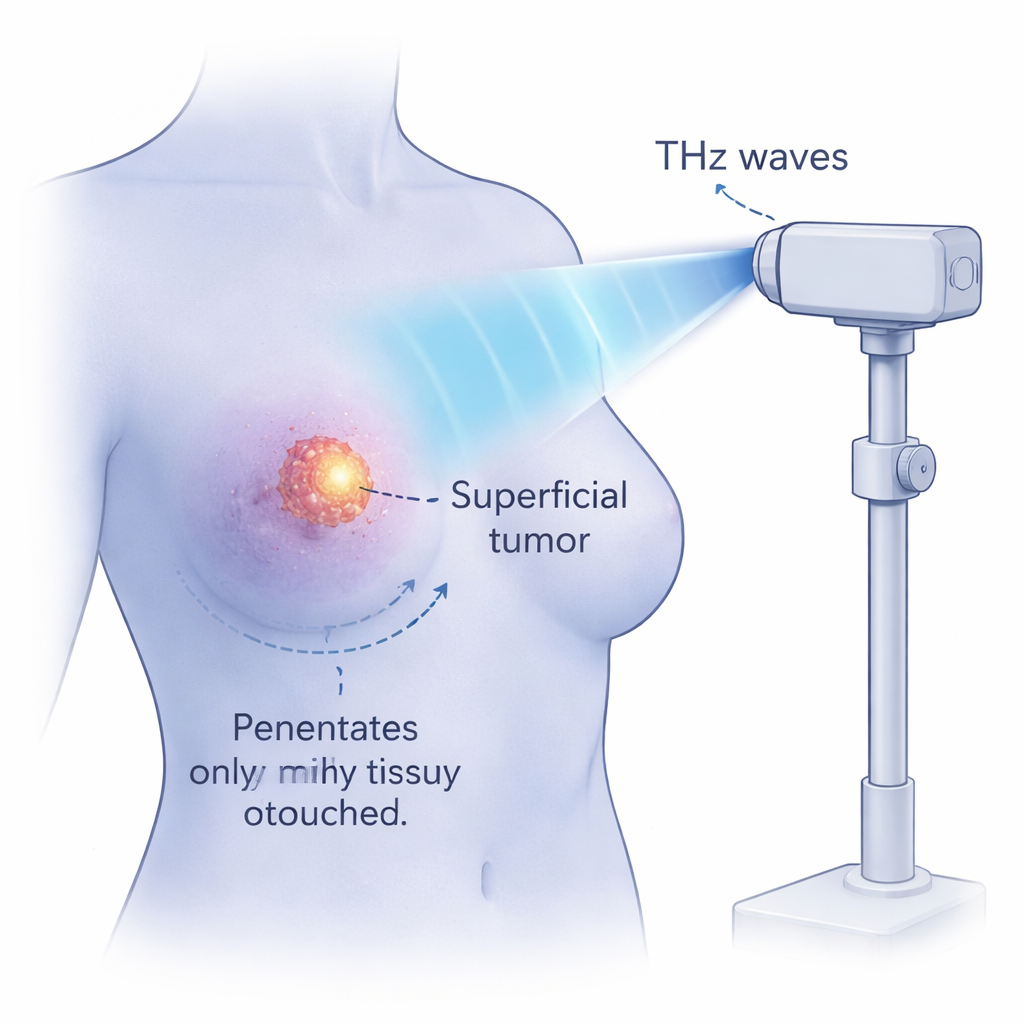
Plakadan Gelecek Terapilere
Bu deneyler hücre kültürlerinde yapılmış olsa da, yeni bir fiziksel kanser terapisi tarzına işaret ediyorlar. Yüksek saha THz dalgaları nemli dokuya birkaç milimetre kadar nüfuz edebiliyor—yüzeysel tümörlere ulaşmak için yeterli—ama hızla zayıflıyor, böylece daha derin organların korunması mümkün olabilir. Etki büyük ölçüde termal olmadığından, teoride çevre dokuyu yakmadan veya güçlü iltihap tetiklemeden kanser hücrelerini katman katman öldürebilir. Yapılacak çok iş var: önerilen DNA "rezonans" mekanizması doğrulanmalı, normal hücreler için güvenlik kapsamlı şekilde test edilmeli ve hayvan ile klinik çalışmalar gereklidir. Yine de bu araştırma, biyomoleküllerin doğal hareketlerine ayarlanmış dikkatle tasarlanmış ışık darbelerinin bir gün belirli kanserleri hassas ve nispeten nazik bir şekilde yok etmek için kullanılabileceği fikrinin kapısını aralıyor.
Atıf: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Anahtar kelimeler: terahertz kanser terapisi, termal olmayan apoptoz, DNA çift zincir kırıkları, meme kanseri hücreleri, fiziksel tümör ablasyonu