Clear Sky Science · tr
Manyetik nanoparçacık tabanlı onkoloji için genelleştirilmiş kan damarı modelleri: geometrik ve mikroakışkanlık özellikleri
Vücudu Kateden Küçük Mıknatısları Yönlendirmek
Bir mıknatıs kullanarak kanser ilaçlarını doğrudan bir tümöre çekebilseydik, geri kalan vücudu zararlı yan etkilerden koruyabilirdik. Bu çalışma, küçük manyetik parçacıkların kan damarı benzeri ağlar içinde nasıl hareket ettiğini inceliyor ve aldatıcı derecede basit bir soruyu soruyor: gerçekçi akış koşulları altında mıknatıslar, bu parçacıkları doktorların istediği yere gerçekten yönlendirebilir mi?
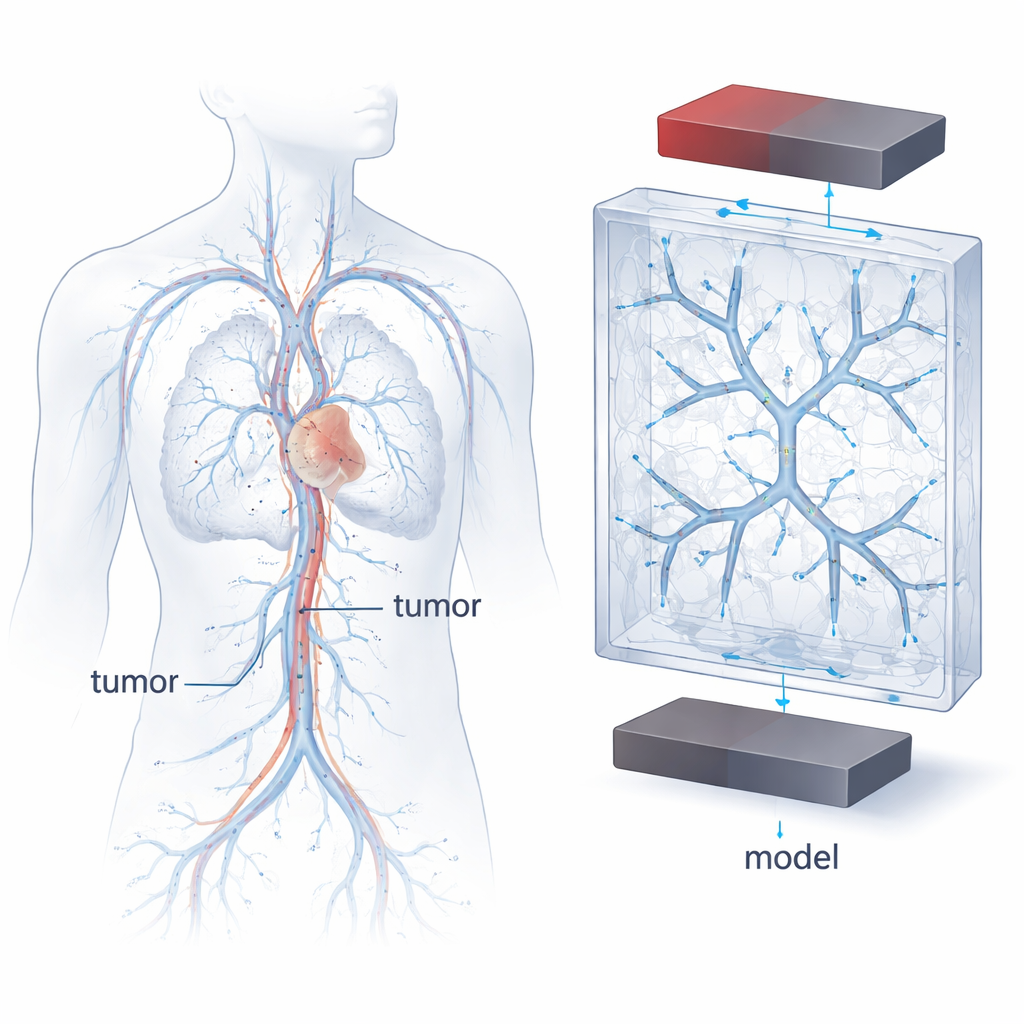
Neden Damar Geometrisi ve Akış Önemli?
Manyetik kanser tedavileri, kan dolaşımı boyunca ilaç taşırken manyetik alan tarafından çekilebilen süperparamanyetik demir oksit nanoparçacıklara (SPION) dayanır. Ancak kan damarları basit düz borular değildir: dallanır, daralır, kıvrılır ve ayrılır; kan hızı da buna bağlı olarak hızlanır ya da yavaşlar. Bu şekil ve hız değişiklikleri parçacıkların nasıl hareket ettiğini, nerede yoğunlaştığını ve damar duvarlarına yapışacak kadar uzun süre temas edip etmediğini etkiler. Gerçek hasta damarları son derece değişkendir, bu da deneyleri karşılaştırmayı veya yeni bir tedavinin nasıl davranacağını öngörmeyi zorlaştırır. Bu nedenle yazarlar, tümörleri besleyen kan damarlarının temel özelliklerini yakalayan, yüksek kontrollü ve tekrarlanabilir bir “model vaskülatür” inşa etmeye karar verdiler.
İdealize Edilmiş Tümör Kan Ağı İnşa Etmek
Bu model damarları tasarlamak için ekip, gerçek arterlerin nasıl dallandığını tanımlayan klasik kurallardan yararlandı. Bu kurallardan biri olan Murray kanunu, enerji açısından verimli bir ağda ana ve yan damarların çaplarını birbirine bağlar. Meme tümörlerinden alınan klinik ölçümler ve bu ölçeklendirme yasalarını kullanarak araştırmacılar, tümörü besleyen damarların kılcallara doğru nasıl küçüldüğünü taklit eden dal veren ağaçları matematiksel olarak ürettiler. Ardından yüksek çözünürlüklü 3B baskı ile iki, üç veya dört dallanma düzeyine sahip içi boş kanal ağlarını şeffaf plastik blokların içine yerleştirdiler. Kanallar simetrik bir dallanma paterni izledi ve üç boyutta uzanarak parçacık hareketini incelemek için basitleştirilmiş ama fizyolojik olarak ilham alınmış bir ortam sundu.
Manyetik Parçacıkları Eylem Halinde İzlemek
Bu basılı ağlardan suyu kan yerine geçecek şekilde pompalayıp yukarıdan SPION içeren sıvı enjekte ettiler ve modelin etrafına statik bir manyetik alan uyguladılar. Yüksek hızlı görüntüleme, karanlık partikül bulutlarının farklı dallardan nasıl geçtiğinin film benzeri kaydını sağlarken, bilgisayar analizi parlaklık değişimlerini yerel parçacık varlığını yansıtan zamana bağlı sinyallere dönüştürdü. Arkaplan akış hızı, parçacık yoğunluğu, dallanma karmaşıklığı ve mıknatısın varlığı ya da yokluğunu değiştirerek araştırmacılar her bir faktörün parçacık dağılımı, kalış süresi ve kanal duvarlarına birikim üzerindeki etkisini ayırabildiler.
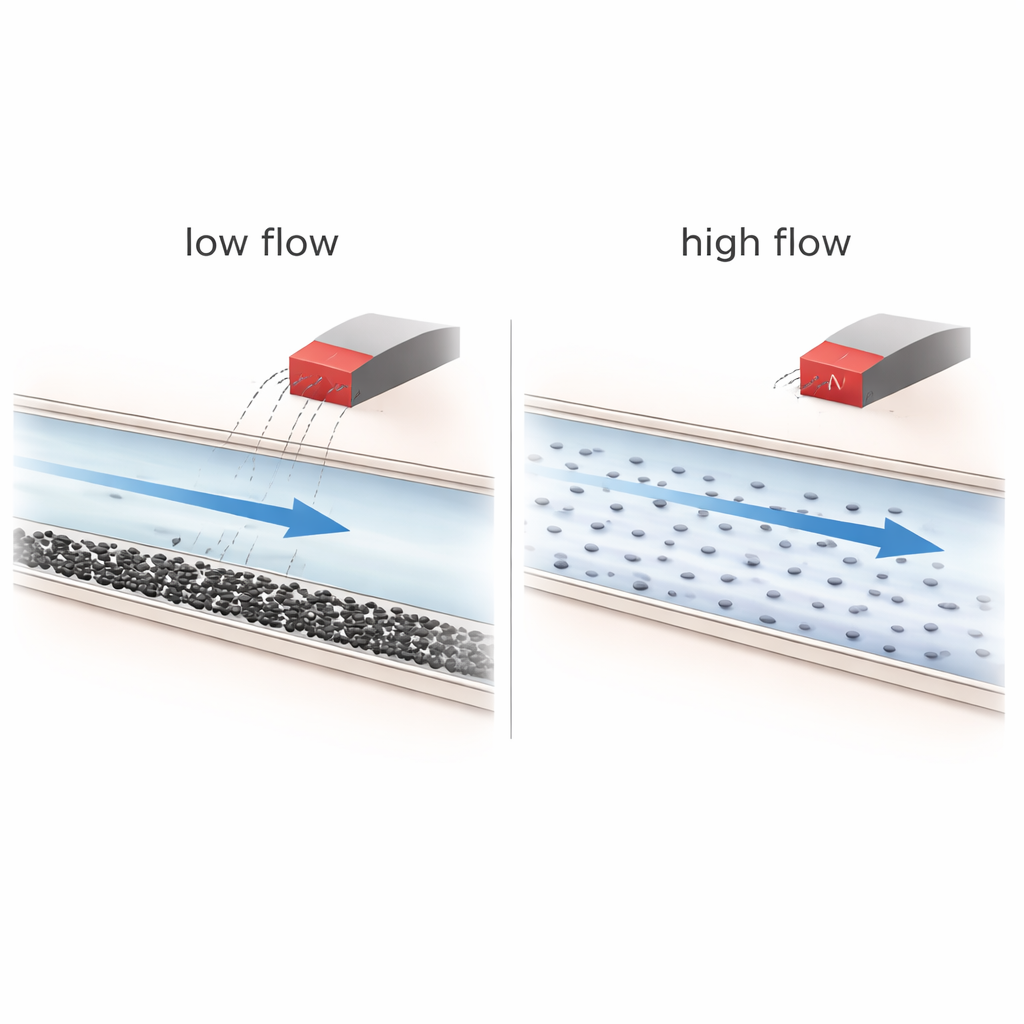
Mıknatısların Yardımcı Olduğu ve Olmadığı Durumlar
Deneyler, hikâyenin hakim unsurunun akış koşulları olduğunu ortaya koyuyor. Daha yüksek akış hızlarında sıvı iyi karışır ve nanoparçacıklar hızla taşınır; bu koşullar altında manyetik alanın neredeyse hiçbir etkisi olmaz ve parçacıklar basitçe ağ içindeki akım hatlarını izler. Ancak düşük akış hızlarında yerçekimi ve yoğunluk etkileri parçacıkların kanalların altına doğru çökmesine neden olur; tabakalaşmış katmanlar ve bazen gevşek kümeler oluşur. Bu zaten düzensiz durumda mıknatıs, daha fazla parçacığı belirli dallara yönlendirebilir ve özellikle daha karmaşık, çok dallı ağlarda kalış sürelerini hafifçe uzatabilir. Yine de hesaplamalar, tek bir 40 nanometre parçacık üzerindeki manyetik kuvvetin, akan sıvının neden olduğu viskoz sürtünmeden birçok mertebe zayıf olduğunu gösteriyor; bu da test edilen koşullar altında gerçek bir “tek parçacık yönlendirmesinin” fiziksel olarak gerçekçi olmadığını ortaya koyuyor.
Gelecek Kanser Tedavileri İçin Anlamı
Bir uzman olmayan için temel çıkarım, yalnızca mıknatısların hızlı hareket eden bir kan akışından serbestçe süspanse olmuş nanoparçacıkları güvenilir şekilde çekemeyeceğidir. Bunun yerine, fark edilir manyetik etkiler yalnızca parçacıklar zaten yavaşladıklarında, çöktüklerinde veya kümelendiğinde ortaya çıkar—bu durumlar manyetik yanııtlarını etkin şekilde büyütür. Burada tanıtılan genelleştirilmiş, 3B baskılı damar modelleri, farklı ağ geometrileri ve akış rejimleri arasında bu tür etkileri keşfetmek için standartlaştırılmış bir yol sağlar. Gelecekte manyetik ilaç hedeflemesi için bu çalışma, başarılı stratejilerin muhtemelen tek tek nanoparçacıkları büyük, hızlı perfüze edilen damarlarda yönlendirmeye güvenmek yerine kontrollü agregasyon veya taşıyıcı sistemler gibi kolektif davranışları kullanmayı gerektireceğini öne sürüyor.
Atıf: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Anahtar kelimeler: manyetik ilaç hedefleme, nanoparçacıklar, tümör vaskülatürü, mikroakışkan modeller, ilaç taşıma