Clear Sky Science · tr
Antimikrobiyal direnç geri dönüşü ile ilişkili küresel düzenleyiciler ve effluks genlerinin entegre analizi: çoklu ilaç dirençli Klebsiella pneumoniae
Neden bu hastane bakterilerini öldürmek bu kadar zor?
Dünyadaki hastanelerde, Klebsiella pneumoniae bakterisinin belirli suşları tedavi edilmesiyle ünlü şekilde zor hâle geldi. Eskiden güvenilir şekilde işe yarayan çoklu antibiyotiklere direnç göstererek rutin enfeksiyonları yaşamı tehdit eden acillere dönüştürüyorlar. Bu çalışma, bu bakterilerin kullandığı önemli bir numarayı anlamak için mikrobiyal düzeyde inceliyor: antibiyotikleri hücre dışına atan mikroskobik pompalar ve bu pompaları yukarı veya aşağı çeviren gibi görünen genetik anahtarlar.
Süperbakteriler ve moleküler kaçış kapakları
Çoklu ilaç dirençli Klebsiella pneumoniae, bu araştırmanın yapıldığı Irak’taki tıp merkezi dahil birçok hastanede artık karşılaşılan bir sorun. Bu bakteriler, florokinolonlar, aminoglikozidler ve üçüncü kuşak sefalosporinler gibi birden çok büyük antibiyotik ailesine aynı anda dayanabiliyor. Bunu yapmanın bir yolu, hücre zarlarına güçlü “effluks pompaları” kurmalarıdır. En önemlilerinden biri AcrAB‑TolC adlı bir sistemdir; bakteriyel zarları kapsayarak hücre içindeki antibiyotik moleküllerini yakalayıp ilacın ciddi hasar vermesini önlemek için dışarı iten küçük bir pompa gibi çalışır. Bu pompalar çok aktif olduğunda, bakteri içindeki antibiyotik konsantrasyonu öldürücü seviyelere asla ulaşmaz.
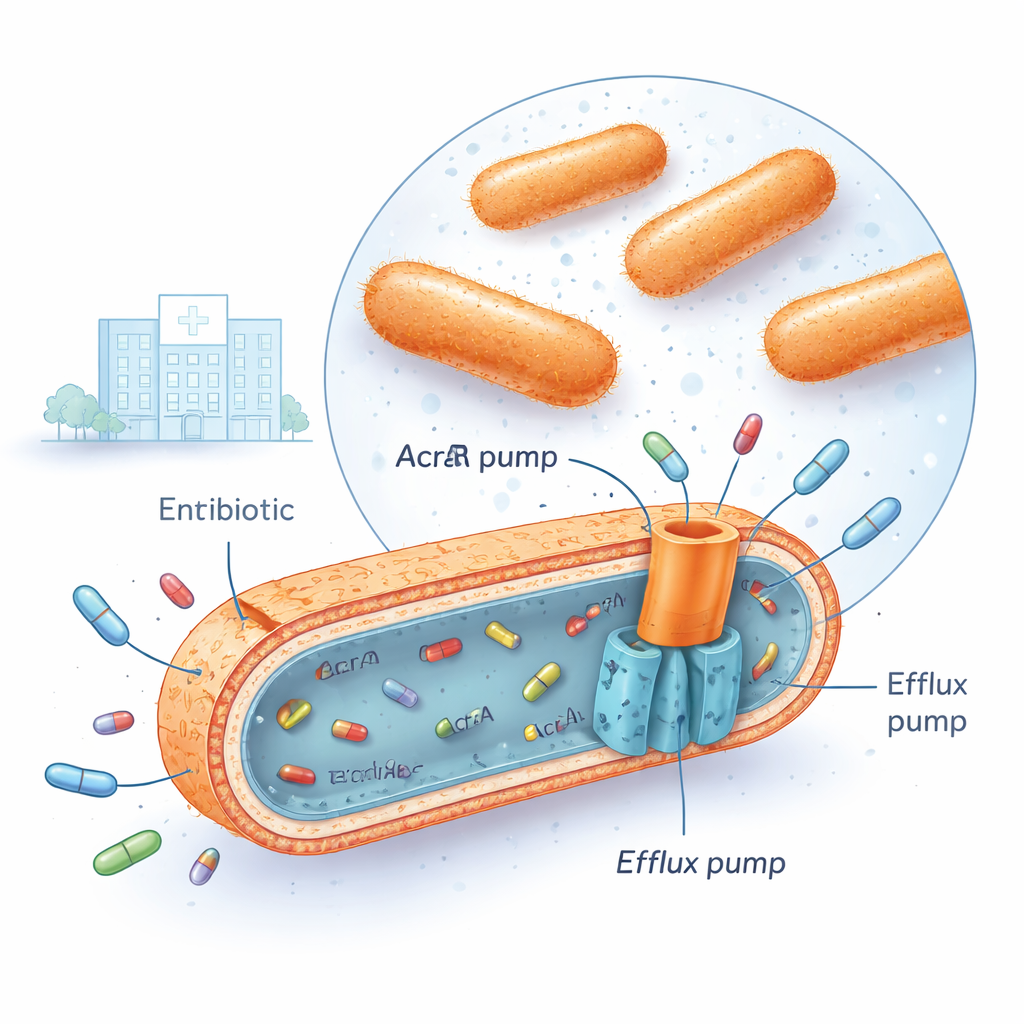
Pompaların hızlanmasına eşlik eden gen anahtarları
Araştırmacılar 30 çoklu ilaç dirençli klinik Klebsiella pneumoniae izolatını topladı ve bunları 10 antibiyotiğe duyarlı izolat ile standart bir referans suşla karşılaştırdı. Kantitatif gerçek‑zamanlı PCR adı verilen bir teknik kullanarak belirli genlerin ne kadar aktif olduğunu ölçtüler. Üç “küresel düzenleyici”ye — marA, soxS ve rob adlı genlere — ve ayrıca AcrAB‑TolC pompasının üç parçasına (acrA, acrB ve tolC) odaklandılar. Dirençli suşlarda iki düzenleyici, marA ve soxS, duyarlı bakterilerle karşılaştırıldığında genellikle yaklaşık dört‑beş kat daha yüksek aktifleştirilmişken, pompanın merkezi bir bileşeni olan acrB neredeyse sekiz kat artmıştı. İstatistiksel analizler, marA ve soxS seviyeleri yüksek olduğunda acrB seviyelerinin de genellikle yüksek olduğunu gösterdi ve bu suşlar ciprofloxacin gibi florokinolon antibiyotiklerine çok daha yüksek dozlarda dayanma eğilimindeydi. Üçüncü bir düzenleyici olan rob ise az değişti ve pompa aktivitesiyle örtüşmedi; bu da test koşullarında daha küçük bir rol oynadığını düşündürüyor.
Direnci zayıflatmak için pompaları kapatmak
Pompaların ve düzenleyici genlerin birlikte aktif olduğunu bulmak düşündürücü olsa da bunun gerçekten direnci sağladığını kanıtlamak için yeterli değil. Pompaların işlevsel olarak önemli olup olmadığını test etmek için ekip PAβN adlı kimyasal bir araca başvurdu. Bu bileşik hastalarda ilaç olarak kullanılmıyor, ancak laboratuvarda AcrAB‑TolC benzeri pompaları tıkayıp antibiyotikleri dışarı atmalarını durdurabiliyor. Bilim insanları, özellikle yüksek acrB gen seviyelerine sahip on dirençli izolatı seçti ve PAβN ile ve PAβN olmadan büyümelerini durdurmak için ne kadar ciprofloxacin gerektiğini ölçtü. Bu on suştan sekizinde, pompayı bloke etmek gerekli ciprofloxacin dozunu en az dört kat, bazen on altı kata kadar düşürdü. Bu düşüş, bu süperbakterilerin çoğunda aktif effluks pompalarının yüksek antibiyotik dozlarına dayanabilmelerinin gerçekten önemli bir nedeni olduğunu gösteriyor.
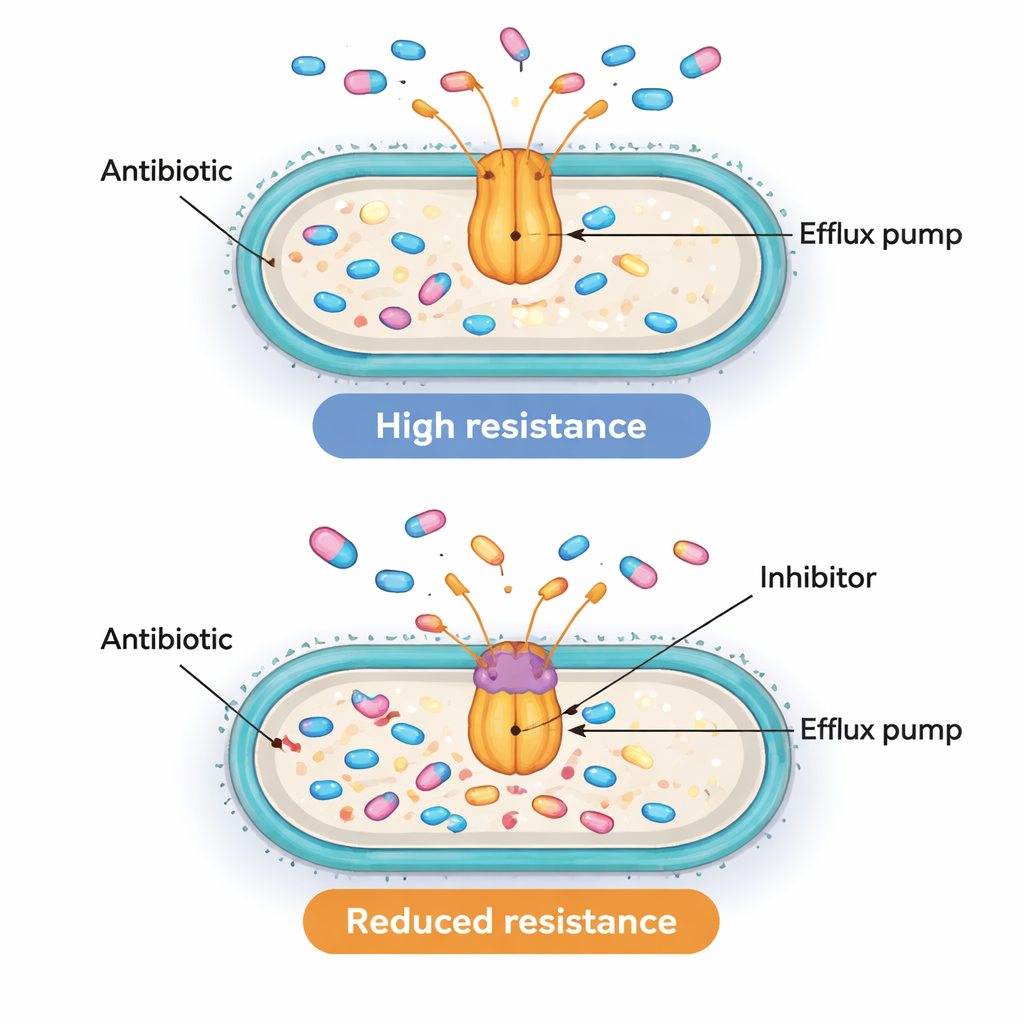
Umut veren hedefleri olan karmaşık bir direnç bulmacası
Her suş aynı şekilde davranmadı. Güçlü şekilde ifade edilmiş pompa genlerine sahip bazı bakterilerde pompalar bloke edildiğinde duyarlılık yalnızca kısmen geri geldi; bu da antibiyotiğin hücre içindeki hedefindeki değişiklikler, ilacı parçalayan enzim üretimi veya alternatif pompalar gibi diğer direnç yollarının da katkıda bulunduğunu gösteriyor. Örneğin aminoglikozid bir antibiyotik olan gentamisin, marA/soxS ve AcrAB‑TolC genlerinde görülen desenlerden büyük ölçüde etkilenmedi; bu da çoklu ilaç direncinin genellikle tek bir mekanizmadan ziyade birkaç örtüşen savunma katmanından oluştuğunu vurguluyor.
Gelecekteki tedaviler için anlamı
Uzman olmayanlar için ana mesaj şudur: Bazı hastane bakterileri, ilaçları engellemenin veya parçalamanın ötesinde, onlara aktif şekilde dışarı atarak hayatta kalabiliyor. Bu çalışma iki gen “anahtarı” MarA ve SoxS’in daha yüksek aktivitesini, daha aktif effluks pompaları ve yaygın kullanılan bir antibiyotik sınıfına karşı daha güçlü dirençle ilişkilendiriyor. Pompalar deneysel olarak tıkandığında, bu bakterilerin çoğu en azından kısmen yeniden duyarlı hale geliyor. Çalışma henüz bu anahtarların pompaları tam olarak nasıl kontrol ettiğini kanıtlamasa da, hem düzenleyicileri hem de pompaları çekici hedefler olarak öne çıkarıyor. Uzun vadede, geleneksel antibiyotikleri güvenli pompa engelleyicilerle — veya bu küresel düzenleyicilerin aktivitesini azaltan ilaçlarla — eşleştirmek, mevcut tedavilerin çoklu ilaç direncine sahip enfeksiyonlara karşı yeniden etkili olmasına yardımcı olabilir.
Atıf: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Anahtar kelimeler: antibiyotik direnci, effluks pompaları, Klebsiella pneumoniae, florokinolonlar, direnç geri dönüşü