Clear Sky Science · tr
Lipit-PEG ankrajlı floresan protein göstergeleri kullanarak hücreler arası biyomoleküllerin görüntülenmesi
Hücrelerin Gerçek Zamanlı Konuşmasını İzlemek
Beynimiz ve vücudumuz, hücreler arasında sürekli bir kimyasal iletişime dayanır. İyonlar ve nörotransmitterler küçük boşluklar boyunca mesaj taşır, ancak bu hızlı ve kısa ömürlü sinyaller bozulmadan görmek zordur. Bu çalışma, hücrelerin dış yüzeyine tutunan parlayan sensörlerle canlı hücreleri "boyamanın" basit bir yolunu sunuyor; bu sayede bilim insanları özellikle potasyum iyonları ve nörotransmitter glutamat olmak üzere bu mesajları canlı olarak ve ayrıntılı biçimde izleyebiliyor. 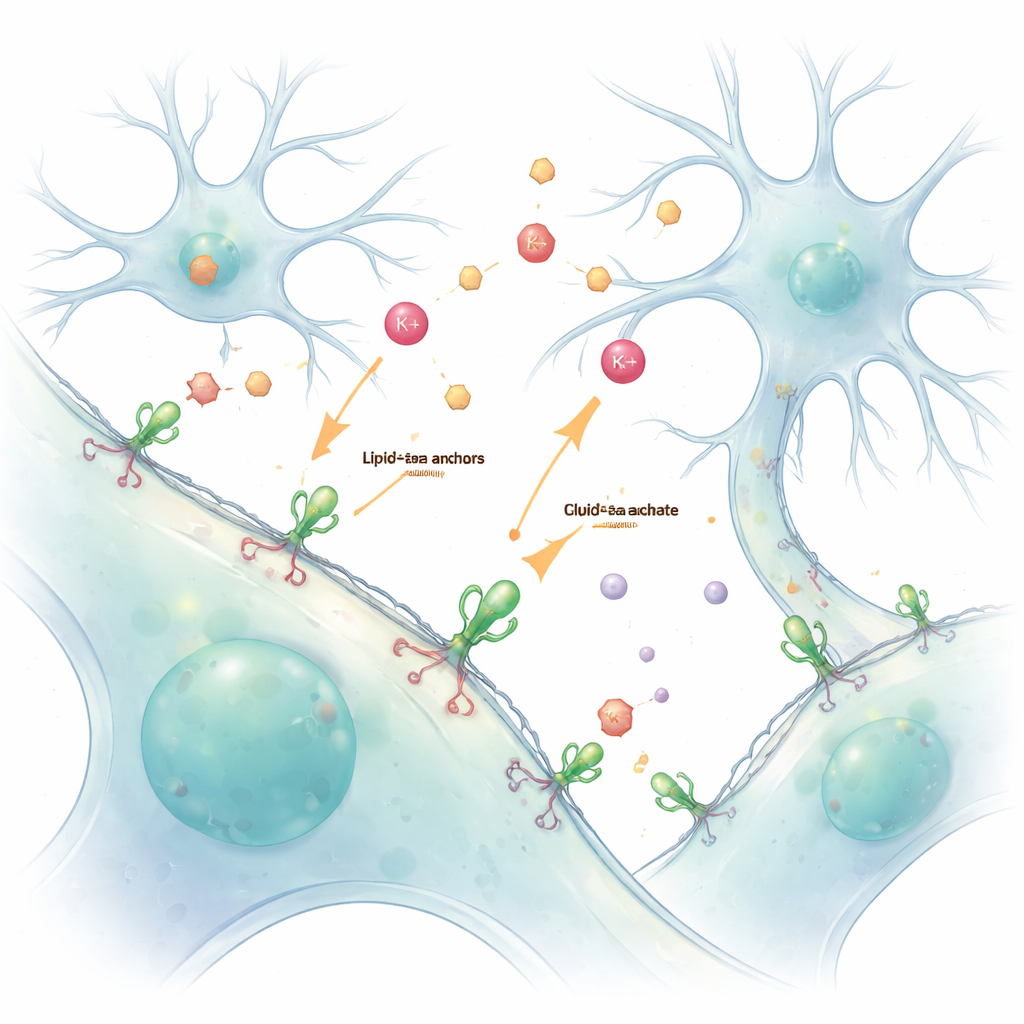
Hücre Yüzeyini Etiketlemenin Yeni Bir Yolu
Geleneksel olarak araştırmacılar, hücreleri kendi DNA’larından floresan protein sensörleri üretecek şekilde tasarlar. Bu genetik yaklaşım güçlü olmakla birlikte, sensörleri sıklıkla hücre içine yerleştirir ve içeride olanları dışarıdakilerden ayırmayı zorlaştırır. Yazarlar bunu lipit–PEG adında kimyasal bir tutamak kullanarak çözdüler. Bu molekülün bir ucu dış zar içine gömülürken, diğer ucu floresan protein sensöre kimyasal olarak bağlanıyor. Hazırlanan bu sensörler canlı hücrelere eklendiğinde dış yüzeyi kendiliğinden kaplayıp çevre sıvıda olanları rapor eden kararlı, parlak bir katman oluşturuyor.
Potasyumu ve Glutamati Işığa Çevirmek
Ekip iki mevcut floresan göstergenin yöntemini uyarladı: potasyuma tepki veren GINKO2 ve glutamata tepki veren R-iGluSnFR1. Bu proteinleri bakterilerden saflaştırdılar ve ardından lipit–PEG ankrajlarını eklediler. Kültürdeki insan hücrelerinde ankrajlı potasyum sensörü hücre yüzeyi boyunca düzgün bir kontur oluşturdu ve ekstrasellüler potasyum arttığında parlaklaştı, seviyeler düştüğünde tekrar söndü. Önemli olarak, tüp içi deneylerde ışık verme özellikleri ve duyarlılığı orijinal, değiştirilmemiş sensörle yakından eşleşti; bu da ankrajlamanın performansı azaltmadığını gösterdi. Aynı durum glutamat sensörü için de geçerliydi: ankrajlandıktan sonra da yanıt vermeye devam etti ve hücrelerin hemen dışındaki alandaki glutamatı net biçimde vurguladı.
Kültürlerde ve Dilimlerde Nöronları Dinlemek
Araştırmacılar ardından öğrenme ve hafıza için önemli bir beyin bölgesi olan fare hipokampusundan alınan sinir hücrelerine geçtiler. Bu nöronları lipit–PEG–ankrajlı glutamat sensörü ile kapladılar ve aynı hücrelerin içini elektriksel aktiviteyi rapor eden ayrı bir kalsiyum boyasıyla doldurdular. Total internal reflection mikroskopisi kullanarak, hücre yüzeyindeki glutamatın kırmızı flaşlarını izlerken hücre içindeki yeşil sinyaller ateşlemeyi bildirdi. Bu çift renkli görüntü, ankrajlı sensörlerin nöronların genetik olarak değiştirilmesine gerek kalmadan spontan nörotransmitter salınımını izleyebildiğini gösterdi.
Beyin Dokusu Üzerinde Kimyasal Dalgaların Haritalanması
Sonra ekip yöntemi hipokampusun doğal bağlantılarını koruyan akut beyin dilimlerinde test etti. Ankrajlı potasyum sensörünü dilimlere uygulayıp sinir liflerini elektriksel olarak uyararak test ettiler. Ankrajlı sensör her uyarı sonrası net, tekrarlanabilir floresans artışları üretti; oysa ankrajlanmamış sensörler hızla yayıldı ve zayıf, kararsız sinyaller verdi. Dilimleri bilinen potasyum seviyelerine sahip çözeltilere batırıp dokunun kendi hafif parlamasını düzelttikten sonra yazarlar bir kalibrasyon eğrisi oluşturup gerçek ekstrasellüler potasyum konsantrasyonlarını tahmin ettiler. Bazal seviyeler yaklaşık 2.5 millimolar civarındaydı ve hafif uyarımla yaklaşık 3.4 millimole yükseldi; bu klasik elektrot ölçümleriyle uyumlu. Hem potasyum hem de glutamat için ankrajlı sensörler bu sinyallerin farklı yayılımını ortaya koydu: glutamat değişimleri etkin sinapslara yakın kalırken, potasyum artışları yüzlerce mikrometreye yayıldı ve ağ uyarılabilirliği üzerinde daha geniş etkiler olabileceğine işaret etti. 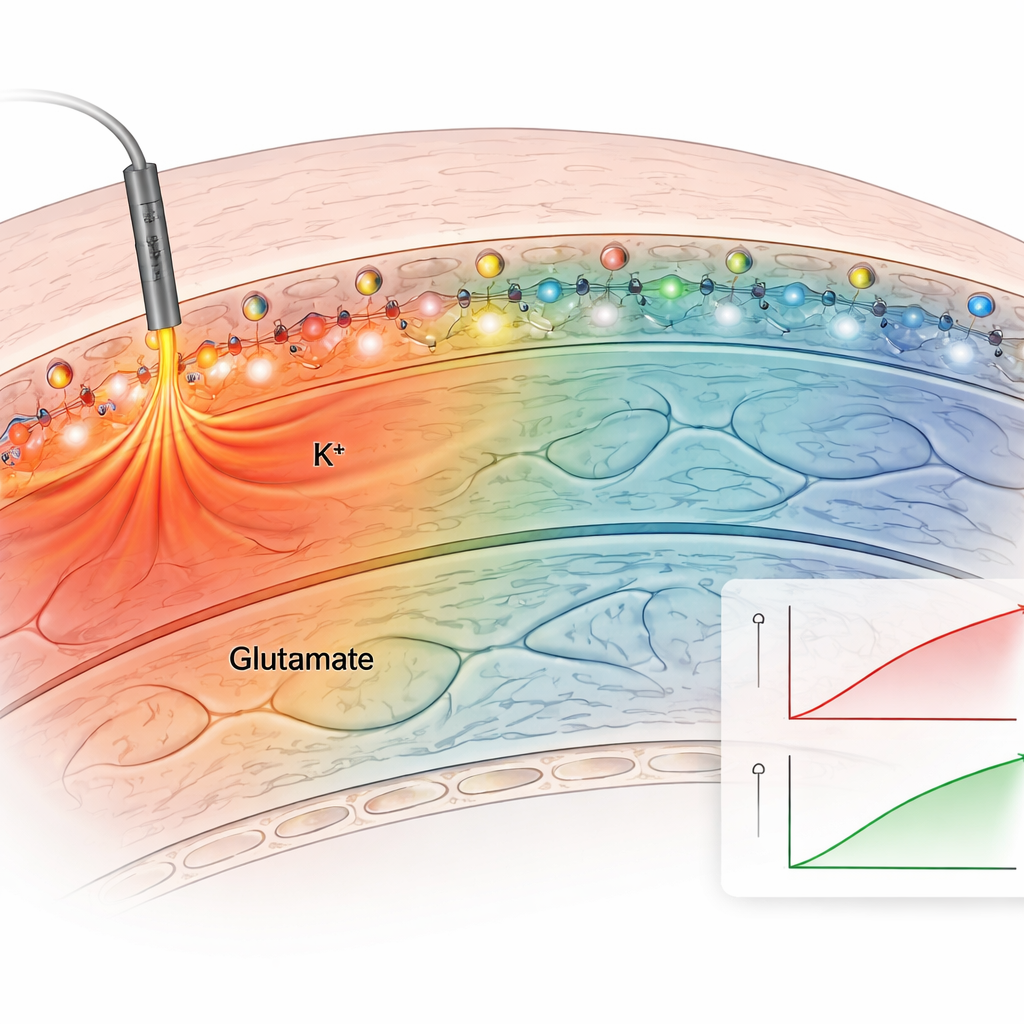
Beynin Sinyalleri Nasıl Temizlediğini ve Oluşturduğunu Sınamak
Sensörler hücre yüzeyine sabitlendiği için yazarlar bu ekstrasellüler dalgaları şekillendiren süreçleri ayrıştırabildiler. Normalde glutamati temizleyen glutamat taşıyıcılarını bloke etmek, ankrajlı glutamat sensöründe daha büyük ve daha uzun süreli sinyaller ortaya çıkardı; bu, yerel alımla glutamat yayılımının sınırlandığını doğruladı. AMPA tipi glutamat reseptörlerini engellemek hem elektriksel yanıtları hem de potasyum sinyallerini azalttı; bu, potasyum artışının çoğunun sinaptik girişle aktive edilen postsinaptik nöronlardan geldiğini gösteriyor. Tetrodotoksin ile sodyum kanallarını bloke etmek potasyum değişikliklerini neredeyse ortadan kaldırdı ve bunları aksiyon potansiyelleriyle doğrudan bağladı. Birlikte, bu deneyler ankrajlı sensörlerin karmaşık, dağıtık kimyayı sezgisel filmler ve haritalar haline getirebileceğini gösteriyor.
Gelecek Beyin Araştırmaları İçin Neden Önemli
Uzman olmayanlar için ana mesaj şu: bu çalışma, canlı hücreleri ve dokuları yüksek duyarlılıklı moleküler raporlayıcılarla kaplamak için hızlı, genetik olmayan bir yol sunuyor. Her hücre tipini yeniden programlamak yerine bilim insanları dışarıdan hazırlanmış sensör proteinleri ekleyip iyonların ve nörotransmitterlerin hücre yüzeyinde gerçek zamanlı nasıl değiştiğini anında görselleştirebiliyor. Bu yaklaşım kontrolü, tekrarlanabilirliği ve mekânsal hassasiyeti artırırken özellikle akut beyin dilimleri gibi hassas hazırlıklarda gen tesliminin zorluklarından kaçınıyor. Farklı kimyasallar için daha fazla floresan gösterge geliştirildikçe aynı lipit–PEG ankrajlama stratejisi, vücut çapında hücrelerin kimyasal dilini izlemek için yaygın kullanılan bir araç seti haline gelebilir.
Atıf: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Anahtar kelimeler: hücre dışı sinyal iletimi, floresan biyosensörler, glutamat görüntüleme, potasyum dinamikleri, hipokampal nöronlar