Clear Sky Science · tr
Hassas lenf nodu metastazı tespiti için kapsamlı budama ve GNN sınıflandırması ile dinamik grafik konvolüsyonu
Lenf nodlarındaki küçük değişimler neden önemli
Meme kanseri yayıldığında, ilk duraklarından biri genellikle vücudun drenaj sistemine dizilmiş küçük filtreler olan lenf nodlarıdır. Kanser hücrelerinin bu nodlara ulaşıp ulaşmadığını saptamak, cerrahi, kemoterapi ve radyoterapi gibi kararları belirlemede doktorların başvurduğu en önemli ipuçlarından biridir. Yine de, özellikle sağlıklı dokuya çok benzeyen çok küçük kanser hücresi kümeleri dijital mikroskop görüntülerinde uzman patologlar tarafından kaçırılabilir. Bu çalışma, dokuyu birbirine bağlı bölgeler ağı olarak ele alan yeni bir yapay zeka çerçevesi sunuyor; bu sayede yayılmanın ince işaretlerini olağanüstü bir doğrulukla bulabiliyor.
Doku görüntülerini ağlara dönüştürmek
Araştırmacılar, meme kanseri lenf nodu biyopsilerinden elde edilen, lekelendirilmiş dokunun devasa dijital slaytları olan bütün slayt görüntüleriyle çalışıyorlar. Bu görüntüler milyonlarca piksel ve şaşırtıcı bir hücre türü, renk ve doku karışımı içeriyor. Bu karmaşıklığı dizginlemek için ekip önce görüntüleri temizliyor: parlaklık ve renkleri normalize ediyor, gürültüyü azaltıyor ve bilgisayarın doğal varyasyonlarla başa çıkmasını sağlamak için yamaları döndürme ve çevirme gibi artırma işlemleriyle çoğaltılmış örnekler üretiyor. Her görüntü yaması daha sonra küçük, oldukça tekdüze bölgelere ("süperpiksel"ler) ayrılıyor; bunlar grafın düğümleri—nokta—olarak görev yaparken, bitişik bölgeler arasındaki ilişkiler de bağlayıcı çizgiler—kenarlar—oluşturuyor. Bu ağ görünümü, gerçek dokunun düzensiz şekillerini ve düzenlerini geleneksel ızgara tabanlı görüntü yöntemlerinden daha iyi koruyor.
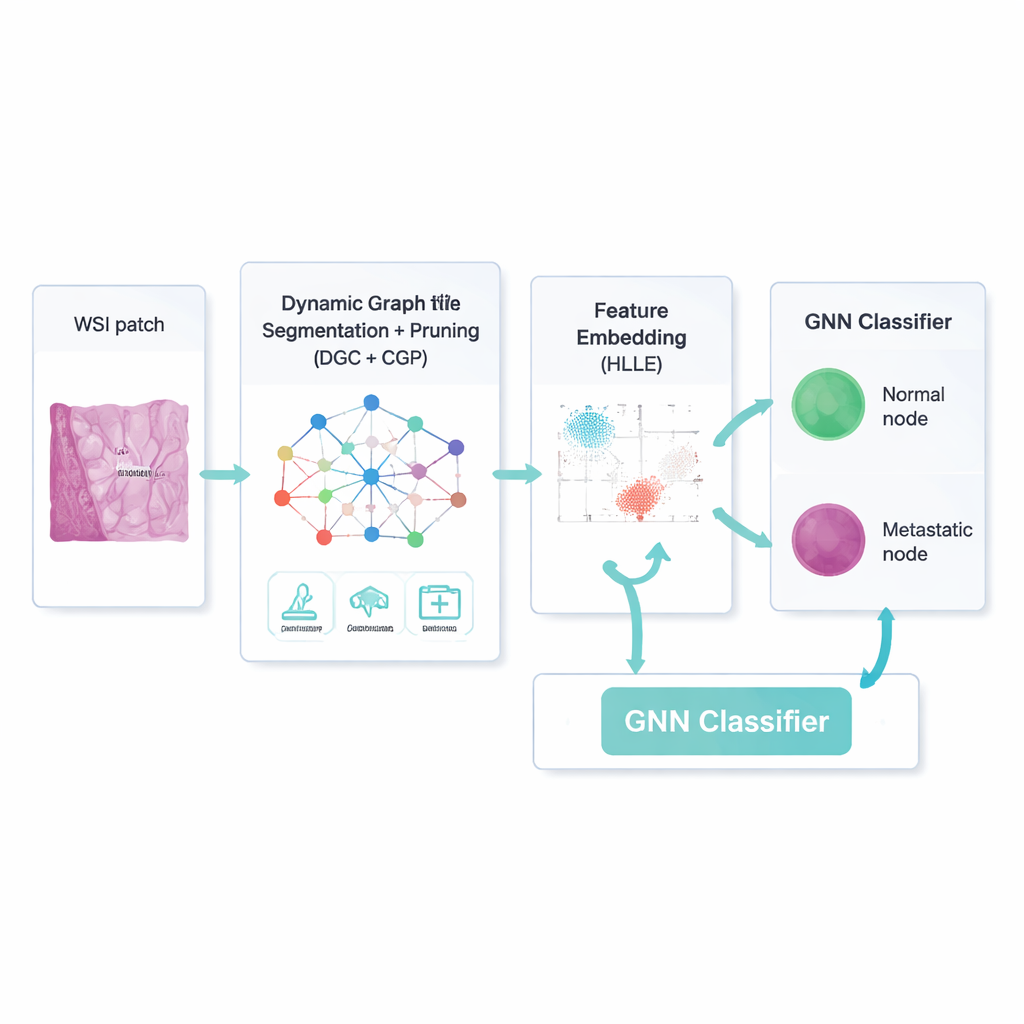
Önemli olana odaklanmanın daha akıllı yolu
Sadece bir ağ kurmak yeterli değil; birçok bağlantı ve görüntü özelliği alakasız veya yanıltıcı olabilir. Bu nedenle çerçeve, her bir bölgenin nasıl göründüğünü ve bölgelerin birbirlerini nasıl etkilediğini öğrenen dinamik bir grafik konvolüsyonel otoenkoder kullanıyor. Eklenen bir "dikkat" mekanizması modelin bazı görüntü kanallarına diğerlerinden daha fazla ağırlık vermesini sağlıyor; örneğin tümör sınırındaki kenarları vurgulamak gibi. Aynı zamanda Kapsamlı Grafik Kademeli Budama (Comprehensive Graph Gradual Pruning) adlı bir strateji, zayıf bölge bağlantıları, daha az faydalı sayısal özellikler ve düşük etkili model ağırlıkları gibi işe yaramayan parçaları istikrarlı şekilde buduyor. Bu budama eğitim sırasında gerçekleşiyor, sonradan değil; böylece sistem daha azla daha fazlasını yapmayı öğreniyor ve sonuçta hem daha hızlı hem de yorumlaması daha kolay bir model ortaya çıkıyor.
Desenleri şekillerini kaybetmeden sıkıştırmak
Model muhtemel lenf nodu bölgelerini arkaplandan ayırdıktan sonra, her bölgeyi kompakt ama anlamlı bir şekilde tanımlaması gerekiyor. Bunu yapmak için yazarlar Hessian tabanlı Yerel Doğrusal Gömme (Hessian-based Locally Linear Embedding) adlı bir teknik kullanıyor. Basitçe söylemek gerekirse, bu yöntem çok sayıda sayısal özelliği daha küçük bir kümeye sıkıştırırken gerçek örneklerin özellik uzayında nasıl düzenlendiğinin kıvrımlı "şeklini" korumaya çalışıyor—örneğin, çok küçük metastazların normal bağışıklık hücrelerinden doku dokusu veya renk kalıpları boyunca nasıl farklılaştığı gibi. Bu sıkıştırılmış tanımlamalar, düğümlerin metastatik olup olmadığını belirleyen, bölgeler ağı ve temizlenmiş bağlantıları üzerinde çalışan bir grafik sinir ağı sınıflayıcısına girdi oluyor.
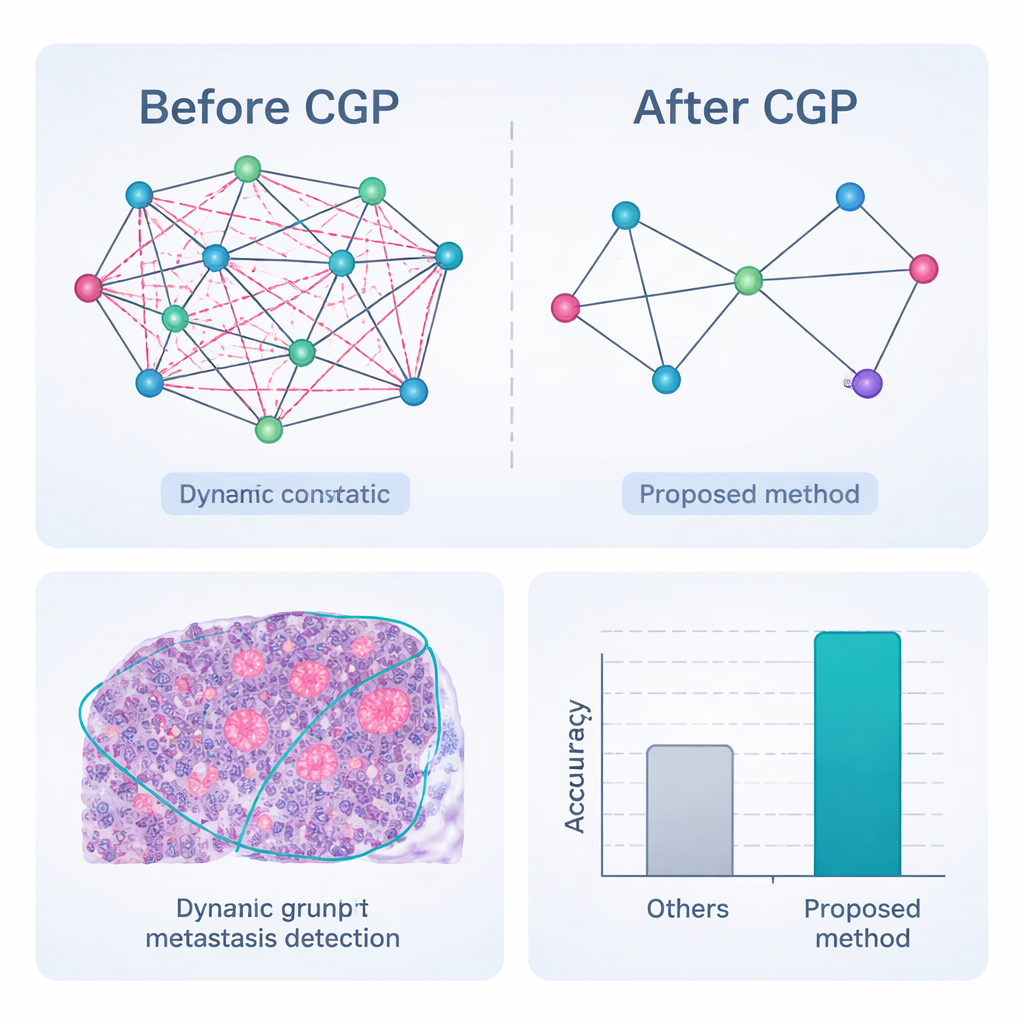
Çerçeveyi teste sokmak
Tam boruhattı—ön işlem, budamalı dinamik grafik segmentasyonu, özellik gömme ve graf tabanlı sınıflandırma—CAMELYON17 üzerinde değerlendirildi; bu veri seti meme kanseri hastalarından alınmış 1.000 uzman tarafından anotasyon yapılmış lenf nodu slaytının halka açık bir koleksiyonudur. Popüler konvolüsyonel ağlar ve hibrit dönüştürücü modeller de dahil olmak üzere güçlü derin öğrenme rakipleriyle karşılaştırıldığında, yeni yöntem neredeyse tüm ölçütlerde en yüksek puanları elde etti. Nodları kanserli veya değil olarak vakaların %98,65'inde doğru sınıflandırdı ve çok küçük ya da zayıf metastazlar için özellikle tümör bölgesi konturlarına uzman çizimleriyle daha iyi uyum gösterdi. Kritik olarak, graf agresif şekilde budandığından sistem bu sonuçlara çok daha az hesaplama ve düşük bellek kullanımıyla ulaşıyor; bu da onu yoğun patoloji laboratuvarlarında gerçek zamanlı kullanım için daha uygun hale getiriyor.
Bu hastalar ve klinisyenler için ne anlama geliyor
Günlük anlatımıyla, bu çalışma dokuyu akıllıca budanmış bir bölgeler ağı olarak düşünmenin bilgisayarların lenf nodu slaytlarında son derece dikkatli ikinci okuyucular gibi davranmasına nasıl yardımcı olabileceğini gösteriyor. Dikkati ve hesaplama gücünü en bilgilendirici yapılara odaklarken gürültüyü elerken, çerçeve aksi halde kaçırılabilecek küçük kanser tohumlarını tespit etmede daha başarılı ve bunu pratik olacak kadar verimli bir şekilde yapıyor. Daha ileri klinik doğrulama gerekse de, bu tür araçlar patologlara kanserin yayılıp yayılmadığına ilişkin kararları daha hızlı ve tutarlı şekilde vermede destek sağlayabilir—bu bilgi doğrudan tedavi planlarını ve nihayetinde hasta sonuçlarını şekillendirir.
Atıf: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Anahtar kelimeler: lenf nodu metastazı, dijital patoloji, graf sinir ağları, tıbbi görüntü segmentasyonu, meme kanseri