Clear Sky Science · tr
İnsan tiyrozilprotein sülfotransferaz 2, TPST2’de metal bağlanmasının yapısal karakterizasyonu
Hücre sinyalleşmesi için küçük metal iyonları neden önemli
Hücrelerimizin içinde sayısız moleküler makine, dokuların nasıl büyüdüğünü, hormonların nasıl işlediğini ve bağışıklık hücrelerinin nasıl iletişim kurduğunu sessizce ayarlar. Bu makinelerden biri olan TPST2 adlı enzim, Golgi aygıtı olarak bilinen hücrenin gönderi merkezinden geçerken bazı proteinlere küçük bir sülfat etiketi ekler. Bu çalışma, sodyum ve mangan gibi basit metal iyonlarının TPST2’nin yapısının bazı bölümlerini hafifçe sertleştirerek daha verimli çalışmasına nasıl yardımcı olduğunu ortaya koyuyor—bu bulgu hücrelerdeki mineral dengesini kanser ve hormonla ilişkili hastalıklarla ilişkilendirebilecek bir bağlantıyı işaret ediyor. 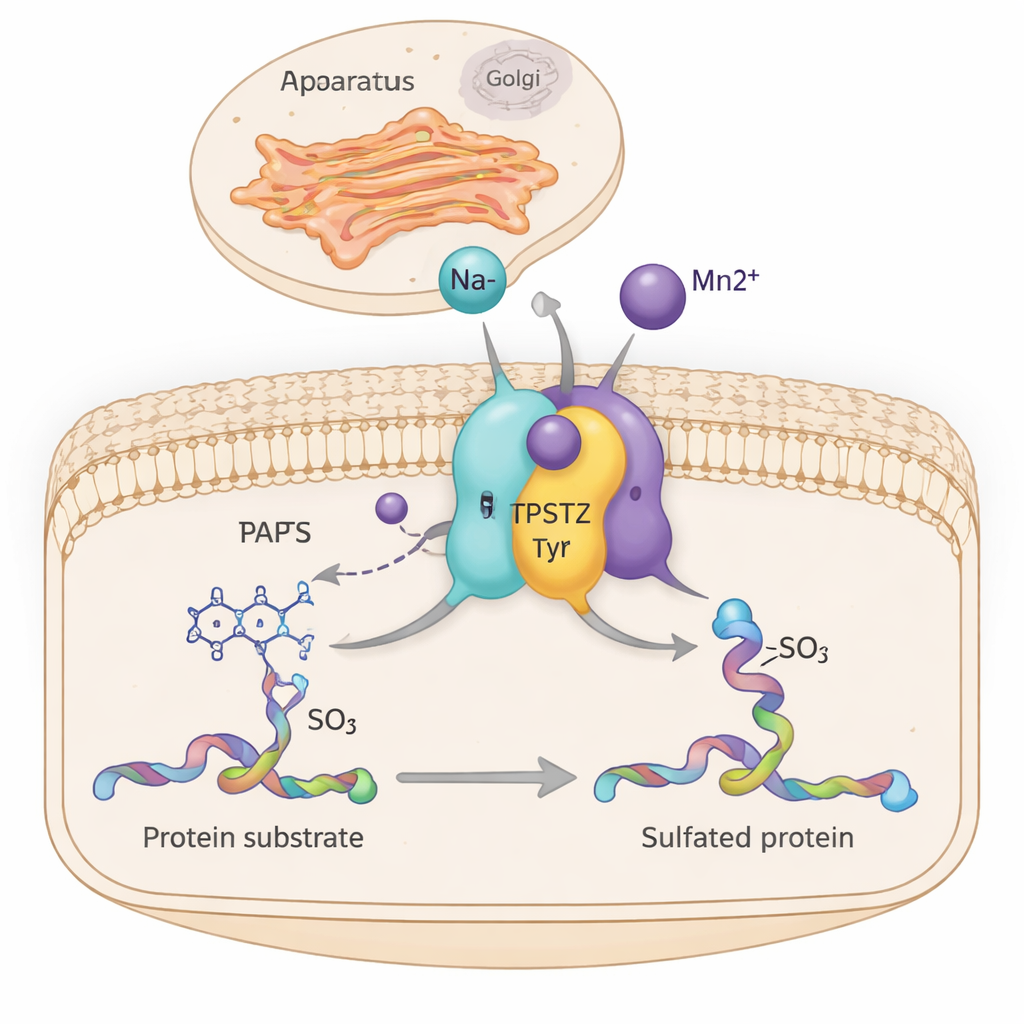
Diğer proteinleri süsleyen bir enzim
TPST2, proteinlerin belirli tiyrozin yapı taşlarına eklenen “tirosin sülfasyonu” adı verilen kimyasal modifikasyonu gerçekleştiren enzim ailesine aittir. Bu sülfatlanmış proteinler hücre dışındaki süreçlerde önemli roller oynar; kan pıhtılaşmasını, beyaz kan hücresi hareketini, hormon–reseptör bağlanmasını ve virüslerin hücrelere giriş şeklini etkiler. İnsanlarda iki ana sülfatlayıcı enzim vardır: TPST1 ve TPST2; bunlar Golgi zarında yerleşir ve proteinler ihraç için hazırlanırken onları değiştirir. Fare çalışmalarında TPST2 kaybının tiroid hormonu üretimini bozduğu, büyümeyi engellediği ve erkeklerde kısırlığa yol açtığı gösterilmiş; bu da TPST2’nin normal fizyoloji için önemini vurgular.
Kanser ve bağışıklıktan kaçışla bağlantılar
Son araştırmalar TPST2’yi doğrudan hastalıklarla ilişkilendirdi. Melanomda TPST2, interferon reseptörünün bir bileşenini immün sinyallemeyi zayıflatan bir şekilde değiştiriyor ve TPST2’nin engellenmesi PD-1 hedefli immün kontrol terapilerinin etkisini artırıyor. Pankreas kanserinde TPST2’ye bağımlı bir yol, tümör büyümesini ve yayılmasını destekleyen bir proteinin (integrin β4) stabil kalmasına yardımcı oluyor. Bu modellerde TPST2’nin inhibisyonu kanser hücrelerinin bölünmesini ve istila etmesini yavaşlatıyor. TPST2 hüre yüzeyindeki proteinlere etki ettiğinden, hücrelerin çevrelerini algılama ve yanıt verme biçimlerini etkili biçimde yeniden düzenliyor; bu da onu yeni terapiler için çekici bir hedef yapıyor.
Metal “açma düğmelerini” bulmak
Biyokimyacılar uzun zamandır divalent metallere, örneğin mangan (Mn²⁺), TPST2’nin aktivitesini büyük ölçüde artırdığı bilgisindeydi, ancak yapısal neden eksikti. Bu çalışmada yazarlar insan TPST2’nin katalitik çekirdeğini ürettiler ve reaksiyon yan ürünü ile birlikte sodyum (Na⁺) veya mangan içerecek şekilde kristalleştirdiler. Yüksek çözünürlüklü X-ışını kristallografisi kullanarak, enzimin içinde iki küçük metal bağlama cepleri keşfettiler; her biri etrafındaki atomların düzeninde düzgün, altı yüzlü (oktahedral) bir dizilime sahipti. X-ışını dalga boyunu farklı metallerin benzersiz imzalarına göre ayarlayarak Mn²⁺’in bu bölgeleri seçici olarak işgal ettiğini doğruladılar; çinko ve bakır gibi metaller ya başka konumlarda zayıfça bağlanıyor ya da hiç bağlanmıyordu.
Tüm proteini yeniden şekillendirmek yerine kilit hareketli parçaları sertleştirmek
Şaşırtıcı şekilde, sodyumlu TPST2 ile manganlı TPST2 genel olarak neredeyse aynı görünüyordu; protein içinde dramatik bir açılma veya kapanma yoktu. Bunun yerine metalller esas olarak aktif bölgenin girişine yakın iki esnek bölgeyi etkiledi: α3 adı verilen bir heliks ve α12–α13 döngüsü olarak bilinen yakındaki bir halka. Metal içermeyen veya gevşek bağlanmış hallerde bu parçalar sallanıyor ve kısmen düzensiz oluyordu. Na⁺ bağlandığında bunlar daha düzenli hale geliyor; Mn²⁺ ise X-ışını verilerinde azalmış termal hareket ve bilgisayar tabanlı esneklik analizleriyle gösterildiği üzere onları daha da sıkılaştırıyor. Bu ekstra katılık enzimin erime sıcaklığını ılımlı şekilde yükseltiyor ve aktif bölgeyi düzenlemenin “entropik” maliyetini düşürdüğü, böylece TPST2’nin substratları sülfasyon için doğru konuma yönlendirmesini daha kolay ve hızlı hale getirdiği düşünülüyor. 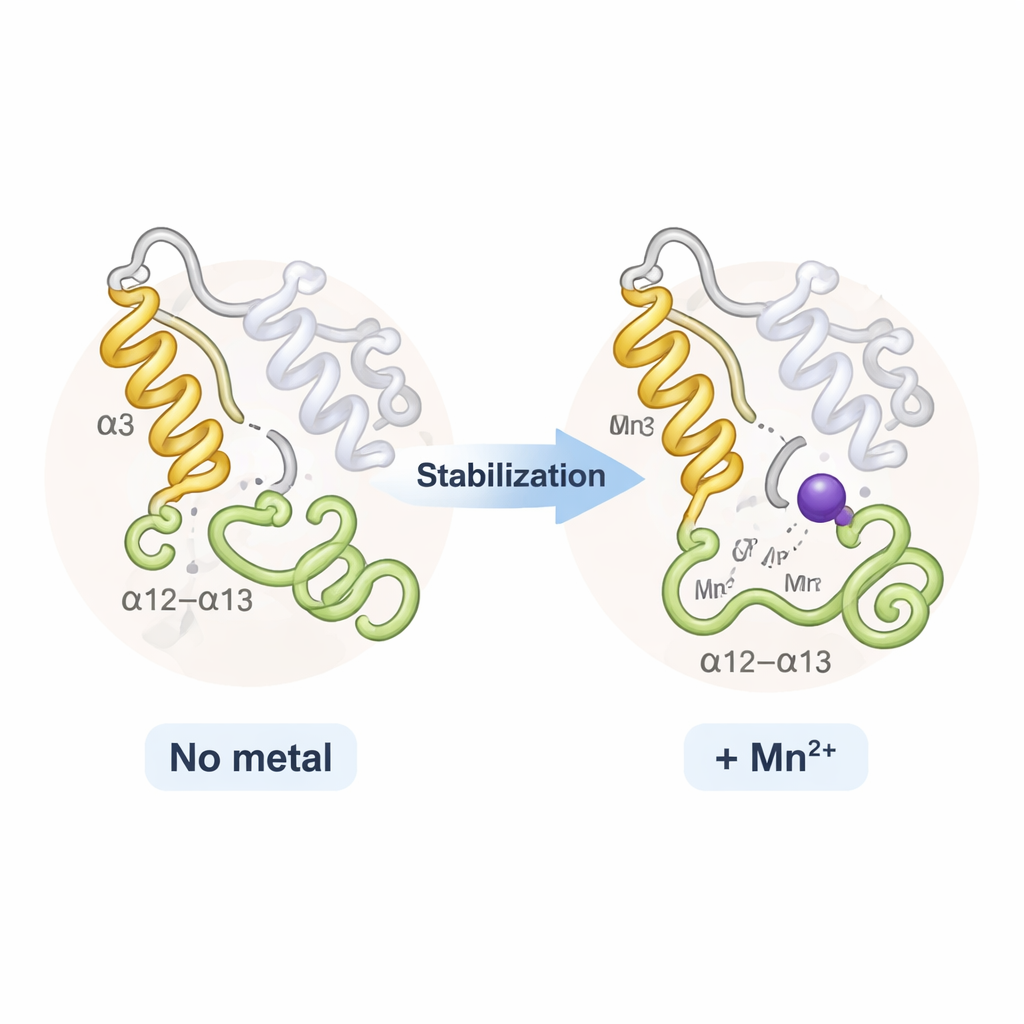
Hücre minerallerinden sinyal kontrolüne
Yazarlar “düzenlenme ile etkinleştirme” modeli öneriyor. Bağlı metal yokken TPST2 aktif bölge girişinde gevşek davranır ve verimsiz çalışır. Hücrelerde bol bulunan sodyum aynı bölgeleri bağlayarak kısmen düzenli, ılımlı derecede aktif bir durum yaratabilir. Golgi içinde mikromolar düzeylerde dikkatle kontrol edilen mangan ise daha güçlü bağlanır ve kilit bölgeleri optimal şekilde düzenlenmiş hâlde kilitler, böylece katalitik verimliliği en üst düzeye çıkarır. Bu, Golgi mangan seviyelerindeki küçük değişimlerin TPST2’nin hedeflerini ne kadar güçlü değiştirdiğini ayarlayabileceğini öne sürer. TPST2 hormon üretimini ve kanser sinyalleşmesini etkilediğinden bu çalışma, metal iyon dengesi, protein “süslemeleri” ve hastalıklar arasında potansiyel bir bağlantıya işaret ediyor ve metal bağlanmasını taklit ederek veya bozarak TPST2 aktivitesini modüle eden ilaçlar tasarlamak için yapısal bir çerçeve sunuyor.
Atıf: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Anahtar kelimeler: tirosin sülfasyonu, TPST2, mangan, Golgi aygıtı, protein modifikasyonu