Clear Sky Science · tr
Genom çapında taramalar, hücre yüzeyindeki prion proteini ifadesinin çekirdek düzenleyicilerini belirliyor
Beyin sağlığı için neden önemli
Creutzfeldt–Jakob hastalığı (insanlarda) ve “deli dana” hastalığı (sığırlarda) gibi prion hastalıkları nadir olmakla birlikte her zaman ölümcül olan beyin bozukluklarıdır. Temel suçlulardan biri, yanlış katlanıp hücreden hücreye yayılabilen normal bir beyin proteini olan prion proteindir. Bu proteinin sinir hücrelerinin yüzeyinde ne kadar çok bulunduğu, hastalığın yerleşmesini o kadar kolaylaştırır. Bu çalışma, tüm genom boyunca hangi genlerin nöron benzeri hücrelerin dış yüzeyinde ne kadar prion proteini göründüğünü kontrol ettiğini haritalamayı amaçladı. Bu harita, bilim insanlarının bu proteini azaltmanın ve potansiyel olarak bir dizi nörodejeneratif hastalığı yavaşlatmanın yeni yollarını tasarlamasına yardımcı olabilir.
Hücudun kontrol düğmelerini bulmak
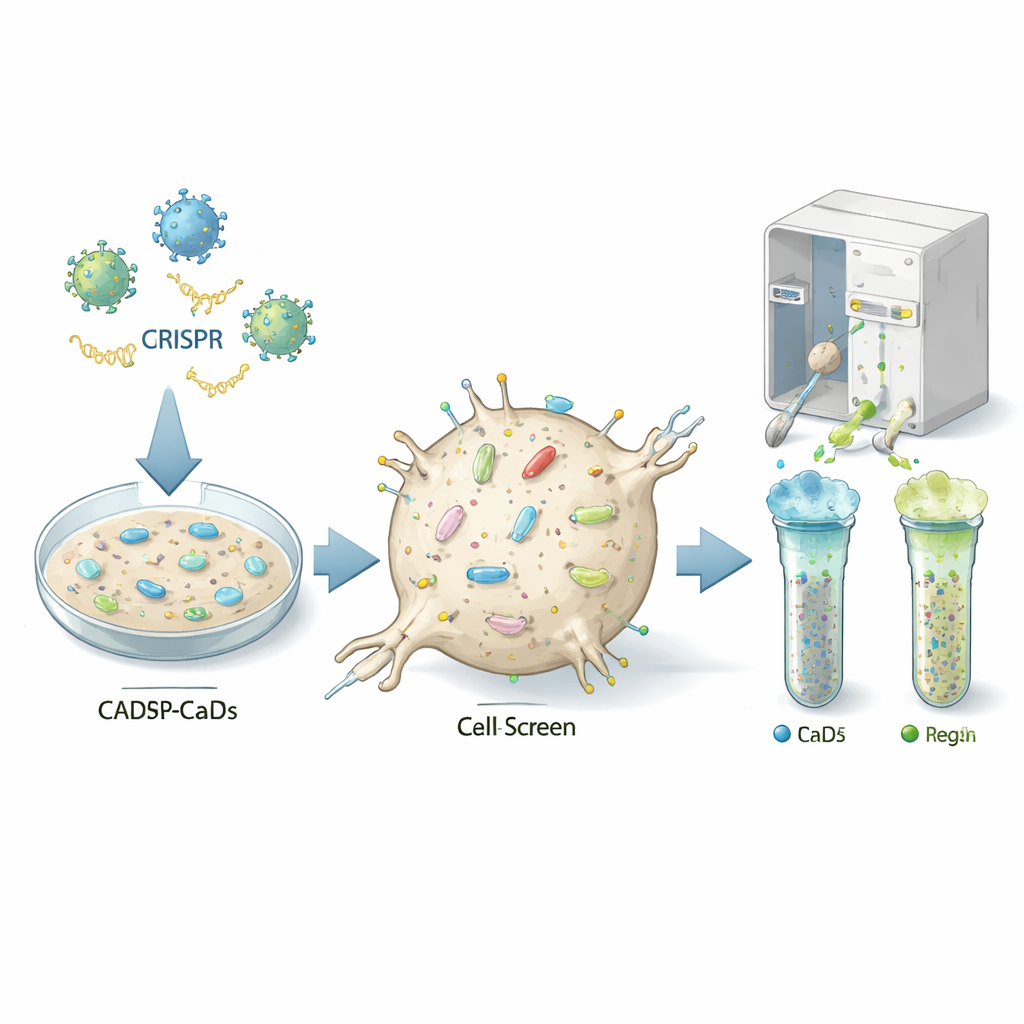
Yazarlar, hemen hemen her geni tek tek devre dışı bırakmak için güçlü bir gen düzenleme yöntemi olan CRISPR’i kullandılar; model olarak prionlarla enfekte olabilen fare kökenli bir nöron benzeri hücre hattı (CAD5 hücreleri) kullanıldı. Her hücreye farklı bir genetik “vuruş” verildi; böylece ortaya çıkan popülasyon, her biri belirli bir genden yoksun milyonlarca varyant içeriyordu. Ekip daha sonra hücre yüzeyindeki normal prion proteinini tanıyan floresan antikorlarla hücreleri boyadı ve bu proteinin olağandışı derecede düşük veya yüksek seviyelerine sahip hücreleri ayırmak için bir hücre ayırma (sıralama) cihazı kullandı. Düşük veya yüksek gruplarda hangi kılavuz RNA’ların zenginleştiğini dizileyerek, hangi knock-out genlerin normalde hücre yüzeyindeki prion proteini için açma ya da kapama düğmesi olarak davrandığını çıkarabildiler.
İki hücre durumu, örtüşen yanıtlar
Nöronlar yaşam süreleri boyunca aynı görünmez veya davranmazlar, bu yüzden araştırmacılar aynı genlerin farklı hücre durumlarında prion proteinini kontrol edip etmediğini sordular. CAD5 hücreleri hızlı büyüyen, daha az özelleşmiş bir durumda tutulabilir veya kültür ortamından serum çıkarılarak daha olgun, nöron benzeri bir forma yönlendirilebilir. Ekip aynı genom çapında CRISPR taramasını her iki koşulda da çalıştırdı. Farklılaşmamış (daha az olgun) hücrelerde, yüzey prion proteinini var olduklarında artıran 46 ve azaltan 21 geni doğruladılar. Farklılaşmış (daha nöron benzeri) hücrelerde 41 olumlu ve 13 olumsuz düzenleyici doğrulandı. Yirmi üç gen—çoğunlukla proteine bir lipid “ankraj” eklenmesine yardımcı olanlar—her iki hücre durumunda paylaşıldı; bu da olgunluktan bağımsız olarak işleyen temel bir düzenleyici mekanizmayı vurguluyor.
En önemli montaj hatları
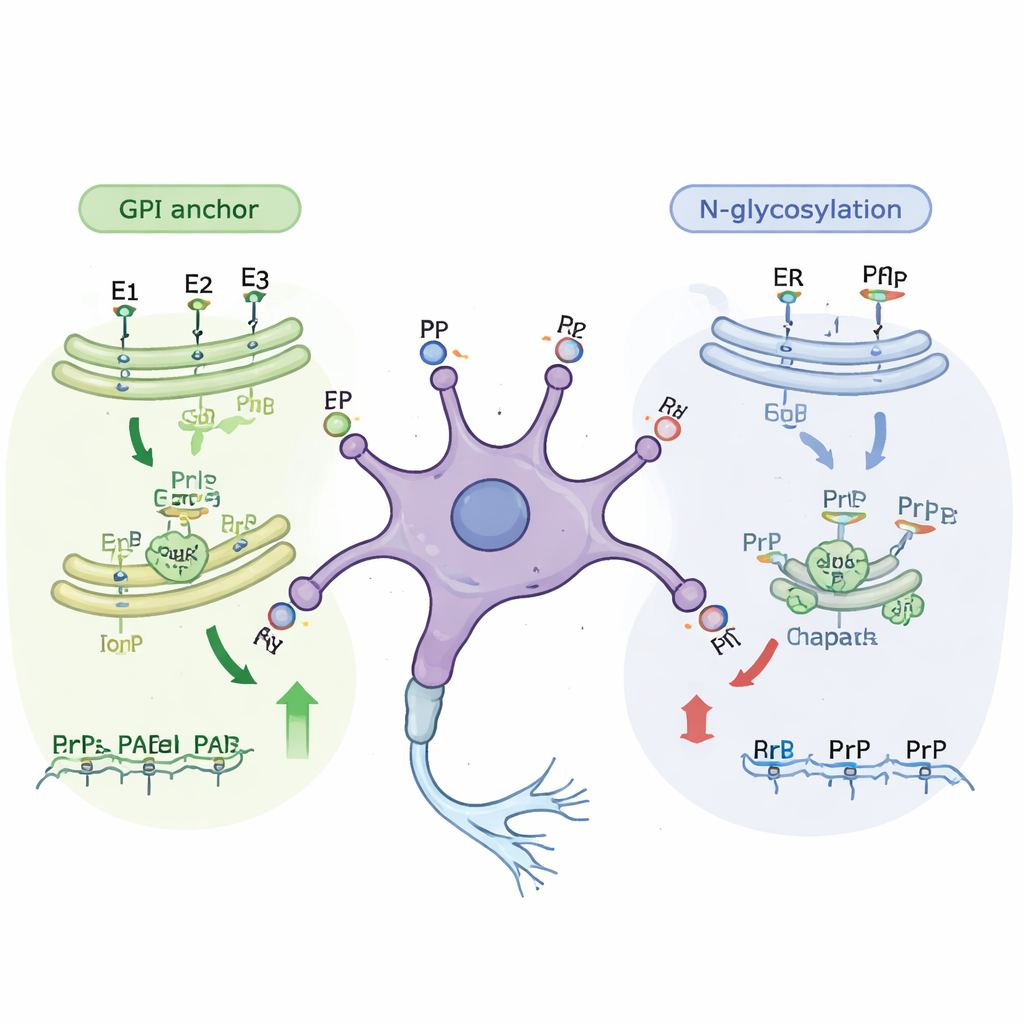
İleri analizler, yeni tanımlanan birçok genin, yüzeye giderken proteinleri değiştiren bilinen hücresel “montaj hatlarına” ait olduğunu ortaya koydu. Birincil yol, prion proteinini hücre zarının dış yüzüne bağlayan yağca zengin küçük bir yapı olan GPI ankrajını inşa eder. Bu yolun neredeyse her adımının bozulması, hem olgunlaşmamış hem de olgun hücrelerde yüzeye ulaşan prion protein miktarını azalttı. İkinci bir yol ise N-bağlantılı glikozilasyonu içerir; bu süreçte karmaşık şeker zincirleri proteinin hücrenin iç membranları boyunca ilerlerken eklenir. Bu şeker ekleme yolundaki genler özellikle daha az olgun hücrelerde önemli olarak ortaya çıktı. Araştırmacılar, belirli glikozilasyon adımlarını engelleyen küçük moleküllerle hücreleri muamele ettiklerinde, yüzey prion proteini seviyeleri hücreleri öldürmeden yaklaşık üçte bir düştü; bu da genetik bulguları doğruladı.
Yardımcı proteinler ve stres yanıtları
Taramalar ayrıca diğer proteinlerin doğru katlanmasına yardımcı olan moleküler şaperonları prion düzenleyicileri olarak öne çıkardı. Özellikle Hspa5 (BiP olarak da adlandırılır), hücrenin protein katlanma bölmesindeki merkezi bir şaperon, daha nöron benzeri hücrelerde pozitif bir düzenleyici olarak belirdi. Araştırmacılar Hspa5’i bir ilaçla inhibe ettiklerinde, yüzey prion proteini seviyeleri her iki hücre durumunda da belirgin bir hücre zararı olmadan düştü. Diğer bulgular arasında proteinlerin hücre içinden taşınmasında görevli genler, genlerin açılıp kapanmasını kontrol edenler ve sinaps işlevi ile Alzheimer ve ALS gibi diğer beyin hastalıklarıyla bağlantılı birkaç protein vardı. Birlikte, bu sonuçlar hücre yüzeyindeki prion proteini seviyelerinin protein üretimi, modifikasyonu, taşınması ve kalite kontrolünü kapsayan bir yol ağı tarafından şekillendirildiğini gösteriyor.
Gelecek tedaviler için ne anlama geliyor
Bu çalışma, prion enfeksiyonuna duyarlı nöron benzeri hücrelerin yüzeyinde ne kadar prion proteini göründüğünü kontrol eden genlerin ilk kapsamlı kataloğunu sunuyor. Bu genlerin bazıları—özellikle GPI-ankraj ve N-glikozilasyon yollarındaki genler ile Hspa5 şaperon sistemi—ilaç keşfi için umut verici başlangıç noktaları olarak öne çıkıyor: Bunların aktivitesini azaltmak, yanlış katlanmaya yatkın prion proteini miktarını düşürmelidir ve önceki çalışmalar kısmi azalmaların hayvanlarda hastalığı önemli ölçüde geciktirebildiğini gösteriyor. Aynı zamanda, olgunlaşmamış ve olgun hücreler arasındaki belirgin farklar, hedef seçerken beyin hücresi durumunun önemli olduğunu vurguluyor. Bu genleri manipüle etmenin gerçek prion enfeksiyonu ve canlı beyinlerdeki diğer nörodejeneratif durumlar üzerindeki etkisini test etmek için daha fazla çalışma gerekli olsa da, bu çalışma araştırmacıların bu yıkıcı hastalıkları yavaşlatmak veya önlemek için keşfedebileceği hücresel kolların bir yol haritasını sunuyor.
Atıf: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Anahtar kelimeler: prion proteini, CRISPR taraması, nörodejenerasyon, protein glikozilasyonu, GPI ankrajı