Clear Sky Science · tr
Makine öğrenimi modellerine dayalı akciğer kanserinin cerrahi sonrası uzak metastazını tahmin etmeye yönelik karşılaştırmalı çalışma
Neden kanser yayılımını tahmin etmek önemli
Akciğer kanseri, cerrahların görülebilen tüm tümörleri çıkarmasına rağmen hâlâ en ölümcül kanserlerden biridir. Birçok hastada daha sonra beyin, kemikler, karaciğer veya diğer organlarda gizli kanser odakları ortaya çıkar. Hekimler, cerrahiden kısa süre sonra hangi hastaların bu tür uzak yayılım açısından daha yüksek risk taşıdığını bilmek ister; böylece takip ziyaretleri ve tedaviler kişiye göre ayarlanabilir. Bu çalışma, hastanelerin rutin bakım sırasında zaten topladığı bilgiler kullanılarak modern bilgisayar programlarının (makine öğrenimi modelleri) kimlerin daha yüksek risk taşıdığını öngörmede yardımcı olup olamayacağını araştırıyor.
Çok sayıda hastayı yakından incelemek
Araştırmacılar, Çin’de tek bir kanser merkezinde tümörü alınmış evre I–III akciğer kanseri olan 3.120 kişinin kayıtlarını inceledi. Hepsinin en az iki yıllık takibi vardı. Her hasta için ekip, yaş, cinsiyet, vücut ağırlığı, sigara öyküsü, tarama bulguları, ameliyat ayrıntıları, laboratuvar testleri ve ameliyat sonrası kemoterapi veya radyoterapi gibi ek tedaviler alıp almadığı da dahil olmak üzere 52 tür bilgi topladı. Zaman içinde bu hastalardan 596’sında uzak metastaz gelişirken 2.524’ünde gelişmedi. Bu gerçek dünya karışımı ekipin hangi özelliklerin gelecekteki yayılımla ilişkili olduğunu görmesini sağladı.
Bilgisayarlara risk desenlerini öğretmek
Tek bir formüle dayanmak yerine, bilim insanları basit karar ağaçlarından birçok küçük modeli birleştiren daha gelişmiş tekniklere kadar dokuz farklı makine öğrenimi yöntemini karşılaştırdı. Önce orijinal 52 faktörü daha küçük, daha bilgilendirici bir kümeye daraltmak için matematiksel bir filtre kullandılar. Ardından tekrarlanan turlarda her modeli verinin bir bölümünde eğittiler ve hiç “görmediği” hastalar üzerinde test ettiler. Hastaların yaklaşık beşte birinde metastaz geliştiği için, bilgisayarın herkes için basitçe “düşük risk” tahmin etmemesi adına eğitim ayarlandı. Performansı, yüksek-risk ile düşük-risk hastaları ne kadar iyi ayırdıkları ve tahmin edilen risklerin gerçekte olanla ne kadar örtüştüğü gibi çeşitli ölçütlerle değerlendirdiler.
En güvenilir modeli bulmak
Dokuz yaklaşım arasında Gradient Boosting Decision Tree (GBDT) adı verilen yöntem öne çıktı. Test verilerinde hastaları yaklaşık %77 doğrulukla doğru sıraladı ve ayrım gücünün özet skoru (ROC eğrisi altındaki alan) 0,81 olarak bulundu; bu, tıbbi tahmin araçları için güçlü kabul edilir. Model özellikle metastazsız kalacak hastaları tanımlamada başarılıydı (yüksek “negatif prediktif değer”), yani düşük risk sonucu genellikle güven vericiydi. Ekip, modelin birçok farklı rastgele veri bölünmesi boyunca nasıl davrandığını incelediğinde performansı istikrarlı kaldı; bu da modelin yalnızca belirli bir alt kümenin özelliklerini ezberlemediğini gösteriyor.
Modelin kararlarını ne etkiliyor
Makine öğreniminin ortak bir eleştirisi onun “kara kutu” olmasıdır. Bunu ele almak için yazarlar, her faktöre her hasta için nihai risk tahminine katkı atan SHAP adlı bir açıklama yöntemi kullandı. Bu analiz, en güçlü sinyallerin ameliyat sonrası kemoterapi veya radyoterapi alıp alınmadığı, kaç lenf düğümünde kanser olduğu, yaş, vücut kitle indeksi (VKİ) ve preoperatif nötrofil sayısı (bir tür beyaz kan hücresi) olduğunu gösterdi. Daha ileri lenf düğümü tutulumuna ve sistemik inflamasyon belirtilerine sahip hastaların tahmini riskleri genellikle daha yüksekti. Yazarlar, kemoterapi ve radyoterapinin yüksek katkı göstermesinin bu tedavilerin metastaza neden olduğu anlamına gelmediğini; bunun yerine hekimlerin hastalığı daha agresif olarak değerlendirdiğinin bir işareti olduğunu ve bu hastaların başlangıçta daha yüksek riskli olduğunu vurguluyorlar.
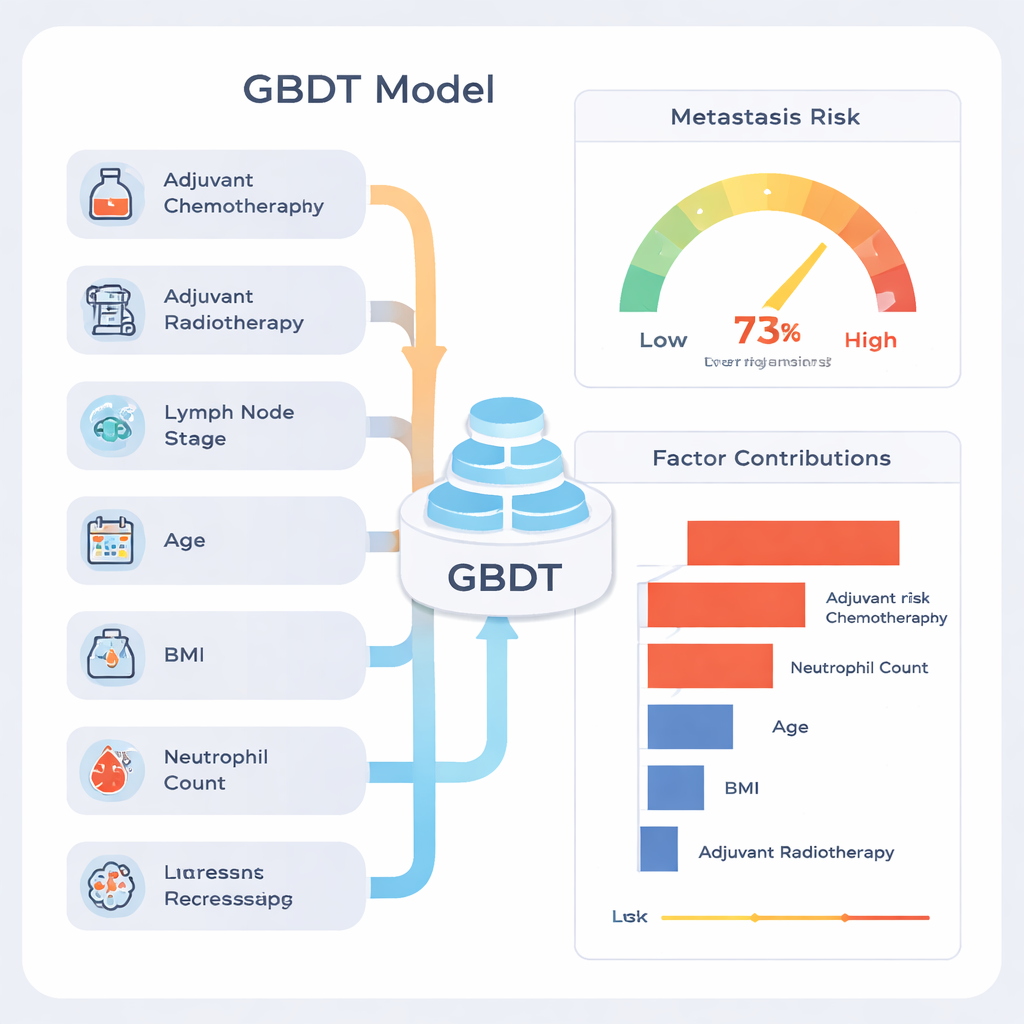
Bu hastalar için pratikte nasıl yardımcı olabilir
Model, çoğu kanser merkezinin zaten kaydettiği bilgileri kullandığı için, ek testlerden sonra hastane yazılımlarına entegre edilebilir. Yeni bir akciğer ameliyatı olmuş hasta için sistem verilerini çekip uzak metastaz olasılığına dair kişiselleştirilmiş bir tahmin ve riskin artmasına veya azalmasına neden olan faktörlerin basit bir açıklamasını verebilir. Klinikler bunu, kimlerin daha sık görüntülemeyle izlenmesi, ek danışmanlık alması veya klinik çalışmalara dahil edilmesi gerektiğine, kimlerin ise yoğun takipten güvenle kaçınabileceğine karar vermede kullanabilir. Çalışma tek bir hastanede yapıldığından araç başka bölgelerde ve sağlık sistemlerinde de doğrulanıp geliştirilmelidir. Ancak rutin klinik verilerle şeffaf makine öğrenimini birleştirerek akciğer kanseri olan kişilerin uzun süreli bakımını iyileştirmek için ümit verici bir yol haritası sunuyor.
Atıf: Guo, X., Xu, T., Luo, Y. et al. Comparative study on predicting postoperative distant metastasis of lung cancer based on machine learning models. Sci Rep 16, 6468 (2026). https://doi.org/10.1038/s41598-026-37113-w
Anahtar kelimeler: akciğer kanseri, uzak metastaz, makine öğrenimi, risk tahmini, cerrahi sonrası takip