Clear Sky Science · tr
RBX1’in LIPT1 transkripsiyonunun düzenleyicisi olarak tanımlanması ve GBM hücrelerinde bakır kaynaklı hücre ölümündeki rolü
Niçin bakır ve beyin tümörleri önemli
Glioblastoma multiforme, agresif cerrahi, radyasyon ve kemoterapiye rağmen teşhis sonrası hastaların çoğunun kısa süre yaşadığı en ölümcül beyin kanseri türlerinden biridir. Bu çalışma, bu tümörlere karşı beklenmedik bir müttefiki araştırıyor: bakır elementi. Araştırmacılar, bakır tarafından tetiklenen yeni tanımlanmış bir hücre ölümü biçimini inceliyor ve doktorların bu süreci kullanarak tümörleri zayıflatmasına ve potansiyel olarak bağışıklık sisteminin kanser hücrelerine saldırısını güçlendirmesine yardımcı olabilecek moleküler bir yolak belirliyor.
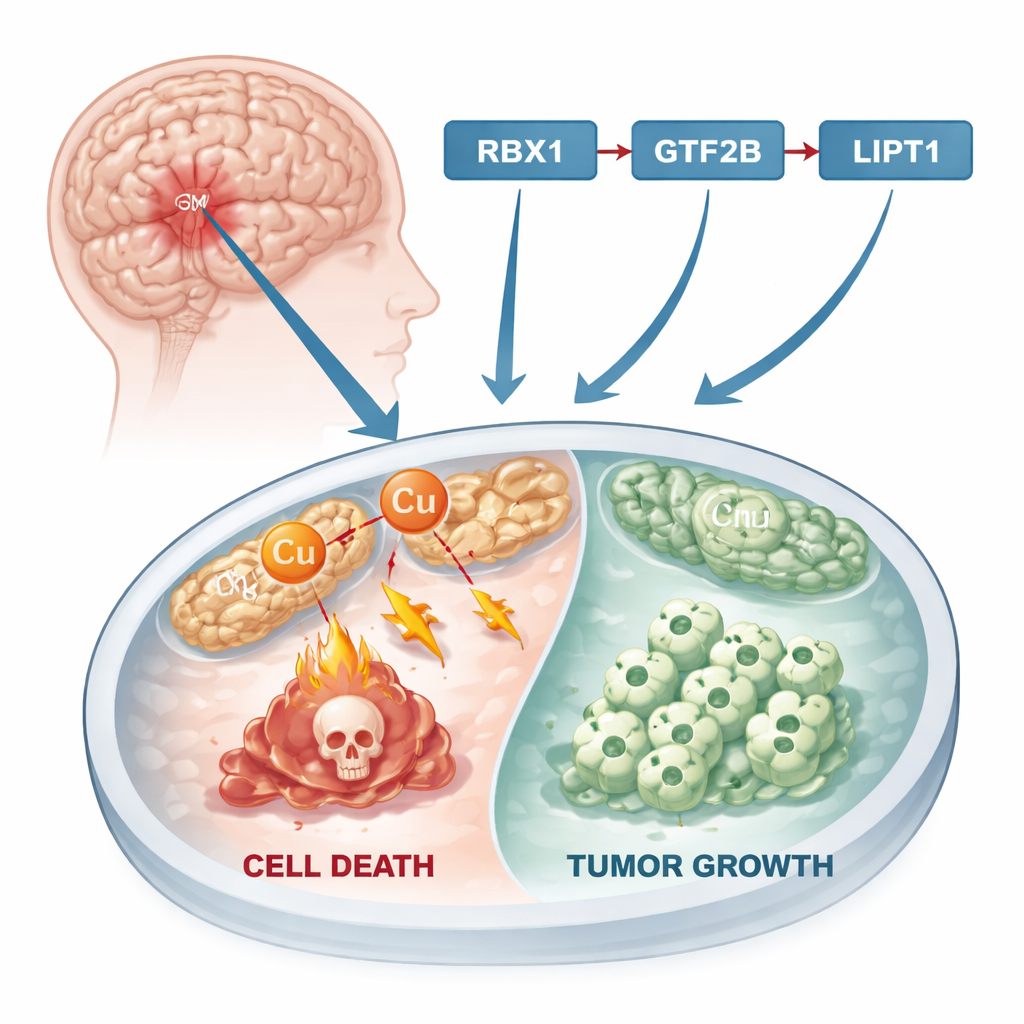
Hücrelerin ölme şekline yeni bir yol
On yıllardır kanser araştırmaları, hasarlı hücrelerin sessizce kendini kapattığı apoptoz gibi tanıdık hücre ölümü biçimlerine odaklandı. Son zamanlarda bilim insanları, bakır kaynaklı hücre ölümü ya da “cuproptoz” olarak adlandırılan farklı bir yol keşfettiler. Bu süreçte, hücrenin enerji merkezleri olan mitokondrilerde aşırı bakır birikir. Bu bakır, temel proteinleri bozarak toksik kümelerin oluşmasına neden olur ve nihayetinde hücreyi öldürür. Birçok tümörde metal metabolizmasının değişmiş olması ve normal dokulardan daha yüksek bakır seviyelerine rastlanması nedeniyle, cuproptoz potansiyel bir baskı noktası sunar: araştırmacılar tümör hücrelerini bu bakır kaynaklı yıkıma itebildiklerinde kanser büyümesini yavaşlatabilir veya durdurabilirler.
Glioblastomada anahtar bir genin ön plana çıkması
Yazarlar, cuproptozda rol oynadığı önceden bilinen bir grup geni tarayarak bunların glioblastoma örneklerinde normal beyin dokusuna kıyasla nasıl davrandığını araştırmakla başladılar. Özellikle LIPT1 adındaki bir gen öne çıktı. Bu gen, glioblastoma dokusunda ve birkaç glioblastoma hücre hattında normal beyin hücrelerine kıyasla daha aktifti. Önemli olarak, tümörlerinde daha yüksek LIPT1 aktivitesi olan hastaların tedavi sonrası kanserin geri dönmesine daha uzun süre ara verdiği gözlendi. Yüksek LIPT1 seviyeleri, tümör ortamını hedef alan bağışıklığın ön saflarındaki CD8 T hücrelerinin daha fazla varlığıyla da ilişkilendirildi; bu da bu genin tümör mikroçevresini bağışıklık saldırısına karşı daha savunmasız hâle getirmeye yardımcı olabileceğini düşündürüyor.
Bakır ölüm anahtarı kapatıldığında ne olur
LIPT1’in gerçekten bakır kaynaklı hücre ölümünü etkileyip etkilemediğini test etmek için ekip, cuproptozu güvenilir şekilde tetikleyen bir bakır taşıyıcı ilaç kombinasyonuna glioblastoma hücrelerini maruz bıraktı. Ardından genetik araçlar kullanarak LIPT1 seviyelerini azalttılar. LIPT1 baskılandığında, tümör hücreleri bakır kaynaklı öldürmeye karşı daha dirençli oldu, daha iyi hayatta kaldı ve daha invazif ve göç edici davranışlar sergiledi—bunlar daha agresif kanserle ilişkili özelliklerdir. Tümör hücreleri ile insan CD8 T hücrelerinin karışık kültürlerinde, LIPT1’in düşürülmesi ayrıca immün sinyal moleküllerinin salımını azalttı ve T hücrelerinin kanser hücrelerini yok etmesini zorlaştırdı. Bu deneylerin tamamı, LIPT1’in bakır kaynaklı ölüme duyarlılığı artırdığını ve tümöre karşı bağışıklık aktivitesini desteklediğini gösteriyor.
Komuta zincirini RBX1’e kadar izlemek
Bir sonraki zorluk, LIPT1’in glioblastomada neden arttığını anlamaktı. Birkaç büyük gen ve protein veritabanını birleştirerek, LIPT1 geninin yakınında bağlanıp muhtemelen ifadesini artıran bir transkripsiyon faktörü—gen aktivitesi için türünün bir anahtarı—olan GTF2B’yi belirlediler. Ardından GTF2B’yi neyin kontrol ettiğini sordular. İkinci bir protein olan RBX1 güçlü bir aday olarak ortaya çıktı. RBX1, diğer proteinleri parçalanmak üzere etiketleyen hücrenin işaretleme ve bertaraf sistemi parçalarından biridir. Glioblastoma hücrelerinde RBX1 seviyeleri normal beyin hücrelerine göre daha düşüktü; oysa GTF2B ve LIPT1 daha yüksekti. Laboratuvar testleri, RBX1’in GTF2B’ye küçük “beni yok et” etiketleri ekleyebildiğini ve bunun sonucunda GTF2B’nin parçalandığını gösterdi; RBX1 arttırıldığında GTF2B seviyeleri ve LIPT1 aktivitesi düştü ve hücrenin parçalama mekanizmasını engellemek bu etkiyi tersine çevirdi.
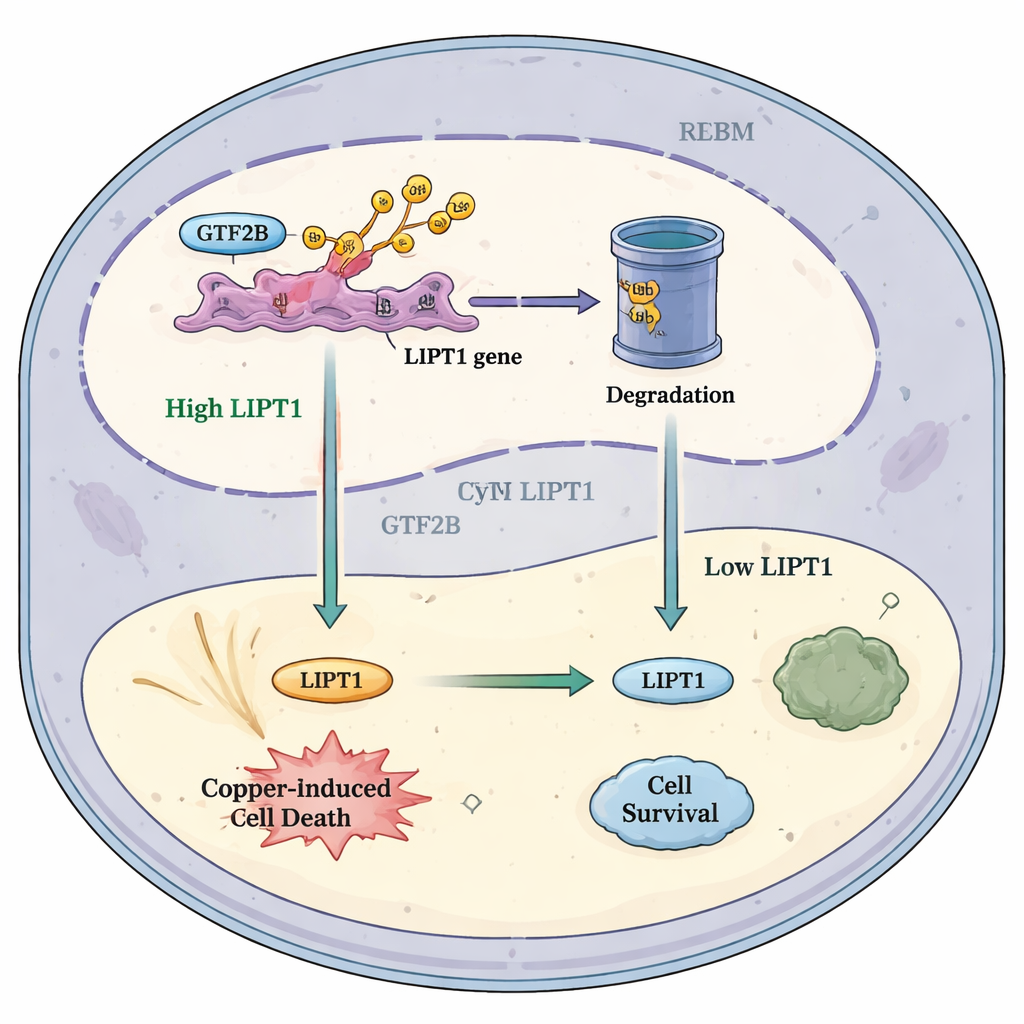
Bu yolak gelecekteki tedavilere nasıl yardımcı olabilir
Bu bulguları birleştiren yazarlar basit bir model öneriyor: sağlıklı koşullarda RBX1, GTF2B’yi kontrol altında tutar ve LIPT1 genini ne kadar güçlü etkinleştirdiğini sınırlar. Glioblastomada RBX1’in azalması, daha az GTF2B’nin parçalanması anlamına gelir. Fazladan GTF2B ise LIPT1’i artırır, böylece tümör hücrelerinin bakır kaynaklı ölüme duyarlılığını yükseltir ve daha fazla kansere karşı savaşan bağışıklık hücresini çeker. Bu model, RBX1–GTF2B–LIPT1 yolunu dikkatli şekilde ayarlamanın, muhtemelen bakır hedefli ilaçlar ve immünoterapilerle birlikte, beyin tümörlerinin içinde yıkımı teşvik edebileceğini öne sürer. Bu fikrin hastalara ulaşmasından önce halen çok çalışma gerekse de, çalışma metal biyolojisi, gen düzenlemesi ve kanser immünolojisinin umut verici bir kesişimini vurgulayarak en inatçı kanserlerden biri için yeni terapötik yollar açabilir.
Atıf: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Anahtar kelimeler: glioblastoma, bakır kaynaklı hücre ölümü, LIPT1, tümör immünolojisi, RBX1 yolu