Clear Sky Science · tr
Makine öğrenimi ile tümör içi lenfositlerin otomatik nicelenmesi, akciğer kanserinde prognostik ve immünyomik özellikleri ortaya koyuyor
Akciğerdeki küçük bağışıklık hücrelerini saymanın önemi
Akciğer kanseri hâlâ en ölümcül kanserlerden biri, ancak tüm tümörler aynı davranmıyor. Bazıları tümör içine giren bağışıklık hücreleri tarafından yoğun şekilde devriye gezilirken, diğerleri neredeyse dokunulmamış kalıyor. Bu tümör-infiltre eden lenfositler (TIL'ler) hastanın gidişatı ve modern immünoterapi ilaçlarından yararlanıp yararlanmayacağı konusunda ipuçları verebilir. Zorluk şu ki günümüzde TIL'ler genellikle mikroskop altında gözle sayılıyor; bu, yavaş ve öznel bir yöntem. Bu çalışma güncel bir soruyu soruyor: rutin patoloji lamları üzerinde bu hücreleri otomatik olarak ölçmek için makine öğrenimini kullanabilir miyiz ve bunun akciğer kanseri biyolojisi ile hasta sağkalımı hakkında ne gibi bilgiler verdiğini öğrenebilir miyiz?
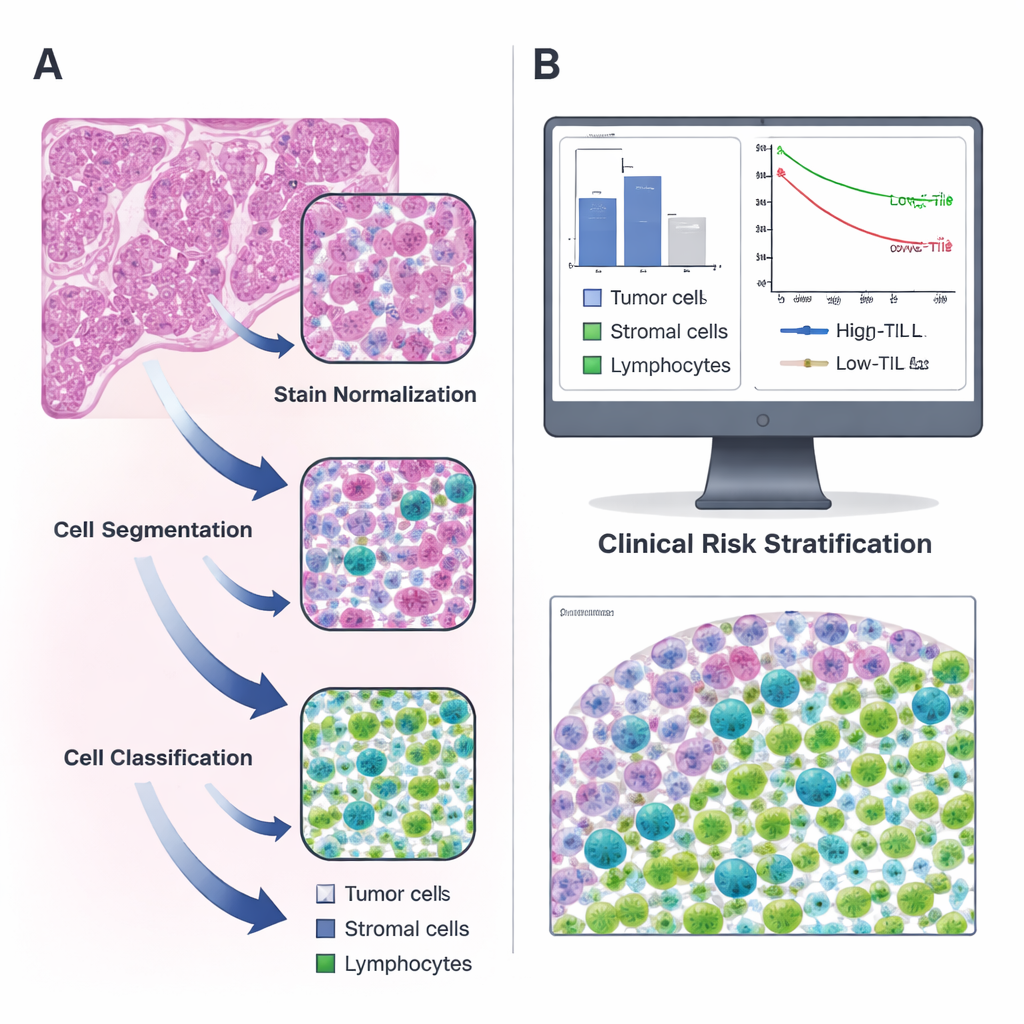
Gündelik lamları dijital haritalara dönüştürmek
Araştırmacılar, yaygın bir akciğer kanseri türü olan akciğer adenokarsinomuna odaklandı ve The Cancer Genome Atlas'tan (TCGA) kamuya açık veriler ile kendi hastanelerinden bağımsız bir hasta setini kullandılar. Her hasta için standart hematoksilin-eozin (H&E) ile boyanmış doku lamlarını analiz ettiler; her patologun iyi bildiği pembe-mor görüntüler. Açık kaynak QuPath yazılımı ile basamaklı bir boru hattı oluşturdular: önce lamlar arasındaki renk farklılıklarını düzelttiler; sonraki adımda, çakışan hücre çekirdeklerini ayırmak için watershed algoritması kullandılar; son olarak, eğitilmiş bir bilgisayar sınıflayıcısı tespit edilen her hücreyi tümör, destek doku (stroma) veya lenfosit olarak etiketledi. İki uzman patolog, makinenin işleri güvenilir şekilde kendi başına tanıyana dek çıktıları tekrar tekrar gözden geçirip düzeltti.
Bağışıklık hücresi sayımlarını hasta sonuçlarıyla ilişkilendirmek
Sistem hücreleri güvenle tanıyabildiğinde, ekip 300'den fazla hasta için milimetrekare başına düşen lenfosit sayısını hesapladı. TIL düzeylerinin geniş bir aralıkta değiştiğini ve ortalamada tüm hücrelerin yalnızca küçük bir kısmını oluşturduğunu buldular. En bilgilendirici eşik değeri belirlemek için istatistiksel bir yaklaşım kullanarak milimetrekare başına 135 TIL'i “yüksek” ve “düşük” TIL tümörleri arasındaki ayırma noktası olarak seçtiler. Bu eşiğin üzerindeki tümörlere sahip hastalar, bağışıklık hücresi infiltrasyonu seyrek olanlara göre daha uzun yaşadı ve bu desen hem orijinal hem de doğrulama gruplarında devam etti. Başka bir deyişle, otomatik bir araç tarafından üretilen basit bir sayı, el ile saymaya dayanan daha emek yoğun önceki çalışmaları yansıtarak sağkalımda anlamlı farkları yakaladı.
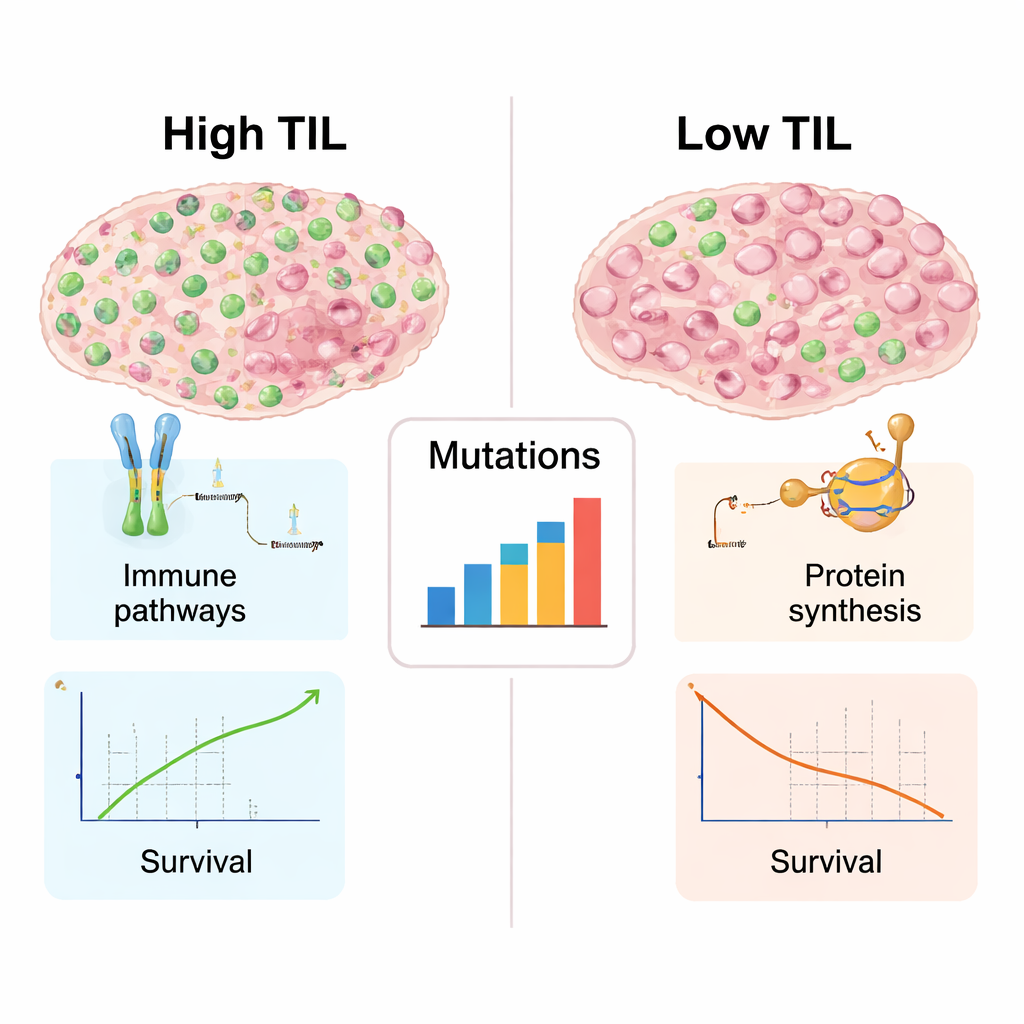
Bağışıklıkça zengin tümörlerin iç yüzü
Birçok tümör için genetik ve moleküler veriler mevcut olduğundan, yazarlar yüksek‑TIL ile düşük‑TIL kanserleri hücre sayılarının ötesinde ayıran özellikleri inceleyebildiler. Lenfositlerle dolu tümörler daha güçlü immün aktivite imzaları gösterdi: anormal proteinlerin tanınması, bunların T hücrelerine sunulması ve bağışıklık saldırısının koordine edilmesiyle ilgili genler daha aktifti. Bu tümörler ayrıca bağışıklık sistemine yeni hedefler yaratabilen daha geniş bir DNA mutasyon karışımına sahipti. Buna karşılık, düşük‑TIL tümörler ribozom üretimi ve protein yapımıyla ilişkili genleri öne çıkarıyordu; bu, yoğun büyüme mekanizmasına işaret ederken bağışıklık etkileşiminin görece sessiz olduğunu gösteriyor. Bu ayrım, immün hücrelerle zengin ve immünoterapilere daha yatkın “sıcak” tümörlerle, bağışıklık tarafından büyük ölçüde göz ardı edilen “soğuk” tümörler arasındaki bilinen karşıtlığı yansıtıyor.
Bir bilgisayara bağışıklık durumunu tahmin etmeyi öğretmek
Ekip bir adım daha ileri gidip kompakt bir görüntü özellikleri setinin her bir lenfositin tek tek sayılmasına gerek kalmadan bir tümörün yüksek mi yoksa düşük‑TIL kategorisine gireceğini tahmin edip edemeyeceğini sordu. Lamlar üzerindeki piksel yoğunluklarının küçük komşuluklar boyunca nasıl değiştiği gibi ince dokusal desenleri—so‑called Haralick özellikleri—özetlediler ve bunları tümörün klinik evresi ile birlikte bir random forest modelinde birleştirdiler. Çapraz doğrulamada, bu sınıflayıcı yüksek‑ ve düşük‑TIL tümörleri güçlü doğrulukla ayırdı ve bağımsız hastane kohortunda makul performansını korudu. Önemli olarak, tüm yaklaşım standart bilgisayarlarda serbestçe erişilebilir yazılımlar kullanılarak çalışıyor; bu da birçok patoloji laboratuvarının özel donanım gerekmeden bunu benimseyebileceğini düşündürüyor.
Gelecekteki akciğer kanseri bakımına etkileri
Uzman olmayan biri için temel mesaj şu: bir bilgisayar, rutin akciğer kanseri lamlarını bağışıklık sisteminin tümöre ne kadar güçlü bağlandığını yakalayan bir biçimde okumayı öğrenebilir. İnfiltre eden lenfositlerin yüksek düzeyleri daha aktif bir bağışıklık savaşı, daha zengin bir mutasyon manzarası ve daha iyi genel sağkalım sinyalleri verir. Ancak özellikle immünoterapiyle tedavi edilen hastalarda daha fazla çalışma gerekli; yine de bu otomatik yöntem sonunda doktorların tümörleri hızlı ve tutarlı biçimde immün “sıcak” ve “soğuk” kategorilere ayırmasına yardımcı olabilir. Bu da kimlerin immün temelli tedavilerden en çok yararlanma olasılığı olduğunu belirlemeye rehberlik edebilir ve soğuk tümörleri sıcak hale getirmeye yönelik yeni stratejileri teşvik edebilir.
Atıf: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Anahtar kelimeler: akciğer adenokarsinomu, tümör-infiltre eden lenfositler, makine öğrenimi, dijital patoloji, kanser immünoterapisi