Clear Sky Science · tr
Evrimsel terapi küçük hücre dışı akciğer kanserinde uygulanabilir mi?
Kanser tedavisini evrimsel bir yarışma olarak yeniden düşünmek
Kanser bakımı genellikle basit bir savaş olarak sunulur: mümkün olan en güçlü ilaçları verin ve her kanser hücresini yok etmeye çalışın. Oysa ileri evre küçük hücre dışı akciğer kanseri (KHDAK) gibi hızlı ve agresif kanserlerde bu “maksimum saldırı” yaklaşımı sık sık ters teper. Tümörler önce küçülür, ama neredeyse her zaman geri döner; bu kez baskın olan ilaç dirençli hücrelerdir. Bu çalışma kışkırtıcı bir soruyu gündeme getiriyor: tümörü yok etmeye çalışmak yerine, doktorlar onu evrimleşen bir ekosistem gibi ele alıp ilaç‑duzenlerini, dirençli hücreleri kontrol altında tutmak için kasıtlı olarak bazı ilaç‑duyarlı hücreleri canlı bırakacak biçimde ayarlasalar ne olurdu?
Neden standart yüksek doz tedavi direnci hızlandırabilir
Güncel uygulamada, metastatik KHDAK’li ve belirli genetik değişiklikleri taşıyan hastalara sıklıkla erlotinib gibi tirozin kinaz inhibitörleri (TKI) şeklinde günlük haplar verilir. Bu ilaçlar başlangıçta tümörleri çarpıcı şekilde küçültebilir, ama neredeyse tüm hastalar sonunda nüks eder çünkü dirençli kanser hücreleri hayatta kalıp baskın hale gelir. Doktorlar dozu hastanın tolere edebileceği en yükseğe çıkardığında, esas olarak ilaca iyi yanıt veren duyarlı hücreleri öldürürler. Yüksek dozlarda bile hayatta kalabilen dirençli hücrelerse aniden alan ve besin için daha az rekabetle karşılaşır. Sonuç, en dayanıklı kanser hücreleri için bir evrimsel “kazanım”dır ve tümör sonunda geri döner; şimdi tedavi edilmesi çok daha zordur. 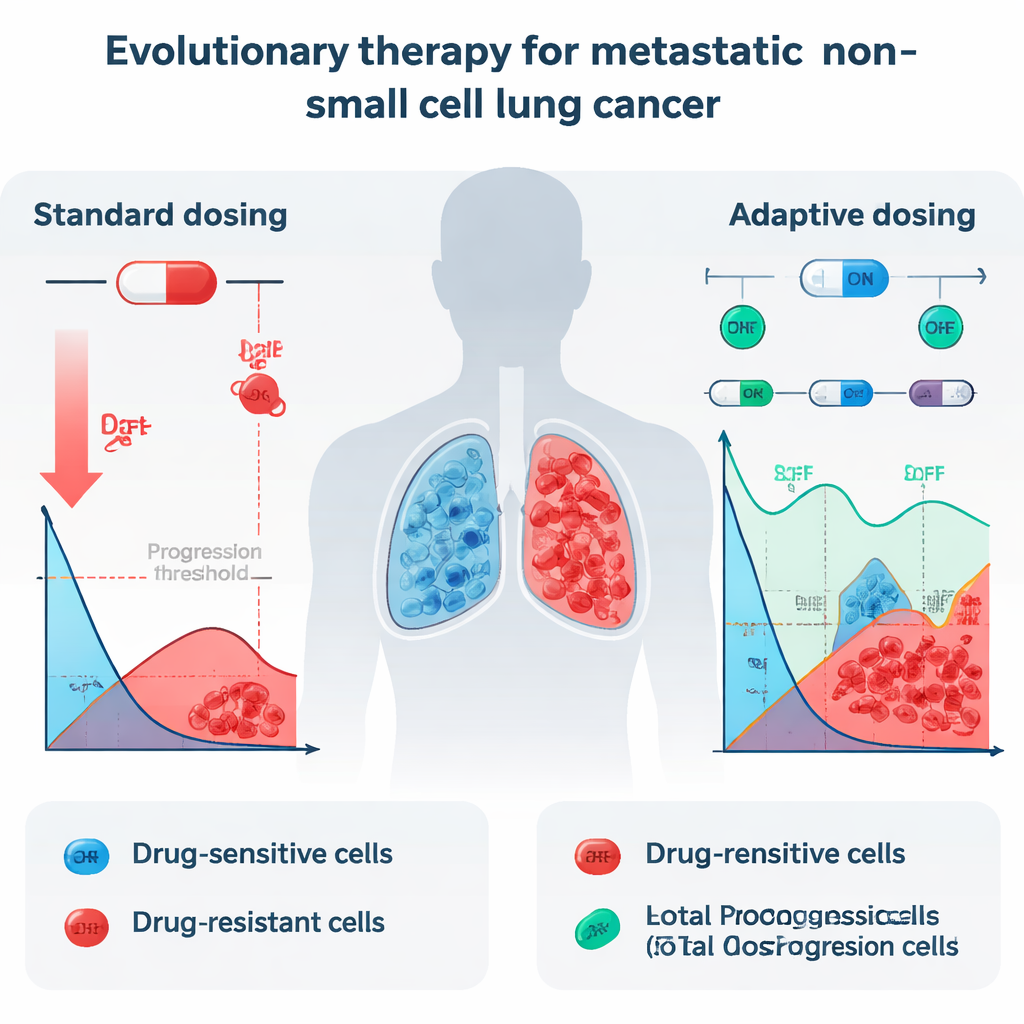
Gerçek hastalarda yeni bir dozlama stratejisini matematikle test etmek
Araştırmacılar, evrimsel terapi adı verilen farklı bir stratejinin IV. evre KHDAK’te işe yarayıp yaramayacağını incelediler. Evrimsel terapi tümörü tamamen ortadan kaldırmayı amaçlamaz. Bunun yerine duyarlı ve dirençli hücrelerin dengeli bir karışımını koruyarak kontrol etmeye çalışır; duyarlı hücrelerin dirençlileri “sıkıştırarak” geri tutmasına izin verir. Ekip, daha önce prostat kanserinde umut verici sonuçlar göstermiş belirli bir aç‑kapa dozlama protokolünü ödünç aldı ve benzer bir stratejinin akciğer kanseri için teorik olarak etkili olup olmayacağını sordu. Bunu yanıtlamak için, bir klinik deneyde erlotinib ile tedavi edilen 13 KHDAK hastasından alınan ayrıntılı tümör boyutu ölçümlerini analiz ettiler, görüntüleri toplam tümör hacmine dönüştürdüler ve bu verileri bir dizi matematiksel modele beslediler.
Direnci gerçekten yakalayan modeli bulmak
Araştırmacılar, tüm kanser hücrelerini iki gruba ayıran 26 farklı tümör büyüme modelini test ettiler: ilaç‑duyarlı ve ilaç‑dirençli. Bu modeller, büyüme limitlerini nasıl tanımladıkları, iki hücre tipinin birbirleriyle nasıl rekabet ettiği, ilacın vücutta nasıl işlendiği ve tedavinin hücreleri nasıl öldürdüğü açısından farklılık gösteriyordu. Tümörler sadece küçülürken birçok daha basit model hasta verilerine makul düzeyde uyum sağladı. Ancak tümörler daha gerçekçi bir “U‑şekilli” seyir izlediğinde—tedaviyle küçülüp sonra direnç ortaya çıktıkça yeniden büyürken—çoğu model başarısız oldu. En iyi eşleşme, iki kritik fikri içeren Gompertz tipi bir modeldi: birincisi, tümörlerin sınırsız büyüyemeyeceği (sıkışmayı hissettiği) ve ikincisi, duyarlı ve dirençli hücrelerin asimetrik bir şekilde rekabet etmesi, yani bir türün başarısının diğer türün sayısına bağlı olması.
Adaptif tedaviyi standart bakım ile karşılaştıran simülasyonlar
En uygun modelleri belirledikten sonra ekip, her hasta için iki tedavi stratejisini simüle etmek üzere bu modelleri kullandı: olağan sabit maksimum doz ve Zhang ve meslektaşlarının ilham verdiği adaptif protokol. Adaptif yaklaşımda erlotinib, tümör başlangıçtaki büyüklüğünün yarısına inene kadar verilir, sonra duyarlı hücrelerin yeniden büyümesine izin vermek için ilaç durdurulur; tümör yeniden başlangıç büyüklüğüne döndüğünde tedavi yeniden başlatılır ve bu döngü tekrarlanır. Hücre tipleri arasındaki rekabeti içeren iyi performans gösteren tüm modellerde, bu adaptif strateji tutarlı şekilde tümörün orijinal boyutunun %110’unu aşmasına kadar geçen süreyi—bir ilerleme gösterge eşiği—uzattı. Rekabet içeren ve en iyi uyumu veren Gompertz modelinde, ilerlemeye kadar geçen medyan süre standart dozlamada yaklaşık 24,8 aydan adaptif protokolde 42,3 aya yükseldi; bu yaklaşık bir buçuk yıllık bir kazanç demekti. 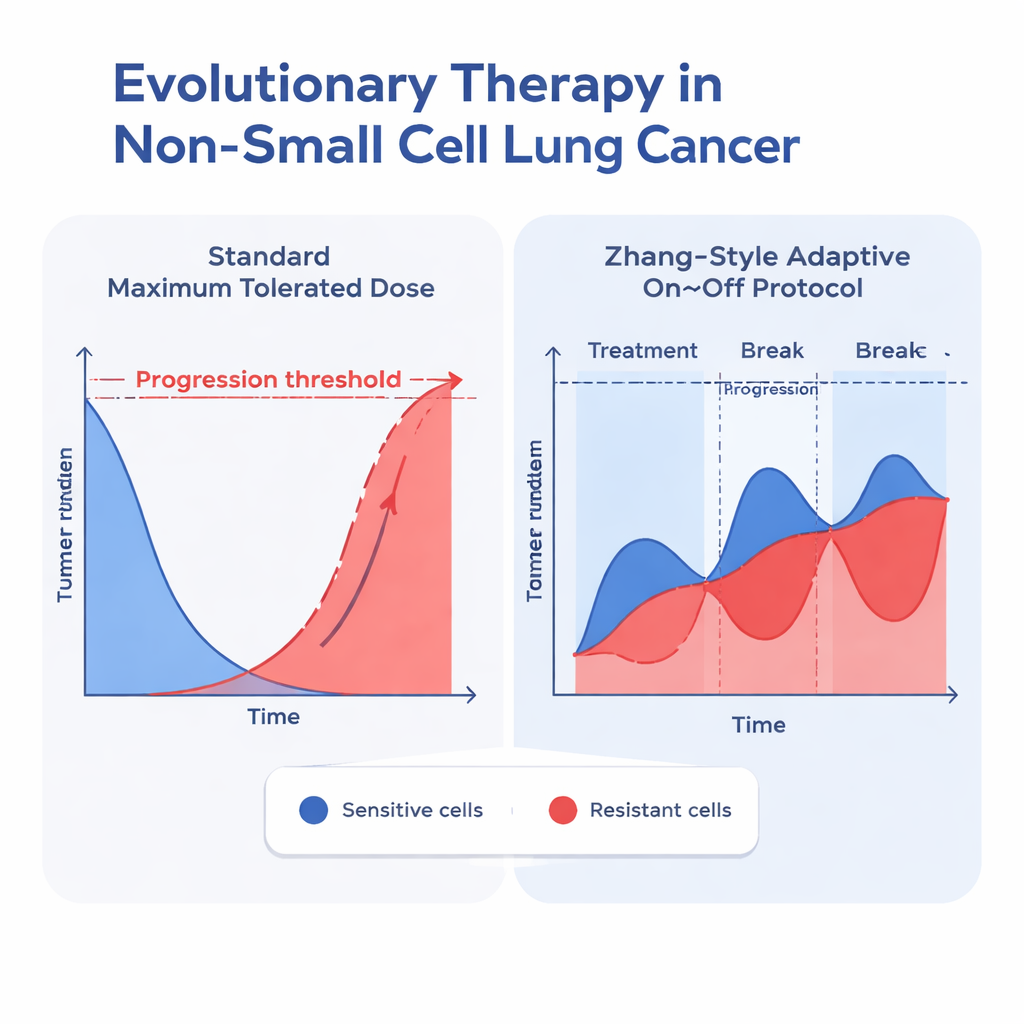
Bu gelecekteki hastalar için ne anlama gelebilir
Bu çalışma henüz doktorların KHDAK hastalarını bugün nasıl tedavi ettiği yöntemleri değiştirmiyor, ancak güçlü bir kavramsal kanıt sunuyor. Modellerini gerçek hasta verilerine dayandırıp, modellerin sadece erken küçülmeyi değil aynı zamanda direnç kaynaklı yeniden büyümeyi de yeniden ürettiğinde ısrar ederek, yazarlar evrimsel terapinin hızlı ve ölümcül bir kanserde bile teorik olarak uygulanabilir olduğunu gösteriyor. Sonuçlar, dikkatle zamanlanmış tedavi molalarının, ilaç‑duyarlı hücreleri zararlı değil müttefik olarak kullanarak hastalığın kontrolünü uzatabileceğini düşündürüyor. Bu fikri uygulamaya dönüştürmek için daha fazla veri, tümör DNA’sını izleyen kan testleri gibi daha iyi belirteçler ve titiz klinik denemeler gerekecek. Yine de, sıradan okuyucuya iletilmesi gereken mesaj net: bazen kanserle mücadelede en akıllıca yol ona olabildiğince sert vurmak değil, evrimini yönlendirerek onu yönetilebilir, daha yavaş ilerleyen bir düşman halinde tutmaktır.
Atıf: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Anahtar kelimeler: evrimsel terapi, küçük hücre dışı akciğer kanseri, ilaç direnci, adaptif dozlama, matematiksel onkoloji