Clear Sky Science · tr
Konakçı m6A modifikasyonları, hücreye özgü ferroptozisi tetikleyen ve kronik solunum hastalıklarına neden olan bir yolak olarak mikrobiotayı şekillendirir
Microplarınızın Akciğerleriniz İçin Neden Önemi Var
Astım ve kronik obstrüktif akciğer hastalığı (KOAH) gibi kronik solunum problemleri genellikle sigara içme, kirlilik veya alerjilerle ilişkilendirilir. Bu çalışma, daha az belirgin bir aktörü öne sürüyor: bağırsaklarımızda ve derimizde yaşayan trilyonlarca mikrobu. Geniş ölçekli genetik veriler kullanılarak, yazarlar bazı mikropların sadece akciğer hastalıklarına eşlik etmekle kalmayıp, aynı zamanda ince kimyasal hücresel değişiklikler ve demir kaynaklı hücre hasarı biçimi aracılığıyla hastalığa neden olabileceğini gösteriyor. Bu gizli ağı anlamak, mikroplarımızı ve onların moleküler yolaklarını daha sağlıklı yönlere iterek kronik solunum hastalıklarını önleme veya tedavi etme konusunda yeni yollar geliştirmeye yol açabilir.
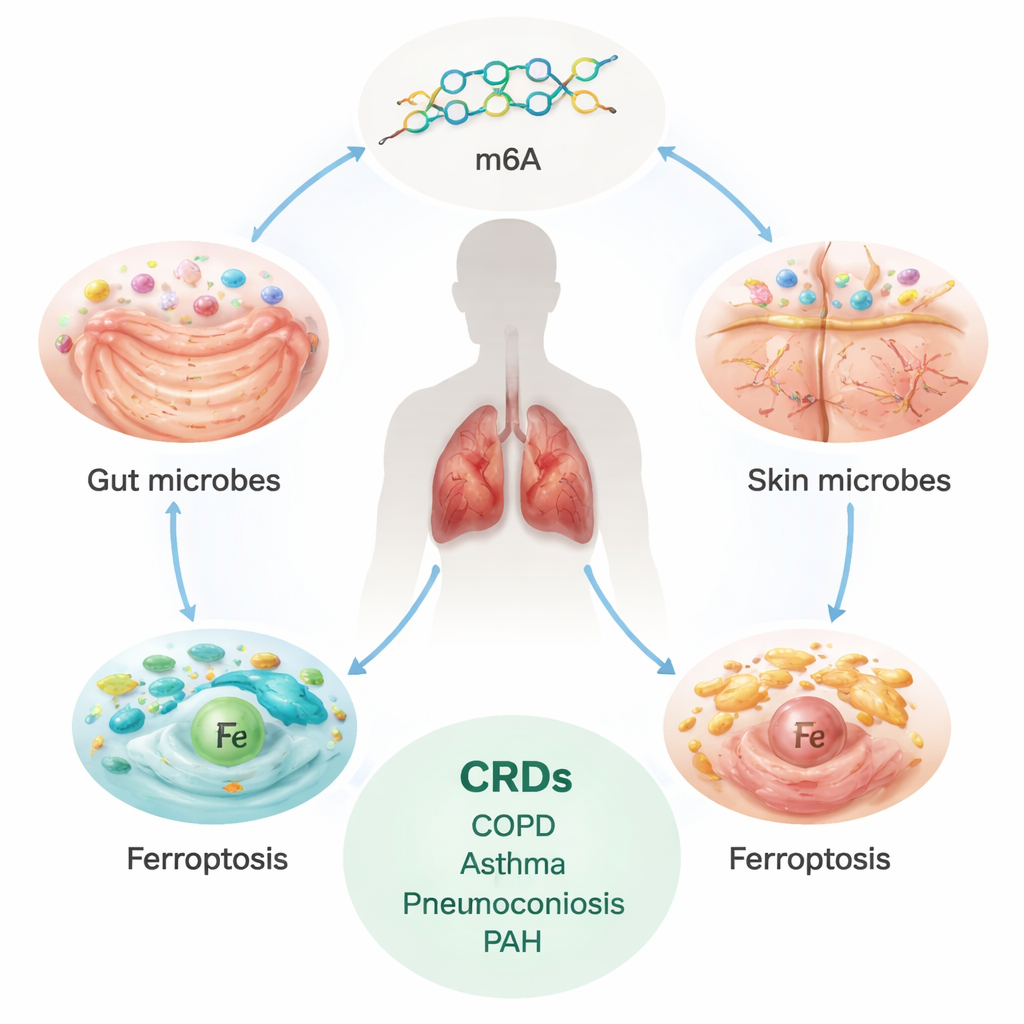
Kronik Akciğer Hastalığının Gizli Yükü
KOAH, astım, interstisyel akciğer hastalığı (İAH), pnömokonyoz ve pulmoner arteriyel hipertansiyon (PAH) dahil kronik solunum hastalıkları dünya genelinde yüz milyonlarca insanı etkiler ve her yıl milyonlarca ölüme yol açar. Bu durumlar genellikle yavaş ama kaçınılmaz bir şekilde ilerler, akciğerleri ve kan damarlarını skarlaştırır veya yeniden şekillendirir ve nefes darlığına neden olur. Mevcut tedaviler ağırlıklı olarak semptomları yönetir; altta yatan hasarı tamamen durdurmaz veya tersine çeviremez. Bu da bilim insanlarını, özellikle şiddetli hastalık ortaya çıkmadan önce değiştirilebilecek daha derin, kök düzeyde nedenleri aramaya yöneltti.
Bağırsak ve Derideki Mikrobiyal Komşular
Artık bağırsak ve derinin bağışıklık sistemini eğiten, metabolizmayı şekillendiren ve bariyer savunmalarını koruyan karmaşık mikrobiyal topluluklara ev sahipliği yaptığını biliyoruz. Peki bu mikroplar gerçekten akciğer hastalığını mı tetikliyor, yoksa insanlar hasta oldukça mı değişiyorlar? Nedeni etikten ayırt etmek için araştırmacılar Mendelyen randomizasyon adı verilen, insanların doğal genetik farklılıklarını bir tür yaşam boyu “deney” olarak kullanan bir yöntemi benimsediler. Yüzlerce bağırsak ve deri mikrop türüne ilişkin genetik verileri, büyük Avrupa çalışmaları tarafından sağlanan beş ana kronik akciğer hastalığı verisiyle birleştirerek, belirli mikropların daha yüksek veya daha düşük seviyelerine yatkınlığın her hastalık riskiyle ilişkili olup olmadığını test ettiler.
Akciğerleri Koruyan veya Zarar Veren Mikroplar
Analiz, her bir solunum hastalığı riskini artıran veya düşüren onlarca bağırsak mikrobu belirledi; bunlar sıklıkla hastalığa özgü örüntüler gösteriyordu. Örneğin bazı bağırsak bakterileri KOAH, astım veya PAH’a karşı koruyucu görünürken, diğerleri İAH veya KOAH riskini artırıyordu. Deri mikropları daha mütevazı ama hâlâ tespit edilebilir bağlantılar sergiledi; bazı türler farklı koşullar arasında daha yüksek riskle, bazıları ise daha düşük riskle ilişkilendirildi. Ekip analiz yönünü tersine çevirerek KOAH, astım ve diğer akciğer hastalıklarına genetik yatkınlığın da bağırsak ve deri mikrobiyotasında değişiklikleri öngördüğünü buldu. Bu çift yönlü trafik, bir geri besleme döngüsünü düşündürüyor: mikroplar akciğer hastalığını şekillendirebilir ve akciğer hastalığı mikroplarımızı yeniden biçimlendirebilir.
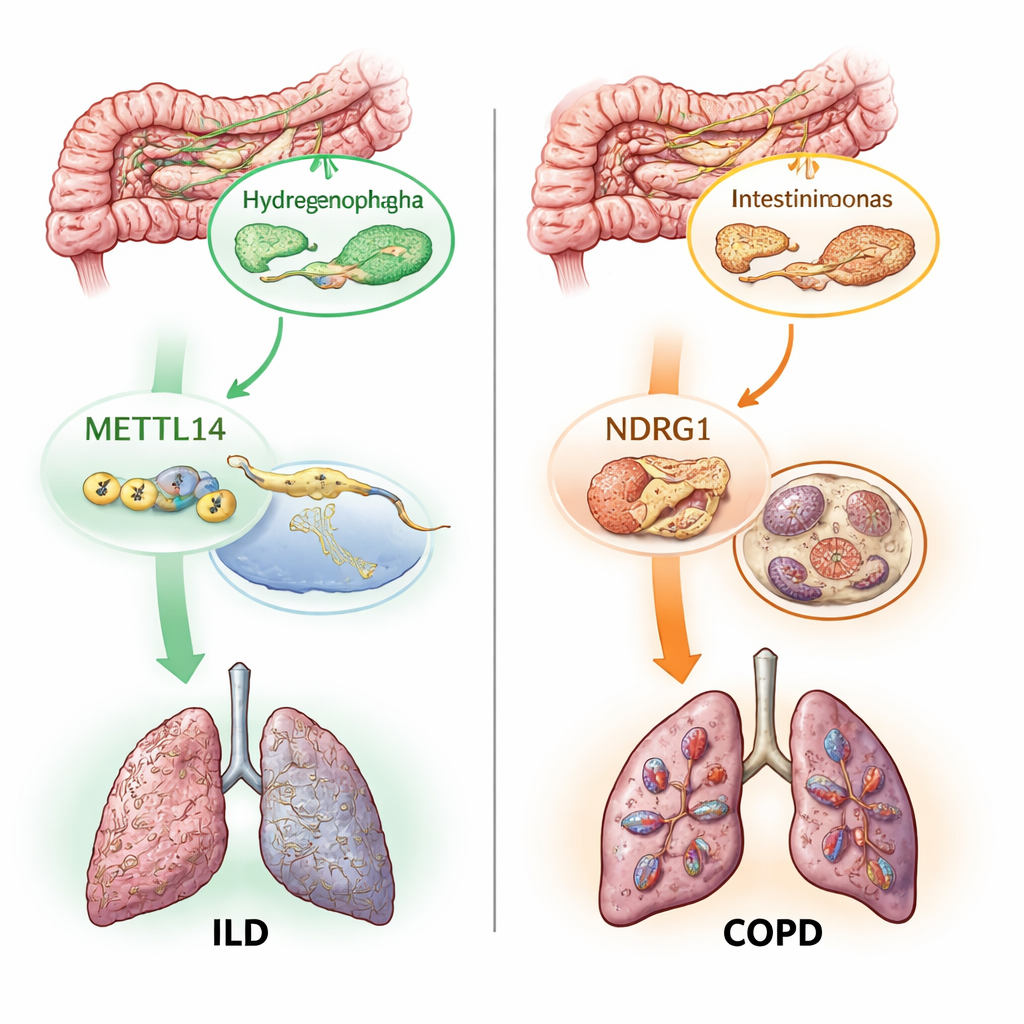
İki Moleküler Anahtar: RNA İşaretleri ve Demir Kaynaklı Hücre Ölümü
Hangi mikropların önemli olduğunu haritalamanın ötesinde, yazarlar bu mikroskobik ortakların akciğer dokularını nasıl etkileyebileceğini de sordular. Odaklandıkları iki moleküler süreç zaten akciğer hasarında kuşkulu görülüyordu. İlki, m6A modifikasyonu adı verilen, RNA’ya eklenen küçük bir kimyasal etikettir ve genlerin açılıp kapanmasını ayarlar. İkincisi, ferroptozis, hücre zarlarındaki yağların kontrolsüz oksidasyonuyla tetiklenen demire bağımlı bir hücre ölümü biçimidir. 19 m6A ilişkili gen ve yüzlerce ferroptozis ilişkili gen için genetik vekilleri kullanarak, bu yolaklardaki değişikliklerin akciğer hastalığıyla nedensel olarak ilişkili olup olmadığını test ettiler. METTL14 adlı bir m6A yazıcı geninin İAH riskini düşürmekle, NDRG1 dahil birkaç ferroptozis geninin ise KOAH, İAH ve astım riskini artırmakla ilişkili olduğunu buldular.
Noktaları Birleştirmek: Mikroplardan Hücrelere, Hücrelerden Hastalığa
Çalışmanın en yeni kısmı, bu parçaların nedensellik zincirlerine nasıl oturduğunu izlemekti. İstatistiksel aracılık analizleri, METTL14’ün İAH üzerindeki koruyucu etkisinin bir kısmının, onun belirli bir bağırsak mikrobu olan Hydrogenophagada indüklediği değişiklikler aracılığıyla gerçekleştiğini öne sürdü. Başka bir yolakta ise Intestinimonas massiliensis adlı spesifik bir bağırsak bakterisinin, NDRG1’i ve ferroptozis ölüm programını aktive ederek KOAH riskini kısmen etkilediği görüldü. Ekip daha sonra insan akciğer dokusu verilerini kontrol etti ve hem METTL14 hem de NDRG1’in hasta örneklerde sağlıklı örneklerden farklı biçimde ifade edildiğini doğruladı. Son olarak, bağışıklık hücrelerinin tek hücre genetik haritalarını kullanarak, NDRG1’in KOAH üzerindeki zararlı etkisini monosit tipi bir bağışıklık hücresi alt grubuna özgü olarak belirlediler; bu da gelecekte bu geni hedefleyen ilaçların hücreye özgü etki göstermesi gerekebileceğini düşündürüyor.
Gelecekteki Tedaviler İçin Anlamı
Uzman olmayanlar için ana mesaj, akciğer sağlığının sadece soluduğumuz şeyle ilgili olmadığı; aynı zamanda içinde ve üzerinde yaşayan mikroplarımız ve bunların hücrelerimizde çevirdiği moleküler anahtarlarla da ilgili olduğudur. Bu çalışma her adımı deneysel olarak kanıtlayamaz ve ağırlıklı olarak Avrupa kökenli insanlarla sınırlıdır, ancak bağırsak mikropları, m6A gibi RNA işaretleri ve demir kaynaklı hücre ölümü arasındaki bağlantının kronik akciğer hasarına götüren bağlantılı bir yol oluşturduğuna dair güçlü genetik ipuçları sunar. Uzun vadede, bu araştırma hattı, mikrobiyom tabanlı terapileri METTL14, NDRG1 veya ferroptozisi hedefleyen ilaçlarla birleştiren yeni stratejiler ilham verebilir; amaç sadece semptomları hafifletmek değil, kronik solunum hastalıklarının ilerlemesine neden olan biyolojik devreleri kesintiye uğratmaktır.
Atıf: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Anahtar kelimeler: bağırsak mikrobiomu, kronik akciğer hastalığı, astım ve KOAH, RNA epigenetiği, hücre ölüm yolları