Clear Sky Science · tr
NEK7’nin kortaktin fosforilasyonu, EML4-ALK V3 eksprese eden hücrelerin göç kapasitesini düzenliyor
Akciğer kanserinde hücre hareketinin önemi
Kanser, hücreler hareket etmeyi öğrendiğinde yaşamı tehdit eden bir hâl alır. Küçük hücre dışı akciğer kanserinde bazı tümörler vücudun diğer bölgelerine diğerlerinden daha hızlı yayılır; bunun sorumlularından biri EML4-ALK adlı hatalı bir füzyon proteinidir. Varyant 3 (V3) olarak bilinen belirli bir form özellikle agresif hastalık ve hedefe yönelik ilaçlara kötü yanıtlarla ilişkilidir. Bu çalışma temel ama hayati bir soruyu soruyor: V3 kaynaklı kanser hücrelerinin şekil değiştirip bu kadar verimli hareket etmesini sağlayan nedir ve bunu mümkün kılan moleküler bileşenleri belirleyebilir miyiz?
Aşırı göç eğilimli bir akciğer kanseri varyantı
Doktorlar uzun zamandır yalnızca bir azınlık akciğer kanserinin EML4-ALK füzyonunu taşıdığını biliyordu, ancak tümörleri V3 formunu ifade eden hastalar diğer varyantlara kıyasla genellikle daha kötü seyir gösterir. Mikroskop altında V3-eksprese eden hücreler farklı görünür: sıkı ve döşeme taşı şeklinde olmak yerine uzanmış, ince formlara dönüşür ve uzun çıkıntılar oluşturur; hareket hâlindeki hücrelere benzerler. Önceki çalışmalar bu davranışın NEK9 ve NEK7 adlı iki enzime bağlı olduğunu, bunların hücrelerde moleküler birer anahtar gibi davrandığını göstermişti. Ancak bu anahtarların kritik aşağı akış hedefleri—hücrenin iç iskeletini doğrudan yeniden şekillendiren bileşenler—iyi anlaşılmamıştı.
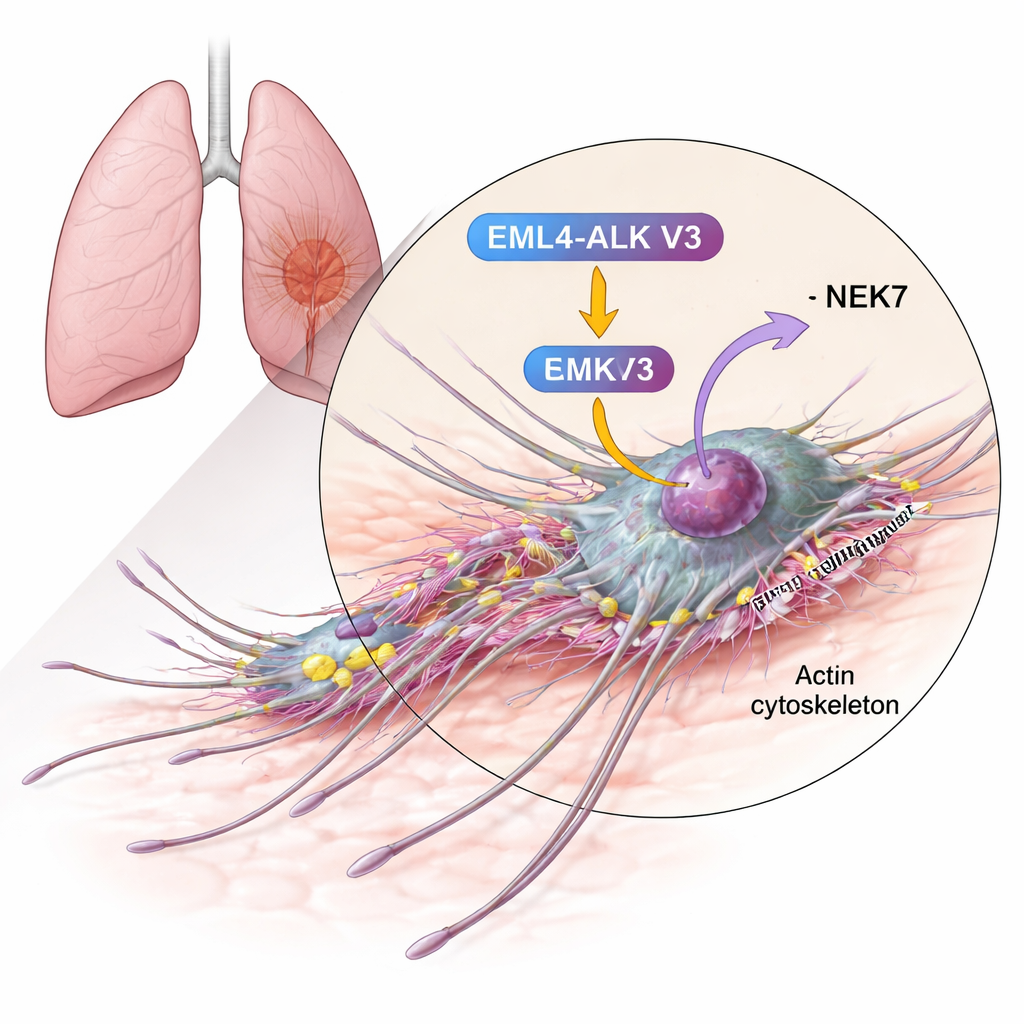
Bir hareket proteini ile agresif bir füzyonu bağlamak
Yazarlar, birçok invazif kanserde bol bulunan ve hücre zarını öne iten aktin filament ağlarını kurmaya yardımcı olduğu bilinen kortaktine odaklandı. Biyokimyasal testler kullanarak kortaktinin NEK6 tarafından ve özellikle NEK7 tarafından kimyasal olarak modifiye edilebileceğini (fosforilasyon) gösterdiler. Bu enzimler, kortaktinin aktine bağlanan bölgesindeki spesifik serin kalıntılarına fosfat grupları ekliyor—tam da aktin liflerini kavrayan ve dallanmış ağları stabilize eden kısım. NEK7 bulunduğunda kortaktin, NEK6’ya kıyasla daha fazla fosfat grupla ve daha fazla yerde süsleniyordu; bu da bu bağlamda NEK7’nin birincil düzenleyici olduğunu düşündürüyor.
Kortaktini kapatmak kanser hücresi göçünü durduruyor
Kortaktinin canlı hücrelerde gerçekte ne yaptığını görmek için araştırmacılar, NEK9 veya NEK7’yi aktive edecek ya da EML4-ALK V3’ü eksprese edecek şekilde tasarlanmış hücrelerde RNA interferansı ile kortaktini azalttılar. Üç durumda da belirgin uzun, mezenkimal benzeri şekiller çöktü: hücreler daha düz ve yuvarlak hale geldi, uzun çıkıntılarını kaybetti ve bunun yerine hücre içine çapraz şekilde geçen kalın, düz aktin “stres fibrilleri” oluştu. Yapay “yaraların” kapanmasından tek hücre takibine ve kimyasal bir sinyale doğru hareket ölçümlerine kadar bir dizi göç deneyinde kortaktin olmadan bu yüksek hareketli hücrelerin hızla yavaşladığı görüldü. Benzer etkiler doğal olarak EML4-ALK V3 taşıyan yerleşik akciğer kanseri hücre hatlarında da gözlendi; bu da yolun klinik önemini vurguluyor.
Ön kenarda ince filamentler ve keskin uçlar
Bronşiyal epitel hücrelerinde yüksek çözünürlüklü görüntüleme daha ayrıntılı bir tablo ortaya koydu. EML4-ALK V3-eksprese eden hücreler, çıkıntılarını süsleyen birçok ince, bazen dallanmış filopodiya-benzeri uzantılar üretti. Bu yapıların uçlarında ve dallanma noktalarında kortaktin, EML4-ALK V3, NEK7 ve fosforile kortaktinin bir formu birlikte birikti. Bu sıkı birlikte lokalizasyon, NEK7’nin kortaktini modifiye ederek hücreyi yönlendirmeye yardımcı olan hassas, dallanmış aktin ağlarını inşa edip koruyan odaklanmış bir “inşaat sahası” olduğunu düşündürüyor. Kortaktin kaldırıldığında bu ince uzantılar kayboldu ve 3B tümör benzeri kürelerden çevreleyen jele doğru invazyon belirgin şekilde azaldı.
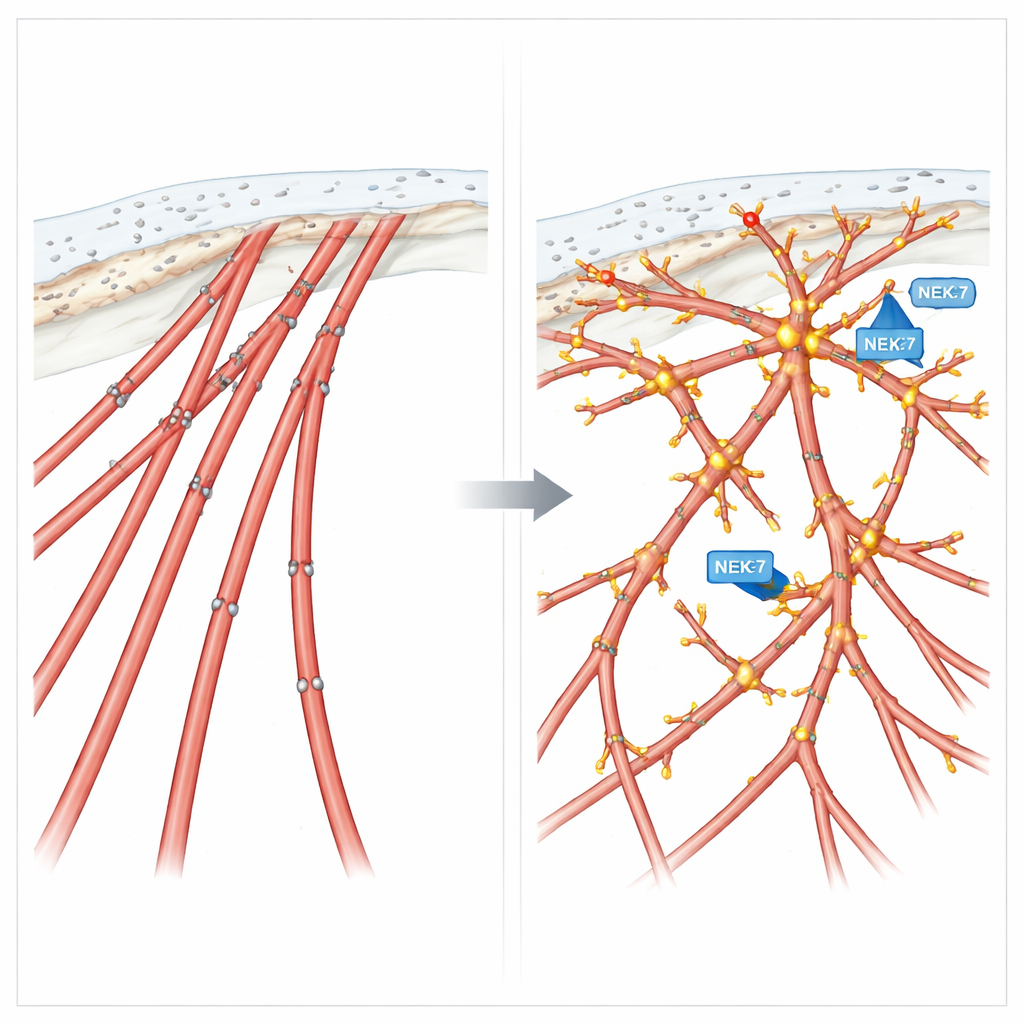
Fosforilasyon bir göç ayarı gibi
Kortaktin üzerindeki bu kimyasal işaretlerin davranışı nasıl etkilediğini sınamak için ekip, proteinin iki tasarım versiyonunu oluşturdu: dört kilit yerde sürekli fosforilasyonu taklit eden bir fosfo-mimetik form ve o bölgelerde fosforilasyon olamayan bir fosfo-null form. Mimetik versiyonu eksprese eden hücreler bol miktarda filopodiya-benzeri uzantılar geliştirdi ve NEK7 veya EML4-ALK V3 aktif olan hücrelere benzer şekilde yönlendirilmiş göçte artış gösterdi. Buna karşılık, fosforlanamaz versiyonu eksprese eden hücreler sert stres fibrilleri oluşturdu, o ince uzantıları kaybetti ve hızlı fakat hedefsiz bir şekilde hareket etti—dolaşmada iyi, bir sinyali izlemekte kötü. Üç boyutlu kültürlerde bu fosfo-null kortaktin, düzenli rehberlikten uzak dağınık invaziv büyümelere yol açtı.
Bu, yayılmayı anlamak—ve hedeflemek—için ne anlama geliyor
Kısacası çalışma, agresif EML4-ALK V3 akciğer kanseri varyantının normal bir hücre-şekillendirme sistemini ele geçirdiğini gösteriyor. NEK7’yi aktive ederek kortaktinin aktine bağlanan bölgesinde spesifik yerlere fosforilasyon eklenmesine neden oluyor. Bu modifikasyon kortaktini, ince dallanmış aktin yapıları ve filopodiya-benzeri uzantılar inşa edip sürdürebilecek şekilde ayarlıyor; bunlar hızlı, yönlendirilmiş hücre göçü ve invazyonu destekliyor. Kortaktin veya onun fosforilasyonu bozulduğunda sistem tersine dönüyor: hücreler ya neredeyse hiç hareket etmiyor ya da yönsüz, kaotik bir şekilde hareket ediyor. Bu bulgular kanserle ilişkili bir füzyondan NEK7 aracılığıyla kortaktin ve aktin sitoskeletine uzanan somut bir moleküler zinciri ortaya koyuyor; bu da bazı akciğer kanserlerinin neden bu kadar etkili şekilde metastaz yaptığını açıklamaya yardımcı oluyor ve hareketlerini yavaşlatmak veya yanlış yönlendirmek için yeni yollar gösteriyor.
Atıf: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, EML4-ALK V3, hücre göçü, kortaktin, aktin sitoskeleti