Clear Sky Science · tr
ATF4 mitokondriyal disfonksiyonu ve mitofajiyi düzenler, korneal endotel apoptozuna katkıda bulunur
Gözün penceresi neden bulutlanabilir
Kornea—gözün saydam ön penceresi—iç yüzeyindeki ince, çok çalışan hücre tabakası sayesinde şeffaf kalır. Fuchs endotel korneal distrofisi (FECD) durumunda milyonlarca insan bu hücreleri yavaşça kaybeder; bunun sonucu olarak ödem, bulanık görme ve sıklıkla kornea nakilleri ortaya çıkar. Bu çalışma temel ama hayati bir soruyu soruyor: bu hücreleri ölmeye hangi etkenler yönlendiriyor ve tek bir moleküler “anahtarı” kapatmak onları kurtarabilir mi?
Görmeyi koruyan kırılgan bir hücre tabakası
Korneal endotel, korneanın şeffaf kalması için sürekli olarak sıvıyı dışarı pompalayan tek sıra altıgen hücrelerden oluşur. FECD’de bu hücreler strese girer ve zamanla kaybolur; aynı zamanda alttaki membranda gutta adı verilen anormal madde çıkıntıları birikir. FECD için onaylanmış ilaçlar yok ve kornea nakli ana tedavi olduğundan araştırmacılar, hücre içi stresin bu hücreleri nasıl ölüme doğru ittiğini tam olarak anlamaya çalışıyor. Önceki çalışmalar hücrenin iki önemli bölümünde—endoplazmik retikulum (hücrenin protein katlama fabrikası) ve mitokondriler (hücrenin enerji merkezleri)—meydana gelen gerilimlere ayrı ayrı işaret etmişti, ancak bu iki stres tepkisinin birbirleriyle nasıl iletişim kurduğu belirsizdi.
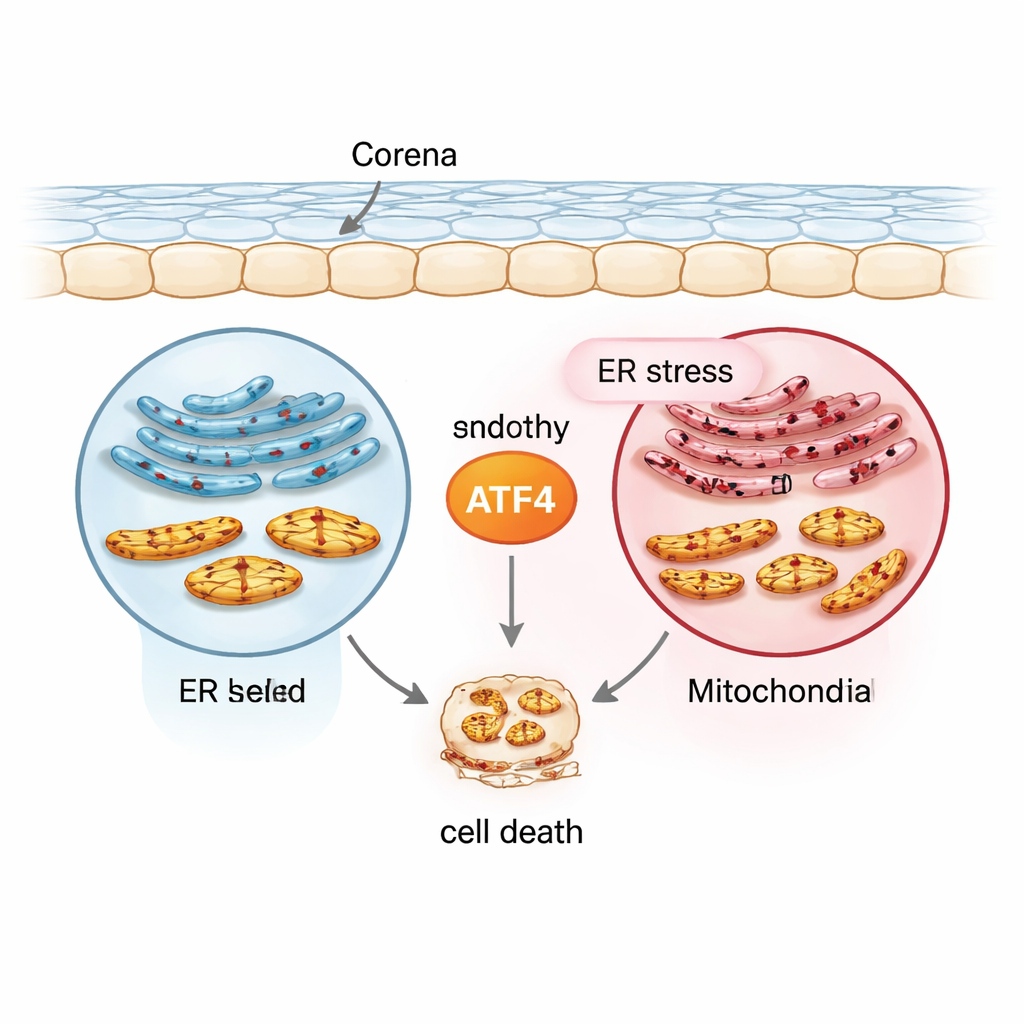
Merkezdeki stres haberci: ATF4
Ekip, birçok stres yanıtı genini açıp kapatan bir transkripsiyon faktörü olan ATF4 adlı proteine odaklandı. Normal insan korneal endotel hücre hattı (21T), hastalıkla ilişkili TCF4 tekrar genişlemesi taşıyan FECD-benzeri hücre hattı (F35T), primer insan korneal endotel hücreleri ve ultraviyole A (UVA) ışığına maruz bırakılan fare modelleri kullanarak kronik stresi taklit eden bir dizi koşul yarattılar. Tunikamisin adlı bir ilaçla endoplazmik retikulum stresini tetiklediler ve ardından ATF4 ile diğer belirteçleri ölçtüler. Normal hücrelerle karşılaştırıldığında, FECD-benzeri hücreler başlangıçta daha yüksek ATF4 ve ilişkili stres proteinleri düzeyine sahipti ve kronik stres altında hem kültürdeki hücrelerde hem de insan kornea dokularında ATF4 daha da yükseldi. Bu desen ATF4’ü erken koruyucu yanıtlarla sonraki, kendini yok edici sinyaller arasında bir kavşakta konumlandırdı.
Güç kaybından programlanmış ölüme
Ardından araştırmacılar bu stresin mitokondrileri nasıl etkilediğine baktı. FECD-benzeri hücrelerde mitokondriler daha az ATP üretti, elektrik membran potansiyelini kaybetti ve uzun, ağ benzeri şekillerden koparak birçok küçük parçaya ayrıldı. Bu değişiklikler endoplazmik retikulum stresi uzadıkça kötüleşti. Aynı zamanda aktive olmuş kaspazlar ve parçalanmış, ölüm yanlısı formdaki DNA onarım proteini PARP gibi klasik hücre ölümü proteinleri artarken; Bcl-2 gibi koruyucu proteinler azaldı. Birlikte bu değişiklikler, FECD’de stres altındaki korneal endotel hücrelerinin mitokondri kaynaklı apoptoza—düzgün ama geri döndürülemez bir programlı hücre intiharına—itildiğini gösteriyor.
Kronik stres altında temizlik sistemi tıkanıyor
Normalde ağır hasarlı mitokondriler, etiketlenip bertaraf için küçük keseciklere sarıldıkları bir geri dönüşüm süreci olan mitofajiyle uzaklaştırılır. Ekip, erken mitofaji “başlatıcı” moleküllerinin (Parkin ve LC3) hem normal hem FECD‑benzeri hücrelerde, özellikle stres sonrası, açıldığını buldu. Ancak destekleyici kilit proteinler azalmıştı ve elektron mikroskobu, veziküllerde sıkışmış kısmen sindirilmiş mitokondrilerin birikimini gösterdi. Bu, temizlik sürecinin başlatıldığını ama tamamlanamadığını; hücrelerin, iyileşme yerine daha fazla stres ve ölüme yol açan kusurlu güç santralleriyle dolduğunu düşündürdü.
ATF4’ü kapatarak hücreleri kurtarmak
ATF4’ün bu kısır döngüyü sürdürüp sürdürmediğini test etmek için araştırmacılar kültürdeki korneal endotel hücrelerinde ATF4’ü kısmen susturmak üzere küçük girişimli RNA kullandılar. Aynı kronik stres koşulları altında, ATF4 düzeyi azaltılmış hücreler daha düşük ölüm‑tetikleyici protein düzeyleri, daha sağlıklı mitokondri membran potansiyeli, daha az parçalanma ve canlılık testlerinde daha iyi hayatta kalma gösterdi. Önemli olarak, tıkanmış mitofaji yapılarının sayısı azaldı; bu da ATF4’ü düşürmenin hasar ve temizlik arasındaki daha etkili bir dengeyi yeniden kurmaya yardımcı olduğunu düşündürdü. ATF4 geninin yalnızca tek bir işleyen kopyasına sahip olacak şekilde mühendislik yapılmış farelerde, UVA maruziyeti pro‑ölüm ortak proteini CHOP’un daha az aktivasyonuna yol açtı ve tam ATF4‑yeterli farelerle karşılaştırıldığında daha normal şekilli endotel hücreleri korundu.
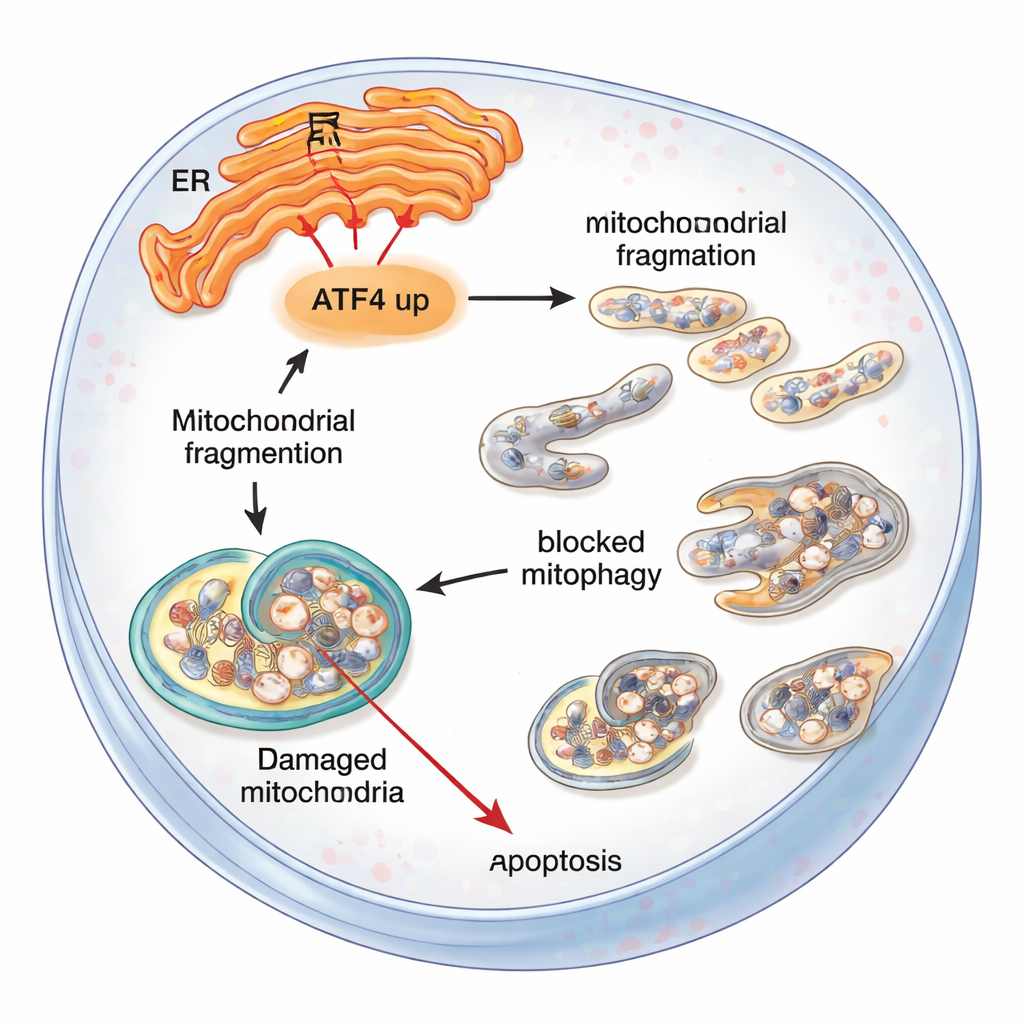
FECD’li kişiler için bunun anlamı
Uzman olmayanlar için çıkarım şudur: ATF4 adlı bir stres habercisi, korneal endotel hücrelerini başa çıkmaktan çökmeye sürekleyebilir. Endoplazmik retikulum stresi uzun süreliyse ATF4 mitokondrileri bozuyor, hücrenin temizlik mekanizmasını tıkıyor ve nihayetinde bu hayati hücrelerin kendi kendini yok etmesini teşvik ediyor. ATF4’ü düşürmek—farelerde genetik olarak veya hücrelerde hedefe yönelik moleküler araçlarla—mitokondrileri koruyor, atık temizliği iyileştiriyor ve daha fazla hücrenin hayatta kalmasını sağlıyor. Bu çalışma hâlâ laboratuvar ve hayvan aşamasında olsa da, ATF4 ve ilişkili stres yollarını, bir gün Fuchs distrofisinin ilerlemesini yavaşlatabilecek veya önleyebilecek ve kornea nakli gereksinimini azaltabilecek umut verici ilaç hedefleri olarak öne çıkarıyor.
Atıf: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Anahtar kelimeler: Fuchs endotel korneal distrofisi, korneal endotel, mitokondriyal stres, mitofaji, ATF4