Clear Sky Science · tr
QAL333’ün antitumör aktivitesi ve öngörüsel modelleme: bütünleşik transkriptomik-biyoenformatik analiz seçici sitotoksisite ve duyarlılık belirleyicilerini ortaya koyuyor
Bu yeni ilaç adayının önemi
Kanser ilaçları bazen bazı hastalarda iyi sonuç verirken diğerlerinde başarısız olur; bunun büyük kısmı tümörlerin iç devrelerinin farklı olmasından kaynaklanır. Bu çalışma, belirli kolorektal kanser türlerine diğerlerine kıyasla çok daha güçlü etki eden, birçok normal hücreyi ise göreli olarak koruyan yeni tasarlanmış bir bileşik olan QAL333’ü tanıtıyor. Aynı derecede önemli olarak, araştırmacılar tümör hücrelerindeki gen aktivite desenlerinin kimin daha çok fayda göreceğini tahmin etmeye yardımcı olabileceğini gösteriyor; bu da daha hassas, kişiselleştirilmiş tedavi stratejilerine işaret ediyor.
Belirli tümör tiplerine odaklı saldırı
Ekip, kanser hücrelerini hasara uğrattığı bilinen bir bileşik ailesiyle ilişkili sentetik bir molekül olan QAL333’ü, 15 insan kanser hücre hattı ve üç kanser olmayan hattı kapsayan geniş bir panelde test ederek başladı. Kolorektal kanser hücrelerinin, özellikle SW620 adlı hattın, nispeten düşük dozlarda ilaca karşı son derece duyarlı olduğu görüldü. Buna karşılık, üçlü negatif meme kanseri hücreleri çok daha dirençliydi ve güvenli şekilde ulaşılması zor on kattan fazla daha yüksek dozlar gerektiriyordu. İlginç bir şekilde, tüm kanser olmayan hücreler aynı şekilde tepki vermedi: bazıları duyarlı iken yaygın kullanılan bir böbrek hücre hattı gibi diğerleri şaşırtıcı derecede dirençliydi. Bu desen, QAL333’ün etkilerinin hücrenin “kanser” veya “normal” olarak etiketlenmesinden çok hücrenin iç biyolojisine bağlı olduğunu gösterdi.
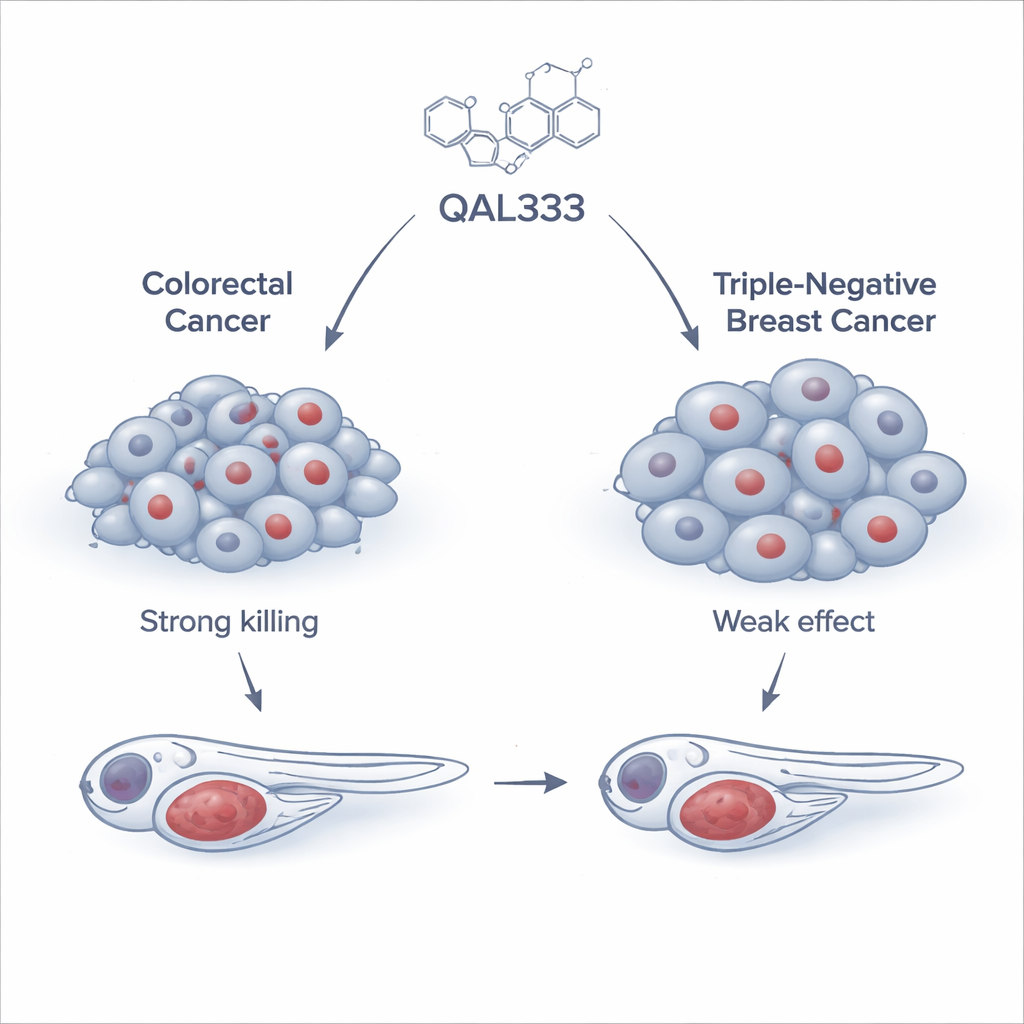
İlacı canlı organizmalarda test etmek
Hücre kültürü sonuçlarının canlı bir organizmada da geçerli olup olmayacağını görmek için araştırmacılar insan hastalığını modellemede yaygın olarak kullanılan küçük saydam bir balık olan zebrada balığına yöneldi. Floresanla işaretlenmiş insan kanser hücrelerini zebrada embriyolarına naklettiler ve QAL333 ile tedavi ettiler. Kolorektal kanser hücreleri taşıyan balıklarda ilaç tümör büyümesini açıkça yavaşlattı ve klinikte kullanılan standart bir kemoterapi kombinasyonunun etkisine yaklaştı. Buna karşılık, üçlü negatif meme kanserinden kaynaklanan tümörler neredeyse yanıt vermedi; oysa aynı modelde yaygın bir meme kanseri ilacı olan paklitaksel iyi çalıştı. Bu in vivo testler, QAL333’ün gücünün tüm kanserlerde değil belirli bir tümör alt kümesinde olduğunu pekiştirdi.
QAL333’ün hücre içinde nasıl çalıştığına bakmak
Bazı hücrelerin neden öldüğünü, bazılarının neden dirençli kaldığını anlamak için bilim insanları QAL333 tedavisinden sonra binlerce genin aktivite seviyelerinin nasıl değiştiğini ölçtü. Duyarlı kolorektal kanser hücrelerinde hücre bölünmesini ve büyümeyi yöneten kilit genler baskılanmış ve ana yaşamı sürdürme yolları zayıflatılmıştı. Oksidatif stresle ve klasik programlı hücre ölümünden farklı bir hücre ölümü formuyla ilişkili sinyaller de değişmişti; bu, QAL333’ün bu hücrelerin içinde hasarı yöneten zaten kırılgan sistemleri aşırı yüklediğini düşündürüyor. Buna karşılık dirençli meme kanseri hücreleri, hücrelerin zararlı koşullarla başa çıkmasına yardımcı olduğu bilinen NF-κB gibi faktörler tarafından kontrol edilen stres ve inflamasyon programlarını etkinleştirdi. Bu yan yana karşılaştırma, QAL333’ün bazı hücrelerde zayıf savunmaları boğarken diğerlerinin etkili bir karşı yanıt oluşturduğunu gösteren bir tablo çizdi.
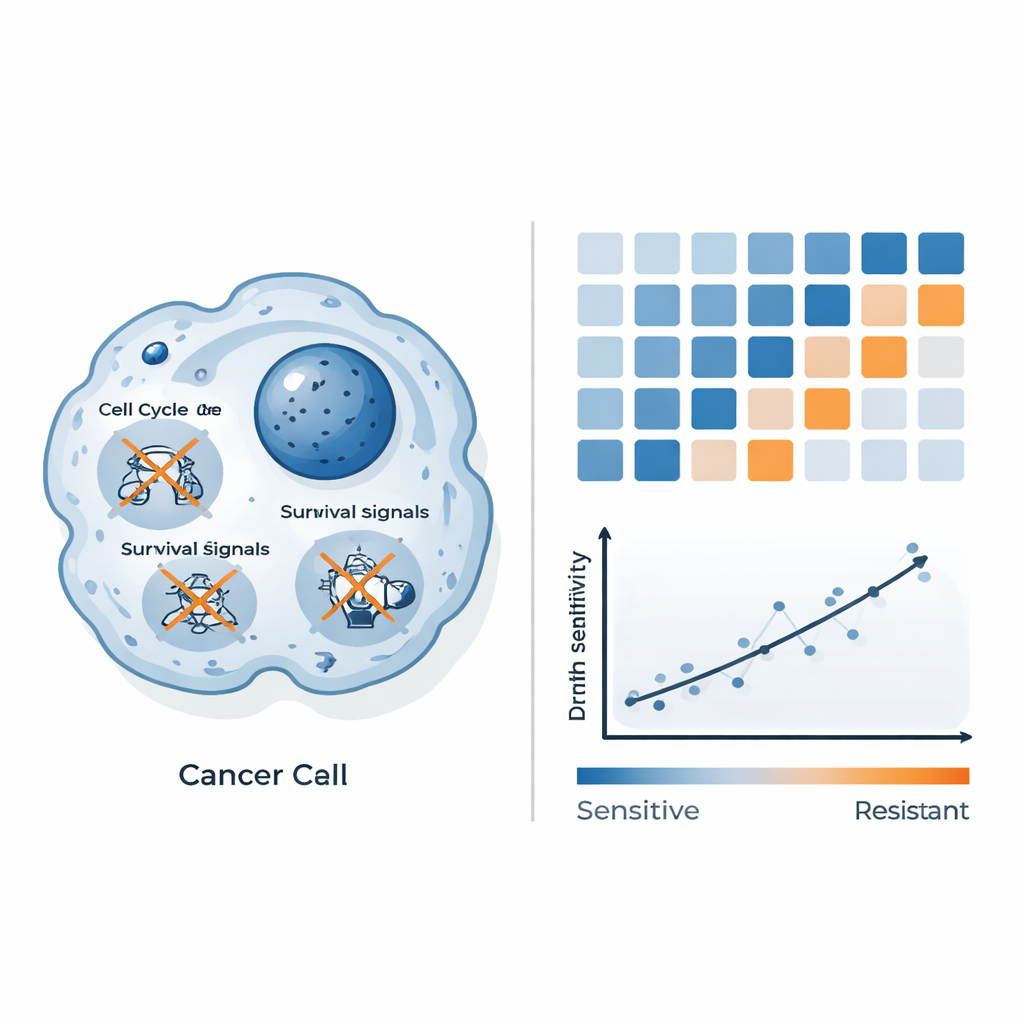
Kimlerin yanıt vereceğini tahmin etmek için gen desenlerini kullanmak
Gen değişikliklerini kataloglamanın ötesinde, araştırmacılar bu desenlerin pratik bir tahmin aracına dönüştürülüp dönüştürülemeyeceğini sordular. Hücre hattı panelinden elde edilen başlangıç gen aktivite verilerini ölçülen ilaç duyarlılığı ile birleştirip en bilgilendirici sinyalleri aramak için makine öğrenmesi kullandılar. Tek bir gene güvenmek yerine genleri biyolojik yollara göre gruplayıp üç sistemden oluşturulan birleşik bir “yol skoru” yarattılar: hücrelerin enerji ve kimyasalları nasıl işlediği (metabolik yollar), çevrelerini nasıl organize ettikleri (kanserle ilişkili proteoglikanlar ve ilgili yapılar) ve iç iskeletlerinin nasıl düzenlendiği. Bu bileşik skor, her hücre hattını öldürmek için gereken QAL333 miktarıyla güçlü bir ilişki gösterdi: düşük skorlar yüksek duyarlılıkla, yüksek skorlar ise dirençle eşleşti. Başka bir deyişle, bu ağların tümör içinde nasıl ayarlı olduğuna bağlı olarak QAL333’ün ne kadar etkili olacağı öngörülebilir.
Daha geniş biyolojik etkilere dair beklenmedik ipuçları
Ana odak kanser olsa da QAL333 ayrıca bakterilerin biyofilm oluşturma gibi davranışları koordine etmek için kullandığı iletişim sistemi olan “quorum sensing”i bozma yeteneği de gösterdi. Çok düşük dozlarda bile bileşik, bir diş eti hastalığı bakterisinin biyofilm oluşumunu azalttı ve bağışıklık hücrelerindeki belirli inflamasyon sinyallerini baskıladı. Yazarlar bu bulguları erken ve keşif amaçlı olarak değerlendiriyor, ancak QAL333 veya ilişkili moleküllerin bir gün bakteriyel toplulukların yok edilmesinin zor olduğu enfeksiyonlar gibi kanser dışı durumlarda da kullanım potansiyeli olabileceğini öne sürüyor.
Gelecekteki hastalar için anlamı
Genel olarak çalışma, hassas kolorektal tümörleri hedef alırken birçok diğer hücre tipini koruyan seçici bir ilaç adayı olarak QAL333’ü konumlandırıyor ve hangi tümörlerin yanıt verme olasılığının yüksek olduğunu tahmin etmeye yönelik bir yol haritası sunuyor. Daha gelişmiş hayvan modellerinde ve nihayetinde hastalarda doğrulanırsa, basit bir gen ekspresyon testi doktorların QAL333’ün ne zaman uygun olduğunu belirlemesine yardımcı olabilir; bu da kanser tedavisini her tümörün devre düzenine göre uyarlama hedefine hizmet eder. Aynı zamanda çalışma, umut vadeden ilaçların da sınırlara sahip olduğunu vurguluyor: meme kanserleri ve diğer dirençli tümörler akıllı kombinasyonlar veya tamamen farklı stratejiler gerektirebilir.
Atıf: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Anahtar kelimeler: kolorektal kanser, hedefe yönelik tedavi, gen ekspresyonu, ilaç duyarlılığı modelleme, zebrada balığı ksenograftı