Clear Sky Science · tr
İn‑silico QSAR modellemeden in‑vitro MTT assayına: üçlü negatif meme kanseri (TNBC) ve deri kanseri için yeni uPAR adaylarının deneysel doğrulanması
Bu araştırma neden önemli
Üçlü negatif meme kanseri ve bazı deri kanserleri gibi kanser türleri hızla yayıldıkları ve sıklıkla standart tedavilere direnç gösterdikleri için tedavisi özellikle zordur. Bu çalışma, kanser hücresi yüzeyinde yer alan ve uPAR adı verilen umut verici yeni bir hedefi araştırıyor ve bilgisayar tabanlı ilaç tasarımı ile laboratuvar deneylerini birleştirmenin, bu agresif tümörlerin yayılmasını yavaşlatabilecek veya durdurabilecek yeni ilaç adaylarını ortaya çıkarabileceğini gösteriyor.
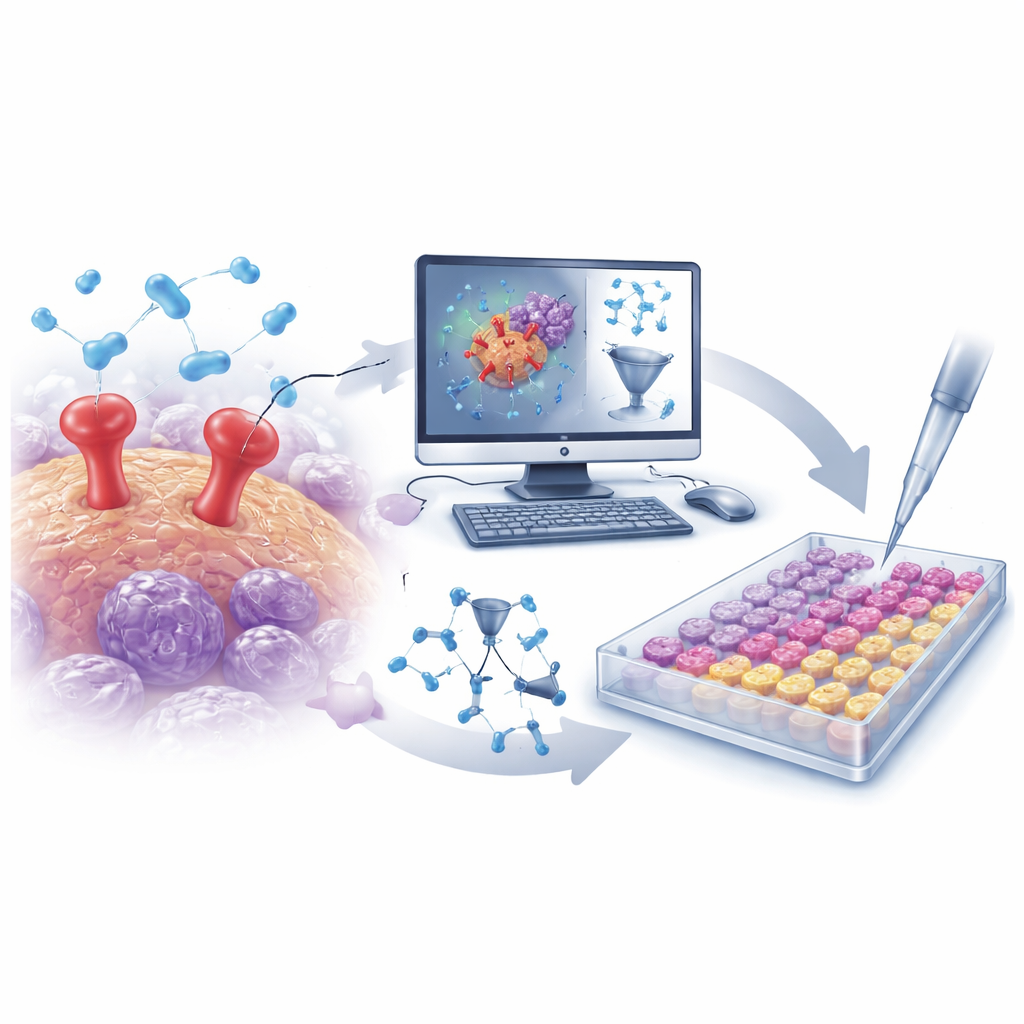
Kanserin yayılmasına yardımcı olan bir kapı
Bir tümörün ölümcül hale gelmesi için hücrelerin orijinal yerlerinden kopup çevre dokuyu aşındırmaları, kana girmeleri ve uzak organları kolonize etmeleri gerekir. uPAR bu süreçte kilit bir yardımcıdır. Kanser hücresi yüzeyinde bulunur ve eşlik eden proteinlerle birlikte çevredeki destek yapılarını çözen enzimleri aktive ederek hücrelerin hareket etmesini ve invazyonunu kolaylaştırır. uPAR, özellikle üçlü negatif meme kanseri hücrelerinde ve bazı deri kanseri hücrelerinde yüksek düzeyde bulunur; bolluğu daha hızlı büyüme, daha yüksek invazivite ve daha kötü hasta sonuçları ile ilişkilidir. Bu nedenle uPAR, çekici fakat bugüne kadar yeterince kullanılmamış bir anti‑kanser ilaç hedefidir.
Büyük kimyasal veriyi akıllı algoritmalarla değerlendirmek
Araştırmacılar, halka açık bir veritabanından 500’den fazla bilinen uPAR engelleyici molekülü bir araya getirerek işe başladı. Her bir molekülün yapısı, boyut, şekil, yük dağılımı ve esneklik gibi özellikleri yakalayan binlerce sayısal tanımlayıcıya dönüştürüldü. Bu veriler kullanılarak, bir nicel yapı‑aktivite ilişkisi (QSAR) modeli oluşturuldu—bir molekülün hangi yapısal özelliklerinin onu daha güçlü bir uPAR inhibitörü yaptığına dair öğrenen matematiksel bir araç. Aşırı uyumu önlemek için titiz doğrulamanın ardından model, görülmemiş bileşikler üzerinde yüksek öngörü gücü gösterdi ve uPAR blokajını güçlendiren veya zayıflatan birkaç temel özelliği öne çıkardı. Bu bulgular yeni ve daha iyi tasarlanmış moleküller arayışına rehberlik etti.
Sanal taramalardan gerçek deney tüplerine
Eğitilmiş QSAR modeliyle ekip, yaklaşık 30.000 proteaz hedefli molekülden oluşan odaklı bir kütüphaneyi sanal olarak taradı. Model, bu geniş havuzu hızla olası uPAR inhibitörleri olan küçük bir gruba daralttı. Paralel olarak, bilgisayar tabanlı doklama simülasyonları her adayın uPAR bağlanma bölgesine ne kadar iyi oturabileceğini değerlendirmek için kullanıldı ve moleküler dinamik simülasyonlar bu doklanmış komplekslerin zaman içinde kararlı kalıp kalmayacağını test etti. Bu birleşik in‑silico kampanyadan iki öne çıkan molekül ortaya çıktı: QSAR modeli tarafından yüksek potansiyele sahip olarak işaretlenen D685‑0061 ve doklama ile simülasyonlarda uPAR ile özellikle kararlı etkileşimler kurduğu vurgulanan C878‑1660.
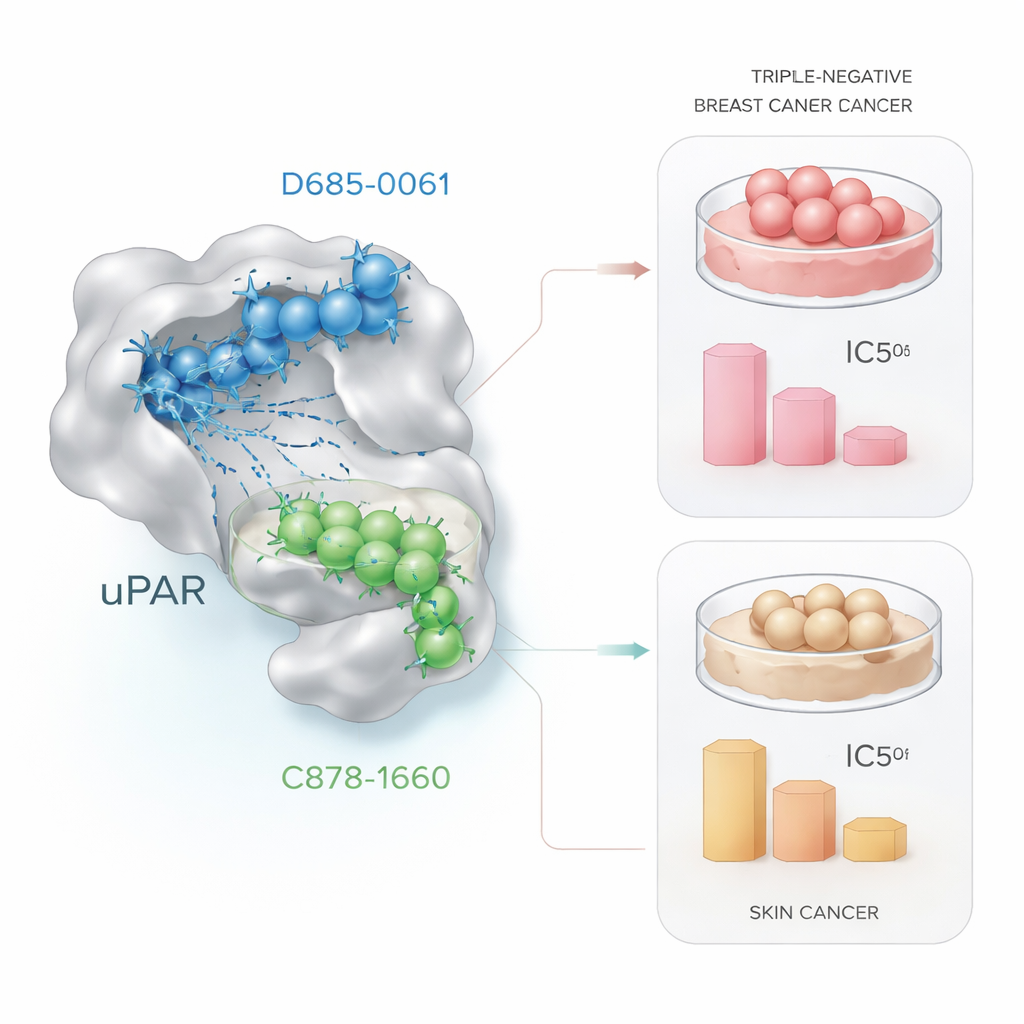
Adayları kanser hücrelerinde teste sokmak
Bilgisayar vaatleri, gerçek biyolojik etkilere dönüşmediği sürece anlamlı değildir. Bunu test etmek için araştırmacılar, iki lider moleküle canlı kanser hücrelerini artan dozlarda maruz bıraktı ve hücre canlılığını standart bir laboratuvar yöntemi olan MTT testi ile ölçtüler. Üçlü negatif meme kanseri hücrelerinde (MDA‑MB‑231), D685‑0061 hücreleri daha etkin şekilde öldürdü; canlılığı yaklaşık 21 mikromolde yarıya indirdi, oysa C878‑1660 yaklaşık dört kat daha yüksek konsantrasyon gerektirdi. Mikroskop altında, D685‑0061 ile muamele edilen hücreler yuvarlanma, yüzeyden ayrılma ve parçalanma gibi programlanmış hücre ölümü belirtileri gösterdi. Buna karşılık, deri kanseri hücrelerinde (A431) C878‑1660 daha güçlü öldürücüydü; yaklaşık 19 mikromolde %50 hücre ölümü sağlarken D685‑0061 için bu değer yaklaşık 28 mikromoldü ve yine doz bağımlı görülür hasar gözlendi.
Gelecekteki kanser tedavileri için ne anlama geliyor
Bu çalışma hemen yeni bir ilaç sunmuyor, ancak iki umut verici başlangıç noktası ve en az bunun kadar önemli bir şekilde daha fazlasını bulmak için güçlü bir yol haritası sunuyor. Büyük veri modellemesi, 3B simülasyonlar ve dikkatli hücre tabanlı deneyleri birleştirerek çalışma, uPAR’ın agresif meme ve deri kanseri hücrelerine zarar veren küçük moleküllerle seçici olarak hedeflenebileceğini gösteriyor. D685‑0061 ve C878‑1660 şimdi kimyagerlerin potensi artırmak, güvenliği iyileştirmek ve farmakokinetik özellikleri geliştirmek için rafine edebileceği lider bileşikler olarak hizmet ediyor. Uzun vadede, bu yaklaşımla geliştirilecek ilaçlar uPAR kaynaklı kanserlerin yayılmasını engellemeye yardımcı olabilir ve bugünkü en tehlikeli tümörlerin bir kısmını daha yönetilebilir hastalıklara dönüştürebilir.
Atıf: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Anahtar kelimeler: uPAR inhibitörleri, üçlü negatif meme kanseri, deri kanseri, bilgisayar destekli ilaç tasarımı, MTT hücre canlılığı testi