Clear Sky Science · tr
Siklofosfamid ve purinetholün bir kovalent triazin çerçevesinde (CTF-2) adsorpsiyonunun ilaç taşıma uygulamaları için bir yoğunluk fonksiyonel teorisi çalışması
Neden Daha Akıllı Kemoterapi Önemli
Kemoterapi ilaçları hayat kurtarıyor, ancak çoğu zaman spot ışığı gibi hedefe odaklanmak yerine bir floodlight (geniş aydınlatma) gibi davranarak kanser hücreleriyle birlikte sağlıklı hücrelere de saldırır. Bu, yorgunluk ve enfeksiyonlardan organ hasarına kadar ciddi yan etkilere yol açabilir. Burada ele alınan çalışma, kovalent triazin çerçevesi (CTF-2) adı verilen ultra ince, yüksek gözenekliliğe sahip bir malzemeyi, iki uzun süre kullanılan anticancer ilacı—siklofosfamid ve purinethol—ihtiyaç duyulan yere daha güvenli ve verimli şekilde taşıyıp tümör benzeri koşullarda serbest bırakabilecek bir “akıllı sünger” olarak inceliyor.
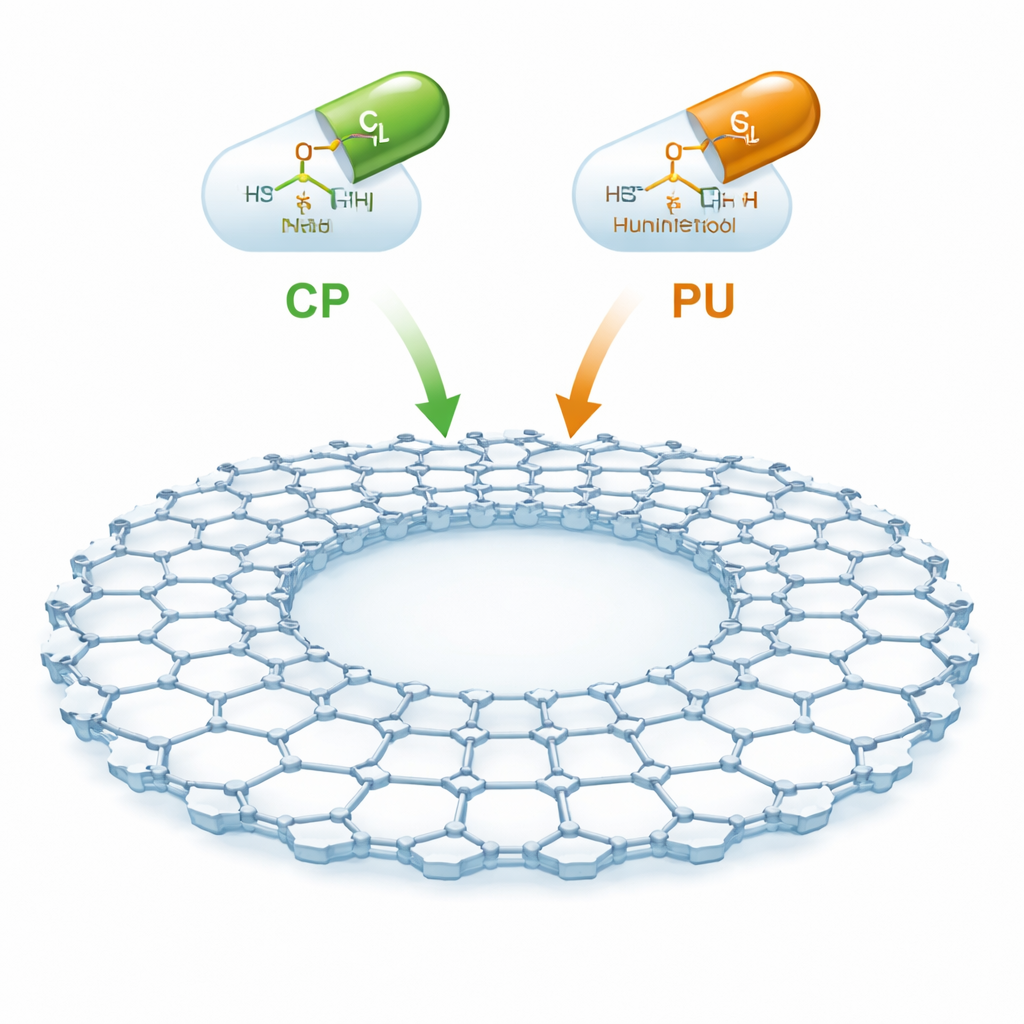
Yeni Türden Moleküler Bir Sünger
CTF-2, karbon ve nitrojenden oluşan halkaların düz, yaprak benzeri bir ağ halinde bağlanmasıyla oluşturulmuş yapay bir malzemedir; ortasında geniş bir boşluk ve bolca açık alan bulunur. İnce, kararlı ve gözenekli olduğu için ilaç moleküllerini hapsetmek için büyük bir iç yüzey alanı sunar. Yazarlar, kan kanserleri ve katı tümörlerde yaygın olarak kullanılan siklofosfamid ile lösemiler ve bazı enflamatuar barsak hastalıklarında kullanılan purinethol (diğer adıyla merkaptopurin) olmak üzere iki önemli kanser ilacına odaklandı. Amaç, bu ilaçları CTF-2 yüzeyine nazikçe tutturmak, böylece kan dolaşımı boyunca taşınabilmelerini ve daha seçici bir şekilde salınarak sağlıklı dokuya verilen zararın azaltılmasını sağlamaktır.
Bilgisayar Deneyleriyle Görünmez Olanı Sorgulamak
Laboratuvarda ıslak deneyler yapmak yerine ekip, her bir ilacın CTF-2’ye ne kadar güçlü yapışacağını ve kompleksleri bir arada tutanın ne olduğunu sormak için gelişmiş kuantum düzeyinde bilgisayar hesaplamaları (yoğunluk fonksiyonel teorisi ve ilgili yöntemler) kullandı. CTF-2 artı her ilacın şekillerini optimize ettiler, temas ettikleri atomlar arasındaki mesafeleri ölçtüler ve bir ilacın çerçeveye yapıştığında ne kadar enerji kazandığını hesapladılar. Siklofosfamid için hesaplanan adsorpsiyon enerjisi yaklaşık −1.04 elektronvolt iken, purinethol için bulunan değer −0.82 elektronvolttu; siklofosfamid için biraz daha güçlüydi. Teknik düzeltmeler ve suyu çözücü olarak simüle etme sonrasında da açıkça elverişli kalan bu değerler, her iki ilacın da yüklenebilecek kadar sağlam bağlandığını ancak daha sonra serbest bırakılamayacak kadar güçlü olmadığını gösteriyor.
Önemli İşleri Yapan Nazik Kuvvetler
Çalışma, ilaçlar ile CTF-2 arasındaki “yapıştırıcının” sert bir kimyasal bağ değil, nazik, kovalent olmayan kuvvetler ağı olduğunu gösteriyor. Paylaşılan elektronların nerede bulunduğuna dair haritalar niteliğindeki özel elektron yoğunluğu analizleriyle araştırmacılar, van der Waals çekimlerinin (geckoların duvarlara tırmanmasını sağlayan aynı zayıf kuvvetler) ve hafif elektrostatik etkileşimlerin baskın olduğunu buldular. Bu etkileşimler, ilaçlardaki ve çerçevedeki hidrojen, azot, oksijen, kükürt ve karbon atomları arasında kısa ancak bağ oluşturmayan mesafelerde gerçekleşir. Toplam çekimi farklı bileşenlere ayıran ek hesaplamalar, stabilizasyonun büyük kısmını elektrostatik ve dağılım (van der Waals) kuvvetlerinin sağladığını doğruladı; itici kuvvetler ise ilacın çok derine gömülmesini veya geri dönüşü olmayan şekilde bağlanmasını engelliyor.
Kararlı Yükleme ve Ayarlanabilir Salımın İşaretleri
Ekip ayrıca ilaçlar CTF-2 üzerinde oturduğunda elektronların nasıl kaydığını ve bunun temel elektriksel özellikleri nasıl değiştirdiğini inceledi. Her bir ilaç ile çerçeve arasında küçük ama belirgin yük transferleri ve dolu ile boş elektronik durumları ayıran enerji boşluğunda hafif bir daralma gözlemlediler. Bu, malzemenin yükleme sırasında reaktivitesinin ve iletkenliğinin ince biçimde ayarlandığını, gelecekteki sensör veya teranostik uygulamalar için faydalı bir özellik olabileceğini ima eder. Kritik olarak, tümör yakınlarında bulunan daha asidik ortamı taklit etmek için ek protonlar eklediklerinde hesaplanan bağlanmanın zayıfladığı ve temas mesafelerinin arttığı görüldü. Basitçe söylemek gerekirse, simülasyonlar CTF-2’nin normal kan benzeri koşullarda ilaçları tutabileceğini, ancak tümör benzeri asidik ortamlarda bunları daha kolay bırakma eğiliminde olacağını—hedefe yönelik dağıtım için arzu edilen davranışın tam olarak bu olduğunu—öneriyor.
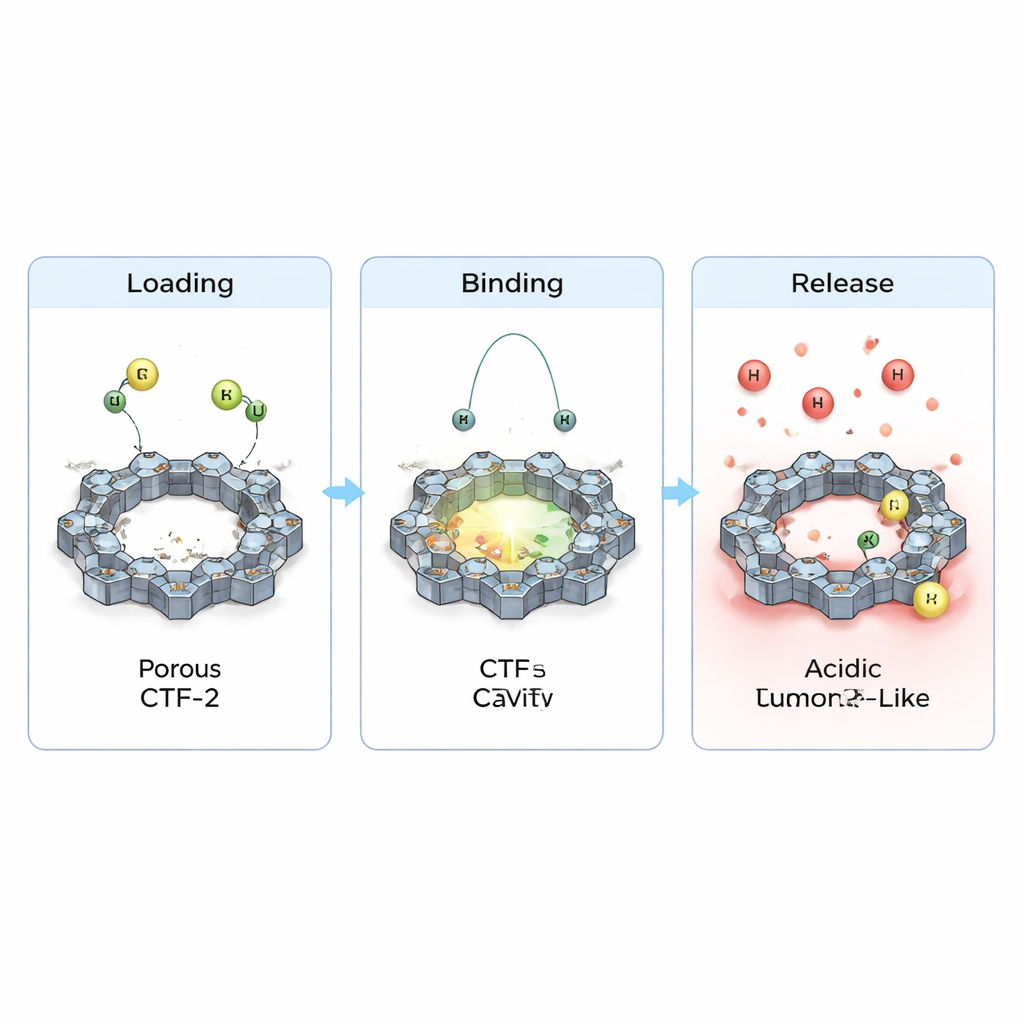
Gelecekteki Kanser Tedavileri İçin Ne Anlama Geliyor
Bir araya getirildiğinde, bu hesaplamalar CTF-2’yi siklofosfamid ve purinethol için umut verici bir taşıyıcı olarak resmediyor: bu ilaçları gözenekli yüzeyine kararlı bir şekilde paketleyebilir, dolaşım sırasında onları koruyabilir ve yerel kimya tümör çevresinde değiştiğinde serbest bırakabilir. Çalışma kuramsal olup deneysel doğrulamaya ihtiyaç duysa da, CTF-2 gibi ince tasarlanmış, azotça zengin çerçevelerin, etkili fakat eski ilaçları daha akıllı ilaçlara dönüştürmeye yardımcı olabileceğini—güçlü dozları gerektiği yere ulaştırırken sağlıklı hücrelere yönelik yan etkileri hafifletebileceğini—öneriyor.
Atıf: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Anahtar kelimeler: nanosürücü, ilaç dağıtımı, kanser kemoterapisi, kovalent triazin çerçevesi, hesapsal modelleme