Clear Sky Science · tr
Pnömoni tedavisi için potansiyel antioksidanlar olarak Bis-1,2,4-triazol türevleri
Akciğerleri “pas”tan korumanın önemi
Pnömoni genellikle antibiyotiklerle düzeltilebilen kötü bir akciğer enfeksiyonu olarak düşünülür. Ancak ağır pnömonili birçok kişi yalnızca mikroplardan değil, vücudun aşırı tepkisinden de hayatını kaybeder. Bağışıklık hücreleri bakteriler veya virüslerle savaşırken yüksek reaktiviteye sahip moleküller — akciğeri tıpkı pasın metali aşındırması gibi zarar verebilen kimyasal “kıvılcımlar” — salarlar. Bu çalışma, hem güçlü antioksidan hem de bakteriyel silahları bloke edici olarak tasarlanmış, laboratuvarda üretilen bis‑1,2,4‑triazoller adlı yeni bir molekül ailesini araştırıyor. Amaç, antibiyotikler enfeksiyonu temizlerken akciğerleri koruyan destekleyici ilaçlar geliştirmektir.
Akciğer enfeksiyonu sırasında gizli hasar
Mikroplar akciğerlere girdiğinde bağışıklık hücreleri reaktif oksijen ve azot türlerinin (ROS/RNS) patlamalarını başlatır. Küçük miktarlarda bunlar patojenleri öldürmeye yardımcı olur; aşırı miktarda ise vücudun kendi yağlarına, proteinlerine ve DNA’sına saldırır. Yakın tarihli klinik çalışmalar, COVID‑19 pnömonisi dahil olmak üzere ağır pnömonisi olan kişilerde oksidatif stres ve redoks dengesizliğinin açık izlerini gösteriyor. Bu kimyasal aşırı yük, akciğerin hassas hava keseciklerini zayıflatır, kontrolsüz iltihabı körükler ve akut solunum sıkıntısı sendromuna katkıda bulunur. Bu durum, hedeflenmiş antioksidanların bir tür yangın şeridi gibi davranıp bu reaktif molekülleri akciğer dokusunu yakmadan önce soğurup soğuramayacağı sorusunu gündeme getirdi.
Akciğerleri koruyacak yeni küçük moleküller tasarlamak
Ekip, birçok ilaçta yaygın olarak bulunan halka şeklinde bir kimyasal yapı olan 1,2,4‑triazole odaklandı. Tek bir halka kullanmak yerine iki halkayı birbirine bağlayarak bis‑1,2,4‑triazoller oluşturmuşlar; bu yapı hem suyu seven hem de yağı seven hücre bölümleriyle ve metal iyonlarıyla etkileşebilir. Altı böyle bileşik daha önce sentezlenmiş, antimikrobiyal etkiler ve iltihap ile kansere bağlı bir enzimin inhibisyonu gösterilmişti. Bu çalışmada yazarlar, karbon zincirinin uzunluğu gibi özellikleri ayarlamanın veya bağlı bir halkaya nitro grubu eklemenin bu molekülleri ROS’u nötralize etmede ve pnömonide rol oynayan bakteriyel virülans faktörlerini engellemede özellikle iyi hale getirip getirmeyeceğini sordu.
Laboratuvarda antioksidan gücün test edilmesi
Altı molekülün serbest radikalleri ne kadar iyi sildiğini ölçmek için araştırmacılar, DPPH adlı stabil bir radikal ile standart bir renk değişim testi kullandılar. Bir antioksidan bu radikali uzaklaştırdıkça çözeltinin rengi moradan sarıya döner ve solma derecesi hassas şekilde ölçülebilir. Tüm altı bis‑triazol doz bağımlı radikal temizleme aktivitesi gösterdi, ancak iki tanesi öne çıktı. Esnek altı karbonlu (heksil) zincir taşıyan bir bileşik ile para‑nitrofenil halkası taşıyan bir başka bileşik, klasik bir antioksidan olan C vitamini ile en yakın performansı gösterdi. Aynı yüzde 50 radikal bloke etme noktasına ulaşmak için yaklaşık iki kat C vitamini konsantrasyonuna ihtiyaç duydular, yine de umut verici ilaç adayları sayılacak kadar güçlü performans sergilediler. Yapıları, yağlı akciğer zarlarına yerleşmelerine ve tuttukları radikalleri stabilize etmelerine yardımcı gibi görünüyor.
Bakteriyel silahlara çarpmak ve ilaç‑benzeri kalmak
Antioksidan etkinin ötesinde ekip, yeni moleküllerin Streptococcus pneumoniae’den iki ana proteini bloke edip edemeyeceğini görmek için bilgisayar simülasyonları kullandı: bakterilerin dokulara tutunup nüfuz etmesine yardımcı olan NanA ve hücre zarlarında delikler açan bir toksin olan pneumolizin (Ply). Bilgisayar ortamında öne çıkan nitrofenil bileşik en sıkı bağlanan oldu; proteinlerin aktif ceplerinde çok sayıda hidrojen bağları ve üst üste yığılma etkileşimleri oluşturdu. Ağır doğal polifenoller kadar yapışkan olmasalar da, bu bis‑triazoller kompakt iskeletlerinin NanA ve Ply’in aynı savunmasız bölgelerini doldurabileceğini gösterdi. Emilim, metabolizma ve toksisite üzerine paralel bilgisayar modelleri, özellikle iki lider bileşiğin yüksek öngörülen bağırsak emilimine, düşük toksisiteye, yaygın ilaçları metabolize eden enzimlerle büyük etkileşime sahip olmamaya ve kalp ritim kanallarını bozma eğiliminin olmamasına işaret etti; bu özellikler bir “ilaç‑benzeri” profilin anahtar unsurlarıdır.
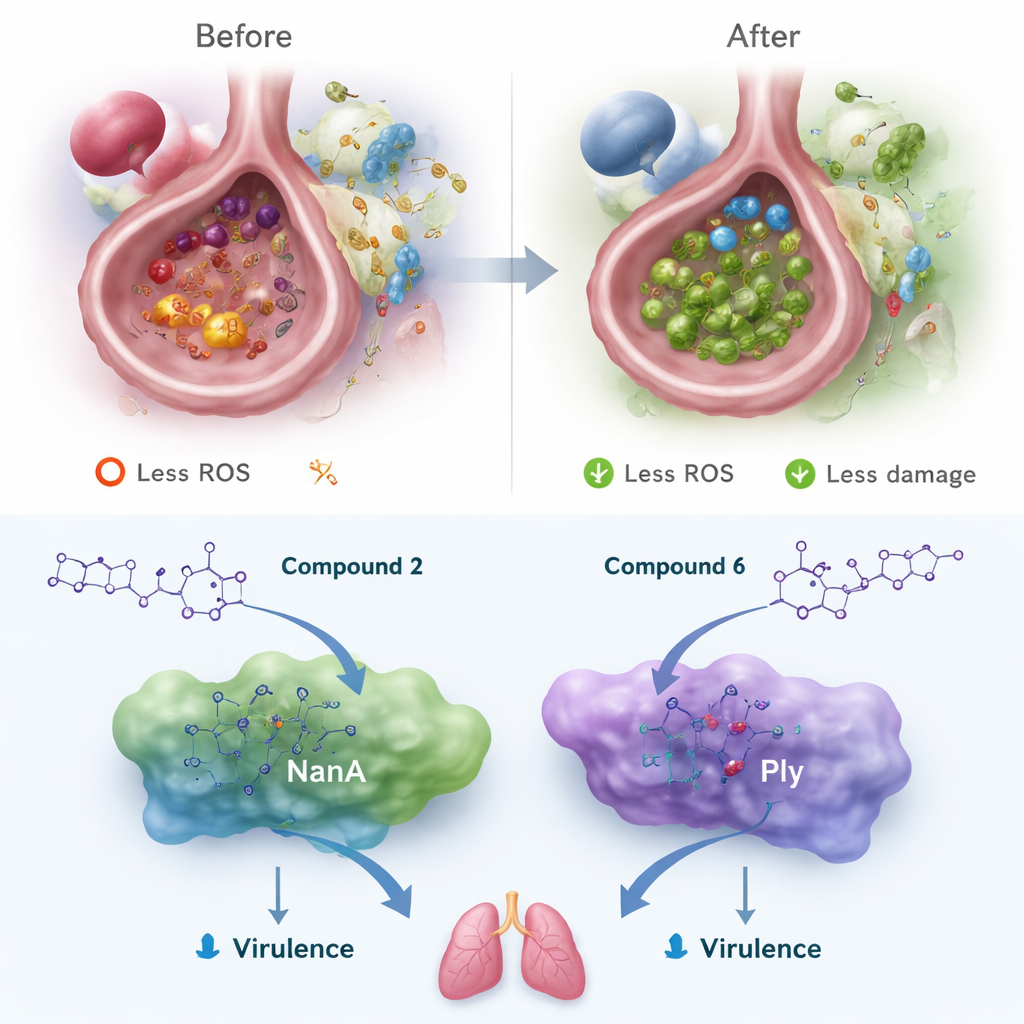
Geleceğin pnömoni tedavisi için olası sonuçlar
Bir arada değerlendirildiğinde sonuçlar, özellikle en iyi performans gösteren iki molekül olmak üzere bis‑1,2,4‑triazollerin pnömoni tedavisi için çift etkili yardımcıların erken prototipleri olabileceğine işaret ediyor. İlke olarak, bu tür bileşikler hem akciğer dokusunu aşındıran zararlı reaktif molekülleri soğurabilir hem de hastalığı kötüleştiren bakteriyel araçları köreltebilir; üstelik oral kullanım için yeterince güvenli olabilir ve büyük ölçüde beyne girmeyebilirler. Çalışma hâlâ preklinik aşamada: bileşiklerin şimdi insan akciğer hücrelerinde ve pnömoni hayvan modellerinde güvenlik testlerinden geçirilmesi, potensi artırmak ve çözünürlüğü iyileştirmek için yapıların muhtemelen rafine edilmesi gerekiyor. Ancak çalışma, uzman olmayan okuyucular için açık bir mesaj veriyor: gelecekteki pnömoni tedavileri yalnızca antibiyotiklere dayanmayabilir; aynı zamanda bağışıklık sistemimizin yol açtığı yan hasardan akciğerlerimizi koruyan küçük molekülleri de içerebilir.
Atıf: Korol, N., Symkanych, O., Pallah, O. et al. Bis-1,2,4-triazole derivatives as potential antioxidants for pneumonia therapy. Sci Rep 16, 5640 (2026). https://doi.org/10.1038/s41598-026-36386-5
Anahtar kelimeler: pnömoni, oksidatif stres, antioksidanlar, bakteriyel virülans, ilaç tasarımı