Clear Sky Science · tr
Yüksek verimli sanal tarama (HTVS) yaklaşımının, antikanser özelliklere sahip yeni laktat dehidrogenaz (LDH) inhibitörlerinin saptanması için uygulanması
Bu araştırmanın kanser tedavisi için önemi
Kanser hücreleri sıklıkla enerji üretim yollarını yeniden düzenler ve bu değişiklik daha akıllı, daha seçici ilaçlar tasarlamak için kullanılabilir. Bu çalışma, tümörlerin zorlu koşullarda hayatta kalmasına ve tedaviye direnmesine yardımcı olan laktat dehidrogenaz (LDH) adı verilen anahtar bir metabolik enzimi inceliyor. Gelişmiş bilgisayar tabanlı tarama ve laboratuvar testleri kullanarak araştırmacılar LDH’yi bloke eden ve prostat kanseri hücre hatlarında vaat eden antikanser etkiler gösteren iki yeni küçük molekül tanımladı.
Kanser hücrelerinin tuhaf metabolizması
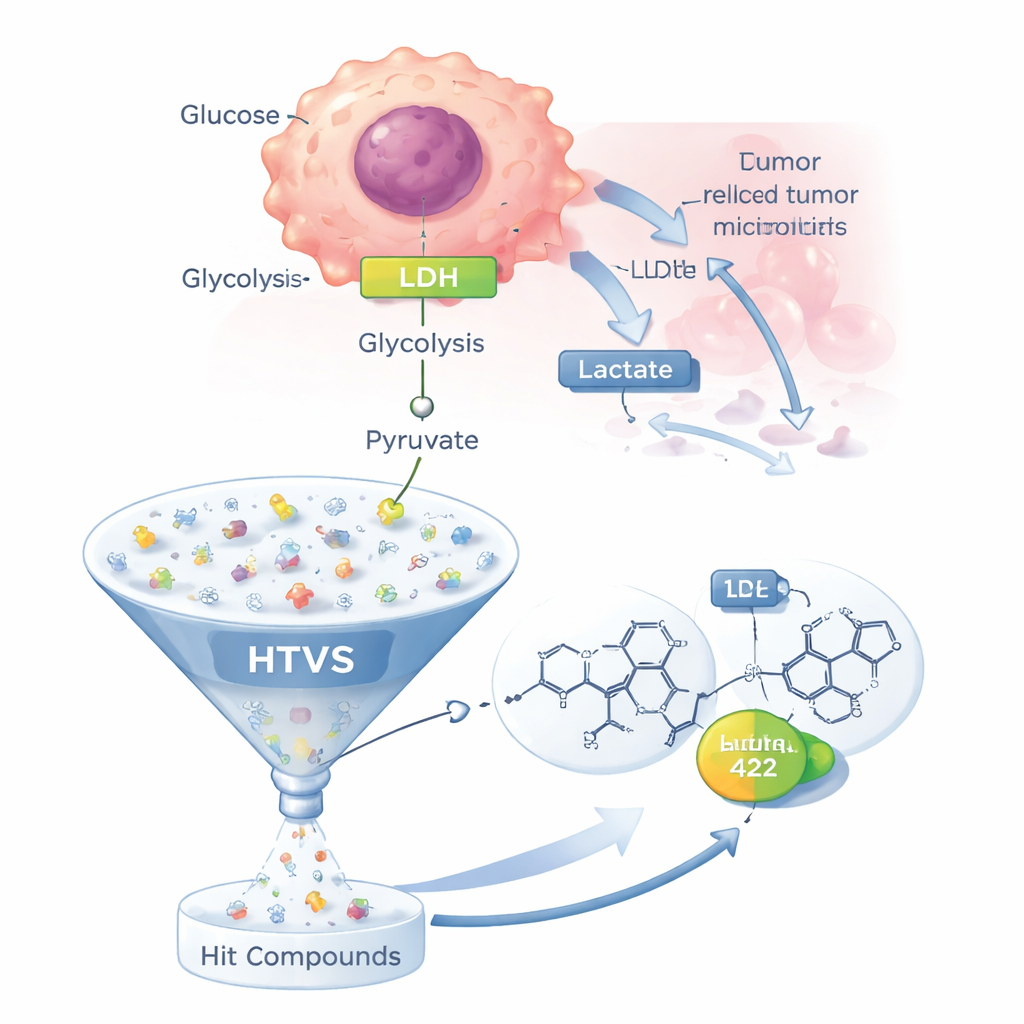
Çoğu sağlıklı hücre enerji üretmek için mitokondrilerinde oksijeni verimli şekilde kullanır. Ancak birçok kanser hücresi, oksijen bol olsa bile daha az verimli olan glikoliz yoluna güçlü biçimde güvenir — bu olgu Warburg etkisi olarak bilinir. Bu kestirme yolda glukoz pirüvata parçalanır ve pirüvat mitokondrilere girmek yerine LDH ile laktata dönüştürülür. Laktat hücre dışına pompalanarak tümörün çevresini asitleştirir, kanser hücrelerinin hücre ölümünden kaçmasına, bağışıklık saldırısını zayıflatmasına ve birçok kemoterapi ilacının etkisini köreltmesine yardımcı olur. LDH bu değişmiş metabolizmanın merkezinde yer aldığı ve hâlâ onaylanmış hiçbir LDH hedefine yönelik ilaç bulunmadığı için yeni antikanser tedaviler açısından yüksek öncelikli bir hedef haline gelmiştir.
Yarım milyon molekülü bilgisayarlarla elemek
Potansiyel ilaçları laboratuvarda tek tek test etmek yerine ekip yüksek verimli sanal tarama (HTVS) stratejisi kullandı. Bilimsel literatürde daha önce rapor edilmiş 28 LDH-bloklayan molekülden başlayıp bunlardan iyi bir LDH inhibitörünün muhtemelen paylaşacağı özelliklerin soyut bir 3B deseni olan bir "farmakofor" çıkardılar. Ardından bu modeli yaklaşık 500.000 tane ilaç benzeri molekül içeren ticari bir kütüphaneye uyguladılar ve hangi adayların temel özelliklerle eşleştiğini sorguladılar. Yaklaşık 110.000 molekül bu ilk eleği geçti ve standart "ilaç-benzeri" kurallara göre yapılan ek seçilim listeleri 2.337 daha gerçekçi adaya düşürdü; bunlar LDH enzimine yerleştirme (docking) için kullanıldı.
En iyi bağlananlara odaklanmak
Bir sonraki adım bu adayların LDH’nin aktif bölgesine ne kadar sıkı sığabileceğini tahmin etmekti. Araştırmacılar çeşitli düzeylerde hesaplamalı docking kullanarak her molekülün enzim cebi içindeki belirli aminoasitlerle nasıl etkileşebileceğini hesapladı. Bu çok aşamalı süreç binlerce adayı kademeli olarak 59 umut verici moleküle ve ardından özellikle güçlü bağlanma öngörülen beş belirgin "hit"e indirdi. Bunlardan ikisi, 15 ve 422 numaralı bileşikler, bilgisayar tabanlı moleküler dinamik simülasyonlarının zaman içinde LDH ile olağanüstü stabil kompleksler oluşturduklarını, aktif bölgedeki kritik kalıntılarla ana temasları koruduklarını ve genel protein yapısını makul ölçüde muhafaza ettiklerini göstermesi nedeniyle öne çıktı.
Tarama sonuçlarını gerçek kanser hücrelerine taşımak
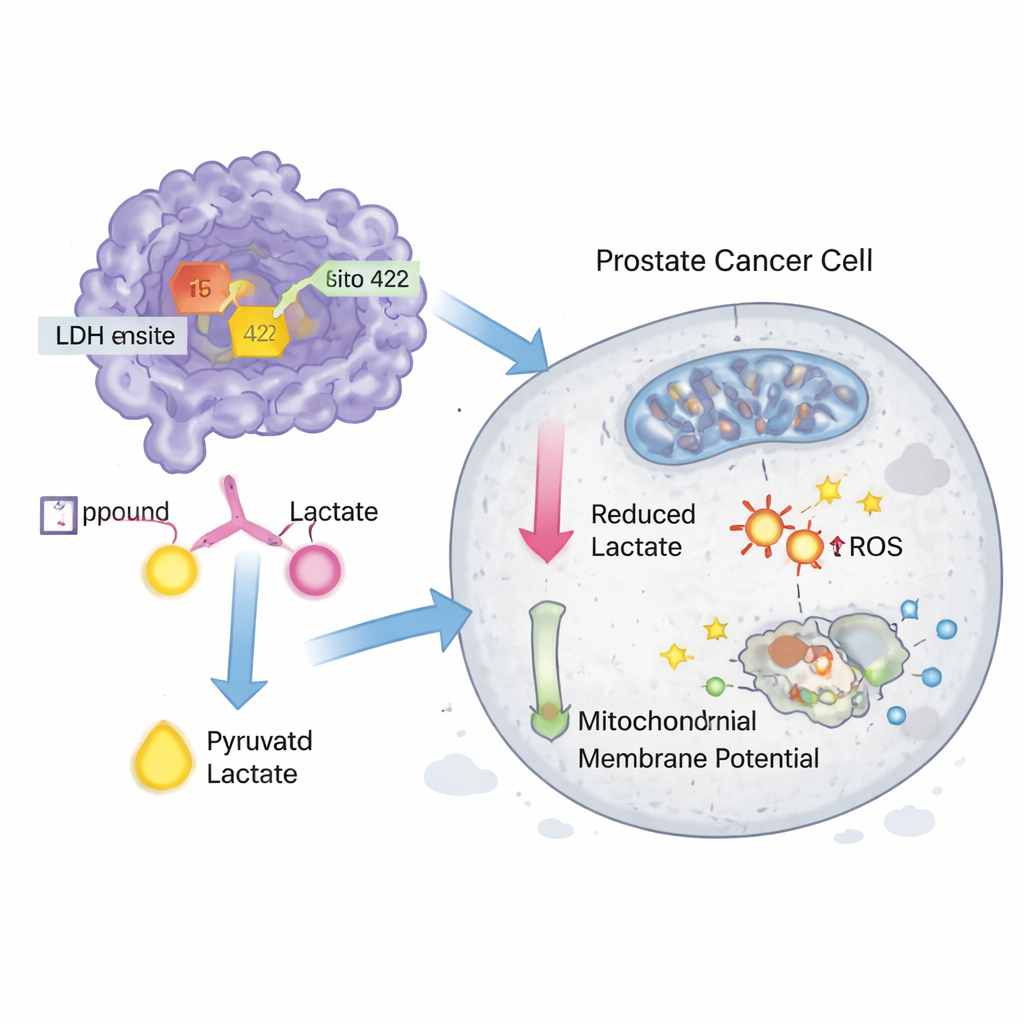
Bu hitlerin canlı sistemlerde önem taşıyıp taşımadığını görmek için bilim insanları 15 ve 422 numaralı bileşikleri satın alıp prostat kanseri hücre hatları DU-145 ve PC-3’te test etti. Her iki molekül de hücrelerde nanomolar konsantrasyonlarda LDH aktivitesini engelledi ve ayrıca saflaştırılmış bir LDH enziminin aktivitesini doğrudan yavaşlattı; ancak deneysel bilinen bir inhibitör olan GNE‑140’a kıyasla biraz daha az güçlüydüler. Büyüme testlerinde bu bileşikler kanser hücrelerinin hayatta kalmasını düşük mikromolar dozlarda azalttı ve yine GNE‑140’a yaklaşan performans sergiledi. Ek deneyler, tedavilerin hücrelerde oksidatif stresi hafifçe artırdığını, enerji fabrikalarının bozulduğuna işaret eden mitokondri zar potansiyelini bozduğunu ve DU‑145 hücrelerinde programlı hücre ölümünü (apoptoz) tetiklediğini gösterdi; bunlar arasında 15 numaralı bileşik iki bileşik içinde daha aktif olan oldu.
Gelecekteki kanser ilaçları için olası çıkarımlar
Bu moleküller hazır ilaçlar olmasa da, ilaç tasarımı için değerli başlangıç noktaları sunarlar. Hem 15 hem de 422 numaralı bileşikler bazı mevcut LDH inhibitörlerine kıyasla daha iyi çözünürlük, geçirgenlik ve genel "ilaç-benzeri" özellikler önerebilecek kimyasal özelliklere sahip olup daha ileri optimizasyon için cazip liderlerdir. Çalışma, bilinen yapısal özellikler tarafından yönlendirilen geniş ölçekli bilgisayar taramasının, kanser hücrelerini değişmiş enerji arzını keserek zayıflatan yeni LDH inhibitörlerini ortaya çıkarabileceğini gösteriyor. Yapıların rafine edilmesi, doğrudan bağlanmanın daha titiz şekilde test edilmesi ve hayvanlarda davranışlarının incelenmesi gibi ileri çalışmalarla bu bileşikler, tümörleri benzersiz metabolik zayıflıkları üzerinden hedef alan yeni bir antikanser ajan sınıfına katkıda bulunabilir.
Atıf: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Anahtar kelimeler: laktat dehidrogenaz inhibitörleri, kanser metabolizması, sanal tarama, prostat kanseri, antikanser ilaç keşfi