Clear Sky Science · tr
MGMT artışı, USP5 bağımlılığının verdiği Temozolomid direncini kolaylaştırır
Neden bazı beyin tümörleri hayati önemdeki bir ilaca yanıt vermeyi keser
Agresif beyin kanseri glioblastomlu kişiler için doktorların güvendiği başlıca ilaçlardan biri temozolomiddir. İlk başta bu kemoterapi hastalığı yavaşlatabilir, ancak tümörler sıklıkla ilaca karşı koymayı öğrenir. Bu çalışma, yaşam‑ve‑ölüm sonuçları olan pratik bir soruyu soruyor: bu kanser hücrelerinin ilacı nasıl atlattığı tam olarak nedir ve tedavinin tekrar işe yaramasını sağlamak için yeni zayıf noktalar bulabilir miyiz?
Başta işe yarayan, sonra etkisini yitiren bir ilaç
Temozolomid, hızla bölünen tümör hücrelerinin DNA’sına zarar vererek onları öldürmeye zorlar. Ancak birçok glioblastom, bu hasarı geri alabilen MGMT adlı bir onarım proteini üretir. Tümörleri MGMT’yi açan (etkinleştiren) hastalar genellikle daha kötü sonuç alır çünkü ilacın etkisi iptal edilir. Doktorlar, MGMT geninin kimyasal olarak kapalı (metile olmuş) veya açık (metile olmamış) olup olmadığına bakarak yanıtı kısmen tahmin edebilir, ama bu durum direncin nasıl geliştiğini veya MGMT düzeylerinin tümör hücreleri içinde zamanla nasıl yüksek kaldığını tam olarak açıklamaz.
Onarım proteininin arkasındaki gizli yardımcılar
Yazarlar kontrolün başka bir katmanını incelediler: hangi proteinlerin yok edileceğine ve hangilerinin korunacağına karar veren moleküler “temizlik ekipleri”. Hücreler normalde yıpranmış proteinleri yıkım için etiketlerken, deubiquitinating enzimler (DUB’ler) adı verilen bir enzim grubu proteinleri bu akıbetten kurtarabilir. Büyük halka açık kanser veri tabanlarını tarayarak ve laboratuvarda büyütülen ilaç dirençli glioblastom hücre hatlarını inceleyerek ekip, USP5 ve USP8 adlı iki enzime odaklandı. Yüzlerce hasta örneğinde daha yüksek USP5 düzeyleri genellikle daha yüksek MGMT düzeyleriyle birlikte gözlendi ve her iki genin de yüksek olduğu tümörlere sahip hastalar genel olarak daha erken yaşamını yitirdi.
Laboratuvarda direnç inşa etmek
Araştırmacılar, hastalarda olanı taklit etmek için iki yaygın glioblastom hücre hattını giderek artan temozolomid dozlarına yavaşça maruz bıraktılar ve hücreler dirençli hale geldi. Bu sertleşmiş hücrelerde birkaç DUB yükseldi, ancak özellikle USP5, USP8, USP10 ve onarım proteini MGMT belirgin şekilde artmıştı. Ekip USP5 veya USP8’i küçük RNA molekülleriyle susturduğunda, dirençli hücreler aniden savunmasızlaştı: apoptoz ve otophaji olarak bilinen stres kaynaklı kendini sindirme dahil olmak üzere kendini yok etme programlarını aktive ettiler. Aynı zamanda MGMT düzeyleri hızla düştü ve başka bir dirençle ilişkili protein olan USP10 da azaldı; bu da bu enzimlerin hayatta kalma ağının üstünde yer aldığını düşündürüyor.
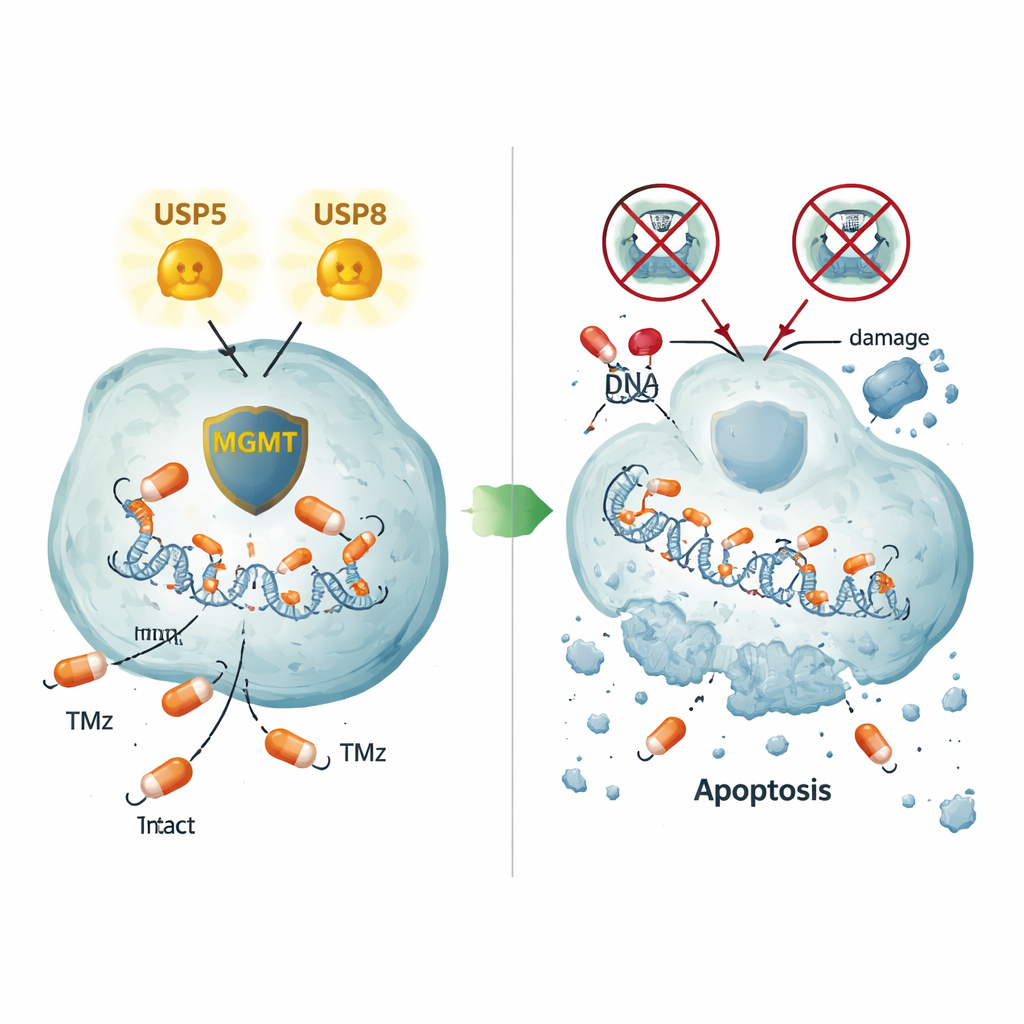
MGMT’yi canlı tutmanın iki farklı yolu
Titiz hücre ve insan tümör dokusu görüntülemeleri USP5 ile MGMT’nin genellikle hücrenin aynı bölgelerinde, özellikle sitoplazmada birlikte bulunduğunu gösterdi. USP5’i engellemek yalnızca MGMT’yi düşürmekle kalmadı, aynı zamanda MGMT’nin hücrenin protein öğüten makinesince parçalanmasına yol açtı; bu süreç, proteazomu bloke eden bortezomib ile tersine çevrilebiliyordu. MGMT üretmeyen hücrelerde USP5’i aşırı üretmek, beyin dışı bir hücre hattında bile MGMT protein düzeylerini yükseltmek için yeterliydi; bu da doğrudan bir stabilize edici etkiyi doğruladı. USP8 ise farklı davrandı: onu azaltmak da MGMT’yi düşürdü, ancak USP5’i değiştirmedi; bu da MGMT’yi koruyan ikinci, USP5’e bağımlı olmayan bir yol olduğunu gösteriyor. Hiç MGMT yapmayan dirençli bir hücre hattında bile USP5 veya USP8’i kapatmak geniş çaplı hücre ölümü tetikledi; bu da bu enzimlerin kontrol ettiği ek direnç yollarına işaret ediyor.
Bağışıklık sistemiyle bağlantılar ve yeni tedavi fikirleri
İlaç direncinin ötesinde, çalışma USP5’i glioblastomun bağışıklık sistemiyle etkileşimiyle ilişkilendiriyor. Genomik veri analizleri, USP5 düzeylerindeki ve gen kopya sayısındaki değişikliklerin tümör çevresindeki çeşitli bağışıklık hücrelerinin dengesini, öldürücü T hücreleri ve düzenleyici T hücreleri de dahil olmak üzere kaydırdığını öne sürdü. Önceki çalışmalar ayrıca USP5’in, tümörlerin saldıran T hücrelerini kapatmak için kullandığı bir protein olan PD‑L1’i stabilize edebileceğini göstermişti. Bir arada değerlendirildiğinde bulgular, USP5’in tümörlerin hem kemoterapiden sağ kalmasına hem de bağışıklık saldırısından kaçmasına yardımcı olabileceğini, bu nedenle onu özellikle çekici bir ilaç hedefi haline getirdiğini düşündürüyor.
Gelecekteki beyin kanseri tedavisi için anlamı
Basitçe söylemek gerekirse, bu çalışma USP5 ve USP8’i MGMT onarım proteininin koruyucuları ve glioblastom hücrelerinin temozolomide direnmesine yardımcı olan kilit bekçiler olarak tanımlıyor. Bu bekçileri dağıtarak yazarlar laboratuvarda ilaç‑dirençli hücreleri öldürebildiler ve MGMT düzeylerini düşürebildiler; bazı durumlarda MGMT tabanlı direnç tek sorun olmasa bile. Bu, gelecekte USP5 veya USP8’i hedef alan ilaçların, mevcut kemoterapi ve bağışıklık tabanlı ilaçlarla kombinasyon halinde, inatçı beyin tümörlerini yeniden duyarlı hale getirebileceği ve hastalara daha fazla zaman kazandırabileceği umudunu artırıyor.
Atıf: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
Anahtar kelimeler: glioblastom, temozolomid direnci, MGMT, USP5, deubiquitinating enzymes