Clear Sky Science · tr
MNX1 aracılı histon değişikliklerinin ve PBX gen ailesinin MNX1 kaynaklı lökemogenezdeki rolü
Neden küçük bir genetik aksaklık hasta çocuklar için önemli?
Çoğu çocukluk çağı lösemisi artık tedavi edilebilir durumda, ancak infant akut miyeloid lösemi (AML) olarak adlandırılan nadir bir tür hâlâ özellikle ölümcüldür. Bu bebeklerin birçoğu aynı genetik kazayı paylaşır: iki kromozom parça değiş tokuşu yapar ve gelişimsel bir gen olan MNX1 susturulmuş halinden çıkarak aşırı aktif bir sürücüye dönüşür. Bu çalışma basit ama hayati bir soruyu soruyor: MNX1 bir kez etkinleştirildiğinde, genç kan hücrelerinin içinde kanseri tetiklemek için gerçekte ne yapıyor — ve bu süreç kesintiye uğratılabilir mi?
Normal bebek kan hücrelerinden kontrolsüz büyümeye
Lösemi, olgunlaşmayı bırakan ve kontrolsüz şekilde çoğalan olgunlaşmamış kan hücrelerinde ortaya çıkar. t(7;12) kromozom değiş tokuşunu taşıyan bebeklerde MNX1, fetal karaciğer ve kemik iliğinde bulunan çok erken kan yapıcı hücrelerde anormal şekilde aktiftir. Araştırmacılar bu durumu taklit eden bir fare modeli oluşturdu: insan MNX1’i fetal kan kök hücrelerinde açtılar, bunları farelere nakletti ve hayvanların pre-lösemik bir durumdan tam lösemiye nasıl ilerlediğini izlediler. Bu farklı evrelerdeki hücreleri sağlıklı kontrollerle karşılaştırarak MNX1’in hücrenin iç kontrol sistemlerini zaman içinde nasıl yeniden kabloladığını izleyebildiler.
MNX1 hücrenin talimat kitabını nasıl yeniden yazar?
MNX1, hangi genlerin açık veya kapalı olacağını kontrol eden DNA üzerinde yer alan bir transkripsiyon faktörüdür. Ekip, MNX1’in birlikte çalıştığı ortakları ve hangi genleri değiştirdiğini görmek için kütle spektrometrisi, RNA dizileme ve kromatin profilleme gibi birkaç güçlü yöntemi birleştirdi. MNX1’in, DNA’nın etrafına sarılı iplik bobini benzeri yapılar olan histon proteinlerine kimyasal işaretler ekleyen enzimlerle ortak çalıştığını buldular. Özellikle, MNX1 belirli genom bölgelerinde “AÇIK” bir işaret olan H3K4me3’ü artırırken “KAPALI” bir işaret olan H3K27me3’ü azaltıyor. Bu değişiklikler yerel DNA yapısını gevşetir ve büyümeyle ilişkili anahtar genlerin açılmasını kolaylaştırır.
Kritik bir kontrol genine yapılan kısa, ama etkili müdahale
Etkilenen birçok gen arasında öne çıkan bir tanesi vardı: PBX ailesinin parçası olan ve uzun süredir lösemiyle ilişkilendirilen Pbx1. Çalışma, MNX1’in Pbx1 geninin kontrol bölgesine doğrudan bağlandığını, orada AÇIK işareti artırıp KAPALI işareti sildiğini gösteriyor. Bu, hücreler hâlâ sadece pre-lösemik haldeydiyken Pbx1 ekspresyonunun erken aşamada hızla artmasına yol açıyor. İlginç bir şekilde, daha sonra — lösemi yerleştiğinde — MNX1 artık o bölgede güçlü bir şekilde bağlı değil, ancak Pbx1 geni açık kalmaya ve histon işaretleri pro-büyüme konfigürasyonunda kalmaya devam ediyor. Bu durum, MNX1’in kritik kromatin bölgelerini kısa süreli ziyaret edip kalıcı epigenetik izler bıraktığı ve sonrasında ayrılabildiği bir “vuruş ve kaç” mekanizmasını düşündürüyor; bırakılan değişiklikler hastalığı beslemeye devam ediyor.
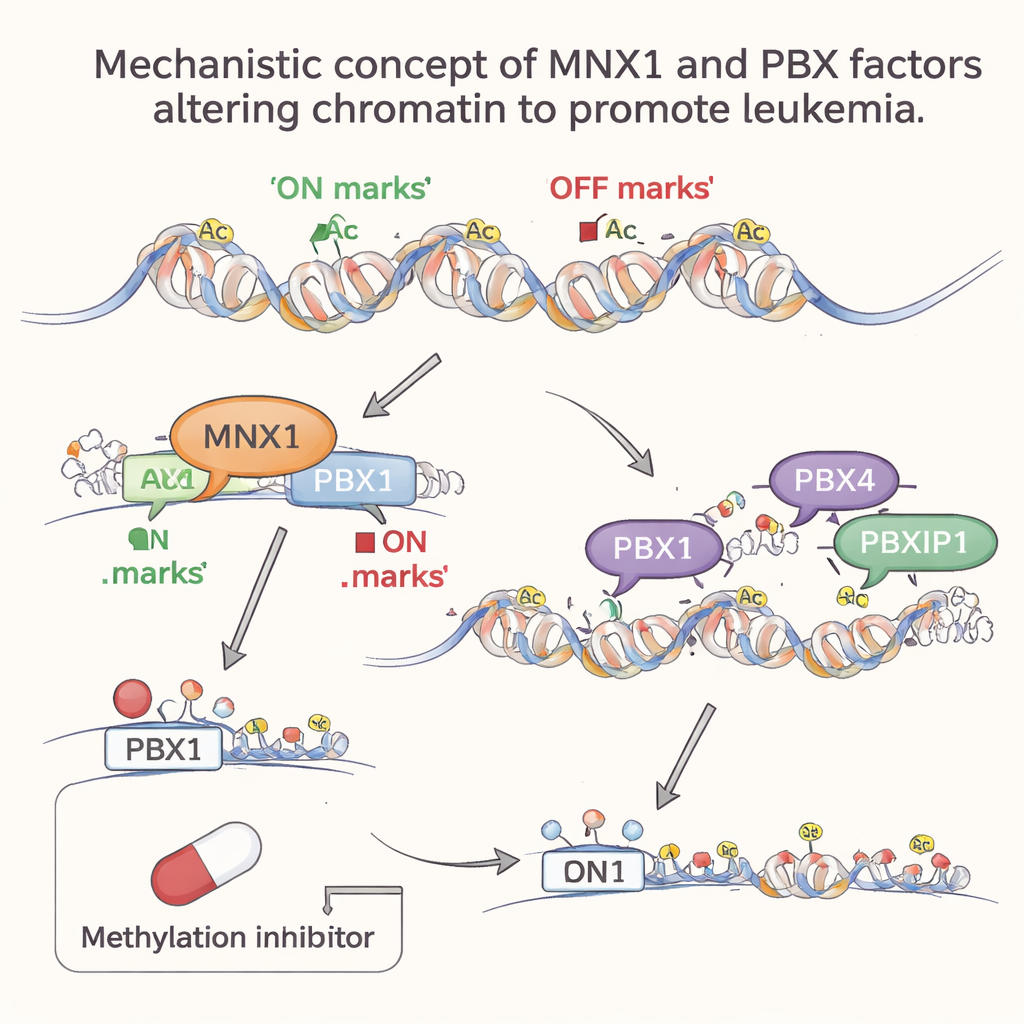
Kanser durumunu kilitlemek için geç dönem yardımcılar devreye giriyor
Lösemi ilerledikçe, PBX ailesinin diğer üyeleri PBX4 ve PBXIP1 daha aktif hale geliyor, ancak bu yalnızca geç dönemde görülüyor. Genom çapındaki analizler, bu genlerin tercih ettikleri DNA motiflerinin MNX1 aktivitesinin ardından yeniden şekillenen açık, aktif kromatin bölgelerinde yoğunlaştığını gösterdi. Başka bir deyişle, MNX1 önce kromatin manzarasını yeniden şekillendiriyor ve Pbx1’i açıyor; ardından PBX4 ve PBXIP1 bu yeni erişilebilir bölgelere girerek hücre bölünmesini teşvik eden, normal kan gelişimini engelleyen ve DNA onarımını zayıflatan anormal gen programlarını pekiştiriyor. Bu aşamalı katılım, bir görev paylaşımına işaret ediyor: PBX1 MNX1’e bağımlı erken bir anahtar olarak görev yaparken, PBX4 ve PBXIP1 lösemik programın sürdürülmesine yardımcı oluyor.
Lösemiyi besleyen kimyasal işaretleri engellemek
MNX1 histonlara metil grubu ekleyen enzimler aracılığıyla çalıştığı için ekip, geniş etkili bir metiltransferaz inhibitörü olan Sinefungin’in bu olay zincirini bozup bozamayacağını test etti. MNX1 eksprese eden pre-lösemik fetal kan hücrelerinde Sinefungin, MNX1’in dayandığı promotor-spesifik metilasyonu engelleyerek Pbx1 düzeylerini keskin şekilde azalttı. Buna karşılık PBX4 ve PBXIP1 düzeyleri neredeyse değişmedi; bu da onların hastalık ilerlemesi sırasında daha geç ve dolaylı olarak aktifleştiklerini destekliyor. Birlikte, bu sonuçlar t(7;12) taşıyan infant AML’nin sadece bozuk bir gen tarafından değil, MNX1’in başlattığı kalıcı epigenetik değişiklikler zinciri tarafından da sürüklendiğine dair ikna edici bir kanıt sunuyor.
Gelecekteki tedaviler için ne anlama geliyor?
Uzman olmayanlar için çıkarılacak ana mesaj şudur: Bu çalışma bir zincirleme reaksiyonun haritasını çıkarıyor — aşırı aktif MNX1 geni DNA paketleyen proteinlerin üzerindeki kimyasal işaretleri yeniden düzenliyor, PBX1’i erken dönemde açıyor ve PBX4 ile PBXIP1’in hücreleri lösemik bir duruma kilitlemesine zemin hazırlıyor. Bu adımlar belirli histon metilasyon modellerine bağlı olduğu için, bu işaretlere müdahale eden ilaçlar için açık, test edilebilir hedefler sunuyorlar. Uzun vadede MNX1–PBX eksenini veya bu epigenetik etiketleri yerleştiren enzimleri hedef alan terapiler, infant bu agresif löseminin sürüklediği hatalı talimatları kapatmaya yardımcı olarak kalıcı kür şansını artırabilir.
Atıf: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Anahtar kelimeler: infant akut miyeloid lösemi, MNX1, PBX1 PBX4 PBXIP1, epigenetik histon metilasyonu, t(7;12) kromozomal translokasyon