Clear Sky Science · tr
Kolorektal kanser tedavisi için polimerik nanojeller aracılığıyla dapagliflozinin yeniden kullanımı
Bir diyabet ilacının kolon kanseriyle savaşta nasıl yardımcı olabileceği
Kolorektal kanser, dünya çapında kanser kaynaklı ölümlerin önde gelen nedenlerinden biridir ve birçok hasta ameliyat ve kemoterapiye rağmen nüks eder. Bu çalışma, bu hastalığa karşı beklenmedik bir müttefiki inceliyor: tip 2 diyabet için yaygın bir hap olan dapagliflozin. Araştırmacılar, bu ilacı midede yumuşak bir jele dönüşen küçük parçacıklar içine paketleyerek, ağız yoluyla alınan dozları mevcut tabletlere benzer tutarken ilacı kolorektal tümörlerin büyüdüğü kalın bağırsağa daha fazla iletmeyi amaçlıyorlar.
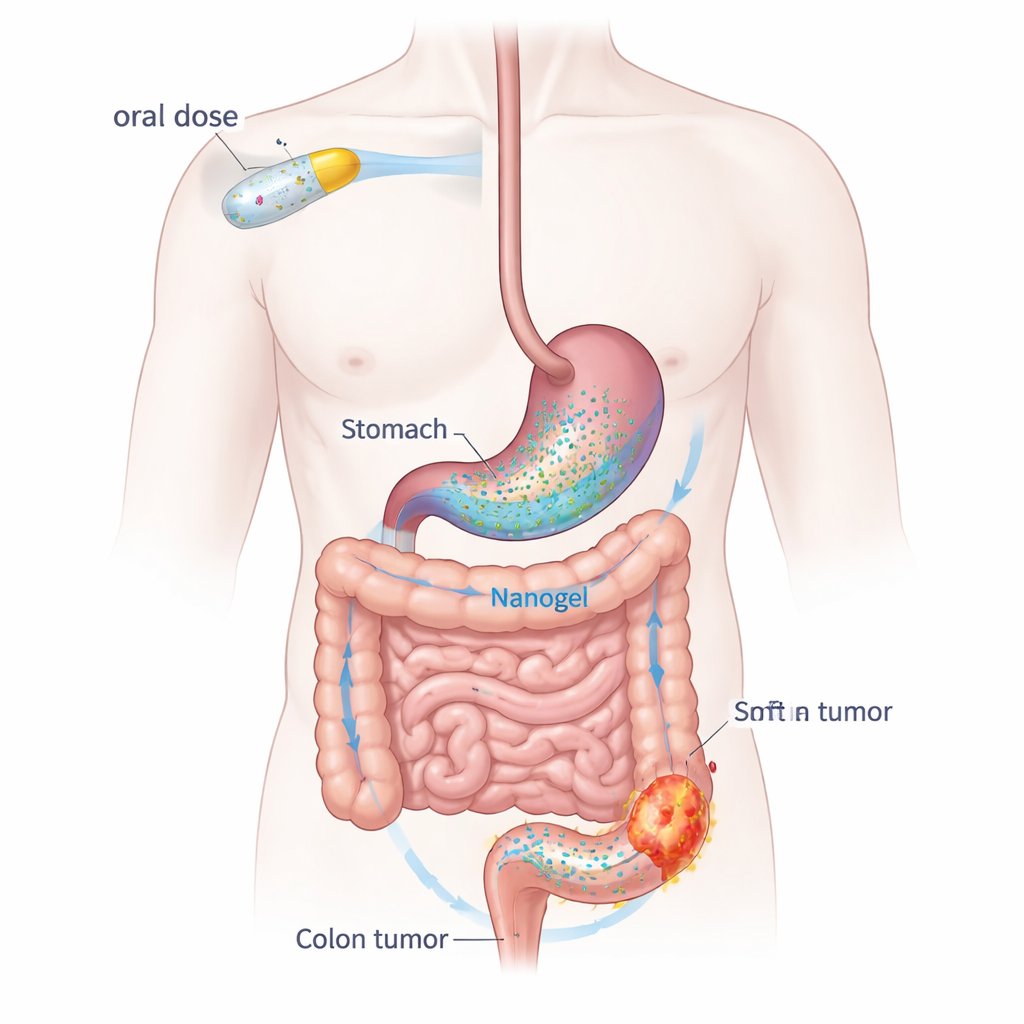
Günlük bir hapı kanser hedefleyen bir yük haline getirmek
Dapagliflozin normalde kan şekeri düşürmek için böbreklerde etki eder, ancak aynı zamanda inflamasyonu yatıştırır ve hücre çoğalmasını yavaşlatır—kanserlerin dayandığı iki süreç. Yalnız başına ilaç suda zayıf çözünür ve vücuttan oldukça hızlı temizlenir. Bunu aşmak için ekip, iki gıdaya yakın polimer kullanarak bir “nanojel” dağıtım sistemi geliştirdi: deniz yosunundan elde edilen sodyum aljinat ve yaygın kullanılan, biyouyumlu bir kıvam arttırıcı olan poli(vinil alkol). İlaç, milimetrenin yaklaşık onbinde bir genişliğindeki nanopartiküllerin içinde tutuluyor. Bu parçacıklar mide asidiyle karşılaştığında bir araya gelip yumuşak bir hidrojeli oluşturuyor, burada bir süre kalıyor ve kolona doğru ilerlerken ilacı yavaşça salıyor.
İlacı daha çözünür ve daha yavaş temizlenen hale getirmek
Bilim insanları önce parçacıkların nasıl üretildiğini optimize etti; nanopartiküllerin küçük, eşit boyutlu ve sıvıda kararlı kalması için iki polimerin oranını hassaslaştırdılar. İlacın polimer ağ içinde iyi gömüldüğünü ve kısmen kristal formdan daha amorf bir forma dönüştüğünü doğruladılar; amorf formlar genellikle daha iyi çözünür. Mide ve bağırsak sıvılarını taklit eden test çözeltilerinde, nanojel formülasyonu dapagliflozinin görünen çözünürlüğünü ham ilaca kıyasla yaklaşık 1,7–1,8 kat artırdı. İlacın ne kadar hızlı sızdığını izlediklerinde, nanojel birkaç saat boyunca nazik bir “yavaş salım” profili gösterdi; saf ilacın sergilediği hızlı salımdan farklı olarak. F2 adlı belirli bir tarif, asidik koşullarda en az iki saat boyunca bir arada kalan, sıkı ve dayanıklı bir jel oluşturdu ve ilacı kararlı şekilde saldı.
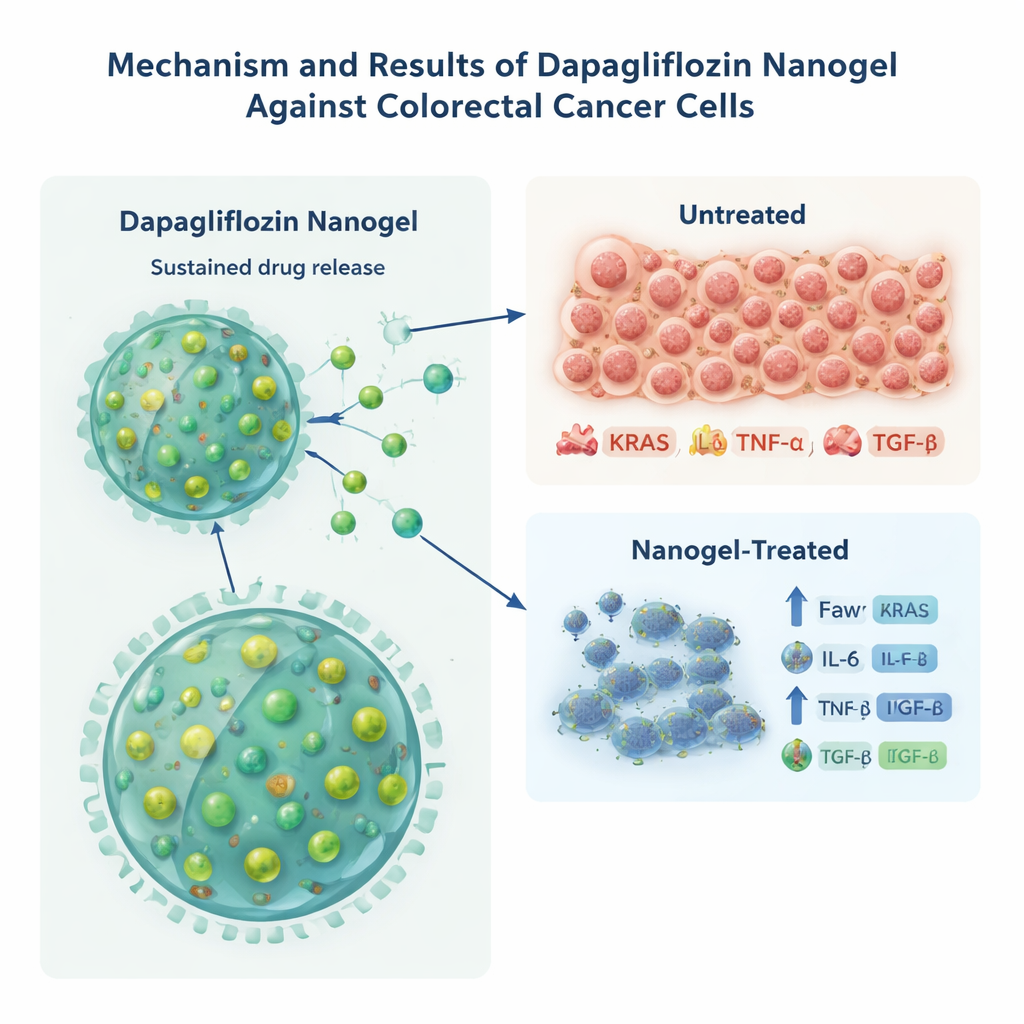
Laboratuvarda kanser hücrelerini strese sokmak
Bu yeni formdaki dapagliflozinin gerçekten kanser hücrelerine zarar verip vermediğini görmek için ekip, HCT-116 kolorektal kanser hücrelerinde test etti. Aynı miktardaki serbest ilaca kıyasla, nanojel versiyonu daha düşük konsantrasyonlarda kanser hücrelerini öldürdü ve hücre büyümesini yarıya indirmek için gereken dozu yaklaşık üçte bir azalttı. Araştırmacılar daha sonra KRAS (anahtar bir kanser sürücü proteini) ve IL-6, TNF-α ve TGF-β gibi kronik inflamasyon ve agresif tümör davranışıyla bağlantılı sinyal proteinleri dahil olmak üzere moleküllere baktılar. İlaç yüklü nanojelle muamele edilen hücreler, serbest ilaç veya boş partiküllerle muamele edilen hücrelere göre bu belirteçlerin tümünde çok daha düşük seviyeler gösterdi; bu da nanopartiküllerden sağlanan sürekli maruziyetin kanser ve inflamasyonla ilişkili sinyalleri daha etkili şekilde düşürdüğünü düşündürür. Hücre hattı zaten sabit bir KRAS mutasyonuna sahip olduğundan, yazarlar KRAS proteinindeki bu düşüşün doğrudan genetik düzelmeden ziyade stres yanıtlarını yansıtabileceği konusunda ihtiyatlı davranıyorlar, ancak bu yine de güçlü bir biyolojik etkiyi destekliyor.
Vücudun ilacı ele alışını değiştirmek
Ekip daha sonra hayvan çalışmalarına geçti ve sıçanlara ağız yoluyla ya basit bir dapagliflozin toz süspansiyonu ya da optimize edilmiş nanojel verdi; her ikisi de aynı dozdaydı. Nanojel grubunda, kanda zirve ilaç seviyeleri daha geç ortaya çıktı ve daha düşük oldu, ancak ilaç dolaşımda daha uzun süre kaldı. Toplam maruziyet (eğri altındaki alan olarak ölçülen) yaklaşık %7 oranında mütevazı bir artış gösterdi ve görünen yarı ömür yaklaşık iki katına çıktı. Bu değişiklikler, vücudun ilacı keskin bir zirve ve hızlı bir düşüş yerine zaman içinde daha pürüzsüz, daha geniş bir doz olarak görmesi anlamına geliyor. Bu davranış, araştırmacıların jeli tasarlarken amaçladığı ile uyumlu: ilacı bağırsakta tutmak, yavaşça salmak ve potansiyel olarak alt bağırsak ve tümörlerin ortaya çıktığı kolonu daha uzun süre daha yüksek düzeyde ilaçla yıkamak.
Gelecekteki kanser bakımına ne anlama gelebilir
Günlük ifadeyle, bu çalışma iyi bilinen bir diyabet ilacını, kolon tümörlerine daha iyi ulaşması ve orada kalması için yeni bir “dağıtım kıyafeti” ile donatıyor. Nanojel ilacı daha kolay çözünür hale getiriyor, bağırsaktan kaçışını yavaşlatıyor ve kolorektal kanser hücreleri üzerinde daha toksik görünürken önemli inflamasyon ve büyüme sinyallerini azaltıyor. Sıçanlarda, toplam dozu dramatik şekilde artırmadan ilacın kan dolaşımındaki varlığını nazikçe uzatıyor. Çalışma hâlâ erken aşamada—tek bir kanser hücre hattı ve kısa süreli hayvan testleriyle sınırlı—ve henüz canlı hayvanlarda veya insanlarda doğrudan tümör küçülmesi göstermedi. Yine de, dapagliflozinin gelecekteki kolorektal kanser tedavilerinin bir parçası olarak yeniden kullanılması için akıllı oral nanojeller kullanarak tanıdık bir hapı daha hedefe yönelik bir anti-kanser araca dönüştürme konusunda ayrıntılı bir temel sunuyor.
Atıf: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Anahtar kelimeler: kolorektal kanser, ilaç yeniden kullanımı, nanopartiküller, oral ilaç dağılımı, dapagliflozin