Clear Sky Science · tr
Prostat kanserinde radyoterapiyi takiben lökosit telomer kısalması: prospektif bir çalışma
Bu araştırma kanser sağ kalanları için neden önemli
İnsanlar kanserden sonra daha uzun yaşıyor, ancak birçok sağ kalan ‘‘hızlandırılmış’’ bir yaşlanma hissi yaşıyor—yorgunluk, güçsüzlük ve çok erken ortaya çıkan gibi görünen diğer kronik sorunlar. Bu çalışma basit ama önemli bir soruyu soruyor: prostat kanseri için uygulanan ışın tedavisi, kromozomlarımızdaki temel yaşlanma saatinde, yani telomerlerde kalıcı bir iz bırakıyor mu?
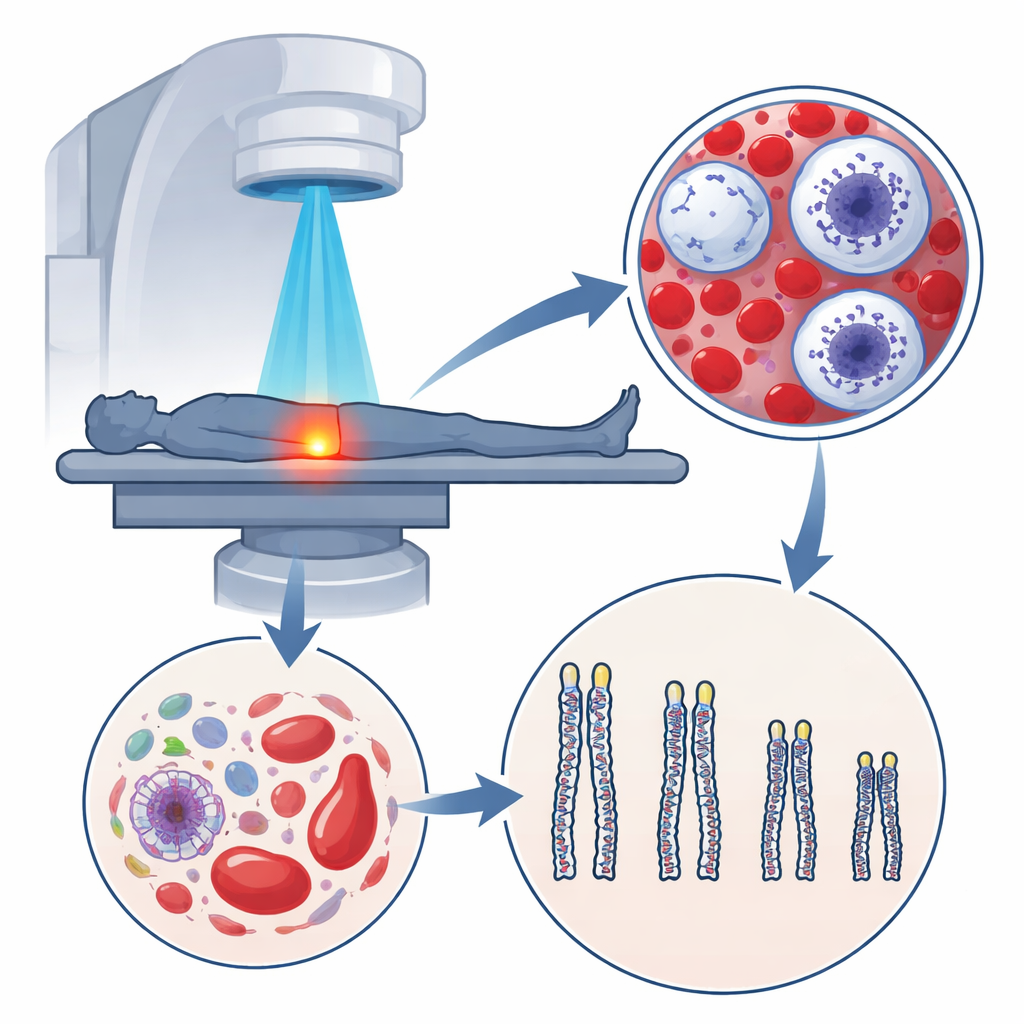
DNA’mızı koruyan küçük kapakçıklar
Kromozomlarımızın uçlarında telomerler bulunur; iplik uçlarındaki plastik koruyucular gibi genetik materyalin dağılmasını önleyen küçük DNA dizileridir. Hücre her bölündüğünde bu kapakçıklar biraz kısalır. Çok kısa olduklarında hücre kapanma durumuna girer ya da ölür; bu süreç doğal yaşlanmayla ilişkilidir. Beyaz kan hücreleri kanla kolayca örneklenebildiği ve birçok dokuda olanları yansıttığı için, bunların telomer uzunluğu sıklıkla yaşadığımız yıl sayısından farklı olabilen ‘‘biyolojik yaş’’ için bir gösterge olarak kullanılır.
Tedavi sırasında ve sonrasında daha yakından bakmak
Modern prostat radyoterapisinin bu yaşlanma ölçütünü nasıl etkileyebileceğini görmek için araştırmacılar, tek bir merkezde kür amaçlı ışın tedavisi alan 65 yaş ve üzeri 314 erkeği izledi. Kan örnekleri dört kez alındı: tedavi öncesinde, birkaç haftalık radyoterapi kürünün sonunda ve sonra 3 ve 15 ay sonra. Her örnekte ekip, beyaz kan hücrelerindeki ortalama göreli telomer uzunluğunu hassas bir DNA testiyle ölçtü. Bu tasarım, farklı insanların tek bir anda karşılaştırılmasındansa her erkeğin telomerlerinin zaman içindeki değişimini izlemeye imkân verdi.
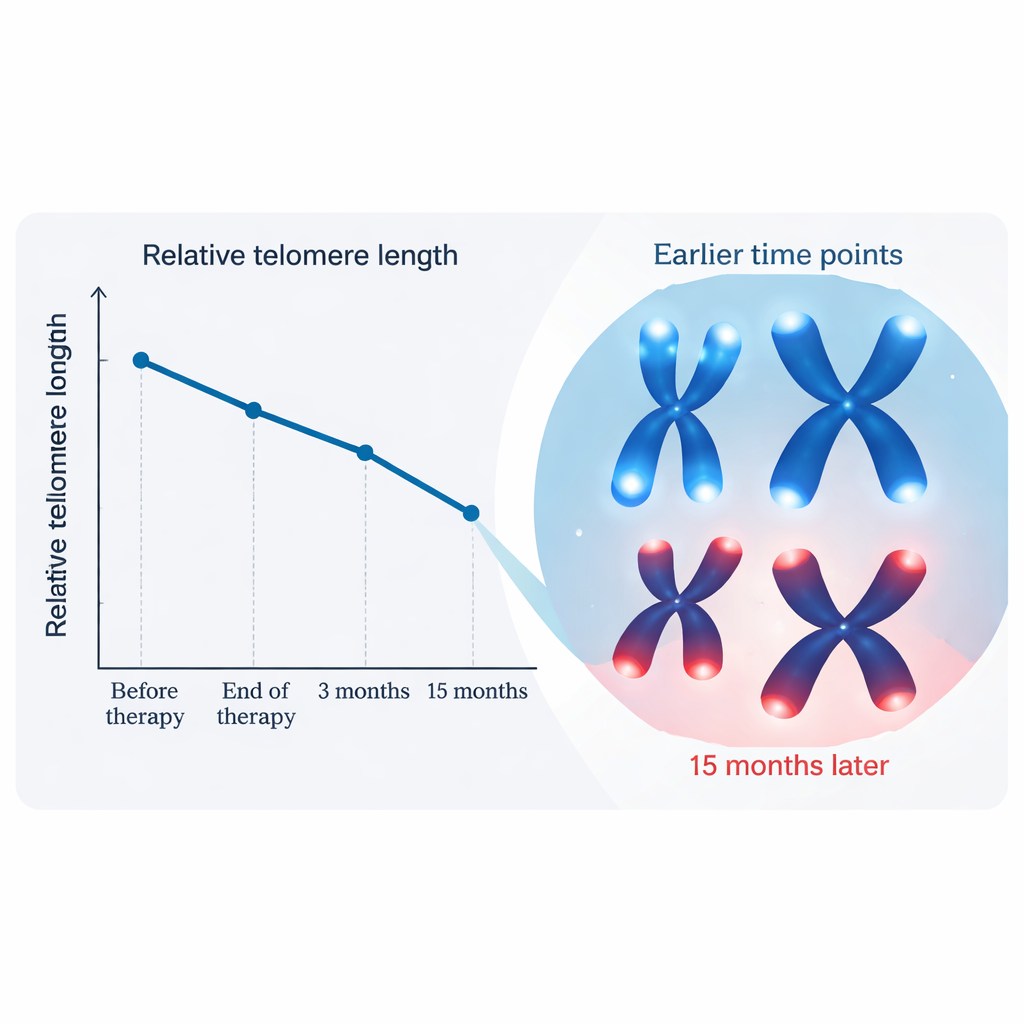
Telomerlerde zaman içinde ne oldu
Telomer uzunluğu tedavi öncesinden radyoterapinin sonuna ve 3 aylık kontrolde büyük ölçüde benzer kaldı; istatistiksel açıdan anlamlı olmayan küçük dalgalanmalar vardı. Çarpıcı değişiklik 15 aylık dönemde ortaya çıktı: ortalama olarak telomerler başlangıca göre yaklaşık %15 daha kısaydı; bu, yaşlı yetişkinlerde yalnızca biraz fazla bir yılda normal yaşlanmayla beklenenden çok daha büyük bir düşüştü. Bu desen, radyasyonun kan üzerindeki uzun dönem biyolojik etkisinin yavaşça, görünür yan etkiler geçtikten sonra ortaya çıkabileceğini düşündürüyor. Araştırmacılar ayrıca yaş, yüksek tansiyon, sigara, tedavi ayrıntıları veya yakın lenf düğümlerine verilen ışın gibi faktörlerin bu değişiklikleri etkileyip etkilemediğini inceledi. Yaş ve yüksek tansiyon kısalmayla mütevazı ilişkiler gösterirken, çoğu tedavi varyasyonu bu grupta sonucu açıkça değiştirmedi.
Radyasyon hüresel aşınmayı nasıl hızlandırabilir
Yerel bir prostat ışın tedavisi dolaşımdaki kan hücrelerindeki telomerleri neden etkilesin? Yazarlar iki bağlantılı sürece işaret ediyor. Birincisi, iyonize radyasyon DNA’ya zarar verebilen reaktif oksijen molekülleri üretir ve telomerler bu tür hasara özellikle hassastır ve diğer bölgelere göre daha az verimli onarılır. İkincisi, radyoterapi vücutta kalıcı bir iltihabi reaksiyon tetikleyebilir; bu da beyaz kan hücrelerinin daha sık bölünmesine ve daha fazla zararlı oksijen yan ürününün salınmasına yol açar. Her iki mekanizma da telomerlerin kademeli aşınmasını hızlandırabilir ve hücreleri bölünmeyi bırakan ama çevre dokuları etkilemeye devam eden geri döndürülemez bir ‘‘yaşlı’’ durum olan senesense doğru itebilir.
Bu hastalar için ne anlama gelebilir
Bu çalışmadaki erkekler için prostat radyoterapisi küratif bir tedavi olmaya devam etti, ancak tedaviden bir yıl sonra kan hücrelerinde daha hızlı biyolojik yaşlanma belirtileriyle de ilişkilendirildi. Daha kısa telomerler tek başına bir kişinin güçsüz veya hasta olacağını kanıtlamaz; yine de kalp hastalığı, diyabet ve bilişsel gerileme gibi yaşa bağlı sorunların daha yüksek riski ile bağlantılıdır. Bulgular, başarılı kanser tedavisinin gizli uzun dönem maliyetler taşıyabileceğini vurguluyor ve sadece tümör kontrolünü değil, yaşlanmayla ilişkili sağlığı da dikkate alan takip bakımına olan gereksinimi öne çıkarıyor. Yazarlar, bu sonuçları doğrulamak ve iltihaplanma veya oksidatif stresi hedefleyen koruyucu yaklaşımlar gibi hastaların tedavi sonrası biyolojik direncini korumaya yardımcı olabilecek yöntemleri test etmek için daha büyük, daha uzun süreli çalışmaların—radyasyonla tedavi edilmeyen kişilerle karşılaştırmaları da içerecek şekilde—gerekli olduğunu savunuyor.
Atıf: Langsenlehner, T., Paal, K., Thurner, E.M. et al. Leukocyte telomere attrition following radiotherapy in prostate cancer: a prospective study. Sci Rep 16, 5905 (2026). https://doi.org/10.1038/s41598-026-36205-x
Anahtar kelimeler: prostat kanseri, radyoterapi, telomerler, biyolojik yaşlanma, hücresel senesens