Clear Sky Science · tr
Fluoro kinolon iskeletlerinde R5 ve R7 pozisyonları F-aktin filament parçalanmasını yönlendirir
Antibiyotikleri Beyin Yardımcılarına Dönüştürmek
Alzheimer’dan Parkinson’a kadar pek çok yaygın beyin bozukluğunun ortak, gizli bir faili var: sinir hücreleri içindeki küçük yapısal çubukların zamanla sıkışıp sertleşmesi. Bu çubuklar normalde hücrenin iç iskelesinin esnek bir parçası olan aktin adlı bir proteinden oluşur. Bu çalışma, beklenmedik bir olasılığı araştırıyor—iyi bilinen bir antibiyotik sınıfı olan fluoro kinolonların, zararlı aktin demetlerini nazikçe parçalayacak ve potansiyel olarak beyni korumaya yardımcı olacak şekilde yeniden tasarlanabileceği.
Hücre İskelesi Yanlış Gittiğinde
Sağlıklı beyin hücreleri, iç iskeletlerini sürekli olarak yeniden şekillendirerek bağlantılar oluşturur ve yeniden düzenler. Aktin filamentleri bu sürecin merkezindedir; gerektiğinde oluşur ve çözülürler. Ancak stres altında aktin, hücreyi tıkayan, hayati yük taşınmasını bozan ve amiloid ve tau gibi hastalıkla ilişkilendirilen proteinlerin birikimini teşvik eden inatçı çubuk benzeri agregatlara kilitlenebilir. Yıllar içinde bu çubuklar Hirano cisimcikleri olarak bilinen yoğun yapılara olgunlaşabilir; bunlar birçok nörodejeneratif durumda hastaların beyinlerinde sık görülür. Mevcut aktin hedefli ilaçlar genellikle son derece toksik olduğundan, araştırmacılar hücrelere zarar vermeden bu agregatları gevşetebilecek daha güvenli küçük moleküller bulmaya heveslidir.
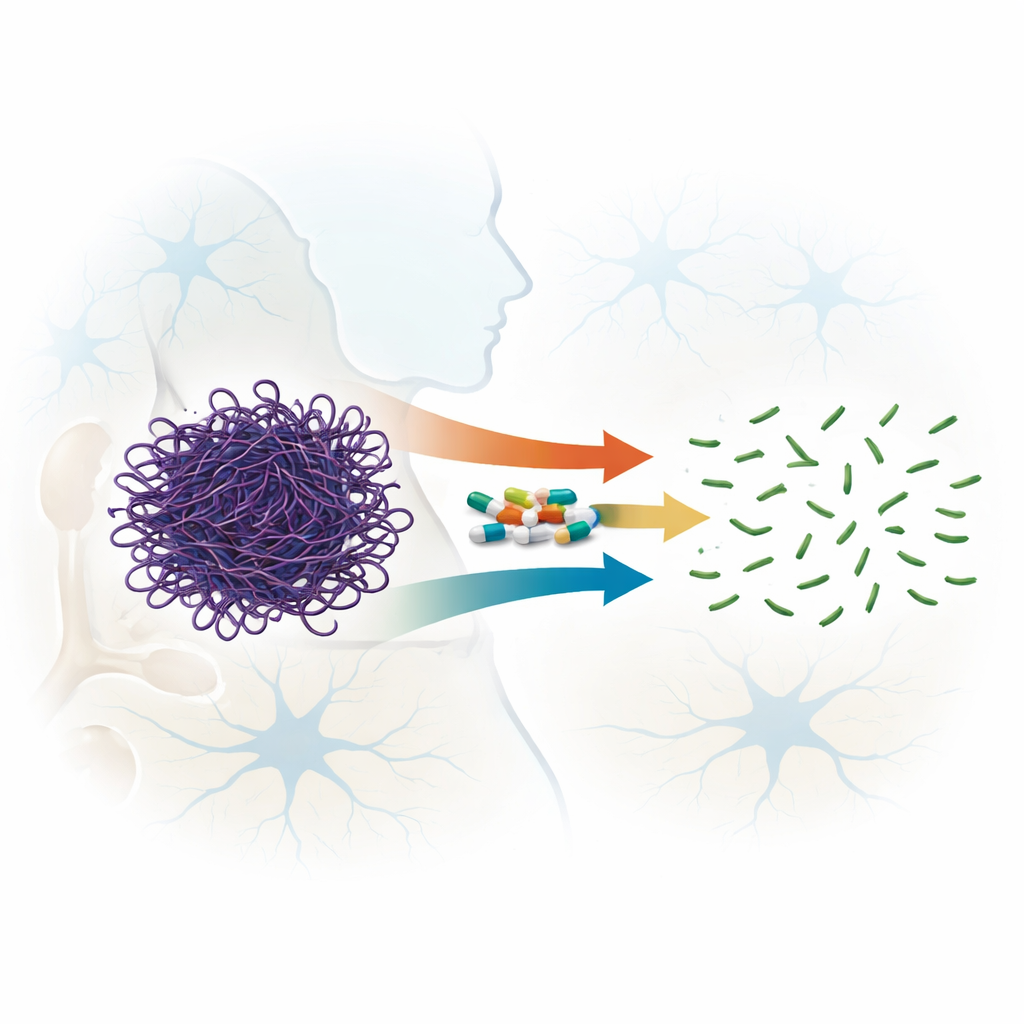
Tanıdık İlaçların Beklenmedik Bir Yeteneği
Fluoro kinolonlar, enfeksiyonları tedavi etmek için dünya çapında kullanılan geniş spektrumlu antibiyotiklerdir ve bu aileden bazı yeni üyeler kan–beyin bariyerini geçebilir. Önceki ipuçları, belirli fluoro kinolonların aktin filamentlerini kararsızlaştırabileceğini öne sürmüştü. Bu çalışmada yazarlar, ilacın oluşumu önlemekten ziyade önceden oluşmuş aktin filamentlerini ne kadar iyi parçaladıklarını görmek için dördüncü nesle kadar uzanan yedi ilişkili bileşiği sistematik olarak karşılaştırdı. Işık saçılımı ölçümleri, elektron mikroskobu ve jel filtrasyonunu kullanarak, test edilen tüm ilaçların aktin filamentlerini bozabildiğini ancak güçlerinin çok farklı olduğunu gösterdiler. İki ilaç—sparfloksasin (üçüncü nesil) ve moksifloksasin (dördüncü nesil)—göreceli olarak düşük ilaç-protein oranlarında bile uzun filamentleri hızla ve geri döndürülemez şekilde çok daha küçük parçalara böldü.
Filamentlerin Parçalanışını Görmek
Yüksek çözünürlüklü görüntüleme ve biyofiziksel testler, filamentlerin ilaç tedavisi altında nasıl değiştiğini ortaya koydu. Elektron mikroskobu, tedavi edilmemiş aktinin uzun, kesintisiz iplikler oluşturduğunu; etkili fluoro kinolonların ise bunları kısa, dağılmış fragmanlara dönüştürdüğünü gösterdi. Daha az potente sahip üyeler, filamentlerde bükülme ve kıvrılma üretti ancak bunları tamamen kırmadı. Proteinin kararlılığını ölçen ısı temelli testler bu fiziksel parçalanmayı doğruladı: tedavi edildikten sonra aktin, daha düşük erime sıcaklıklarıyla serbest, toplanmamış formuna daha çok benzedü; ancak temel yapı taşı neredeyse değişmeden kaldı. Bu, ilaçların aktini açıp zarar vermediğini—daha çok birimlerin filamentlerde birbirine nasıl tutunduğunu söküp ayırdığını düşündürür.
Moleküler Tutmayı Yakından İncelemek
Neden bazı fluoro kinolonların diğerlerinden daha iyi çalıştığını anlamak için ekip gelişmiş nükleer manyetik rezonans deneylerini ilaç–protein etkileşimlerinin bilgisayar simülasyonlarıyla birleştirdi. Tüm bileşiklerin aktinle temas kurmak için paylaşılan halka biçimli bir “çekirdeğe” dayandığını ve özellikle filament üzerinde yineleyen iki pozisyonla temas ettiğini buldular. Ancak R5 ve R7 olarak adlandırılan belirli noktalara eklenen kimyasal gruplar, her molekülün ne kadar sıkı ve nerede bağlanacağını güçlü biçimde etkiliyordu. En etkili parçalayıcılarda bu pozisyonlarda bir amino grubu ve komşu aktin iplikleri arasındaki arayüzde küçük bir cebe uzanan hacimli halka sistemleri bulunuyordu. Orada, filamentleri bir arada tutmaya yardımcı olan önemli bir tuz köprüsü de dahil olmak üzere kritik stabilize edici etkileşimlere müdahale ediyorlardı.
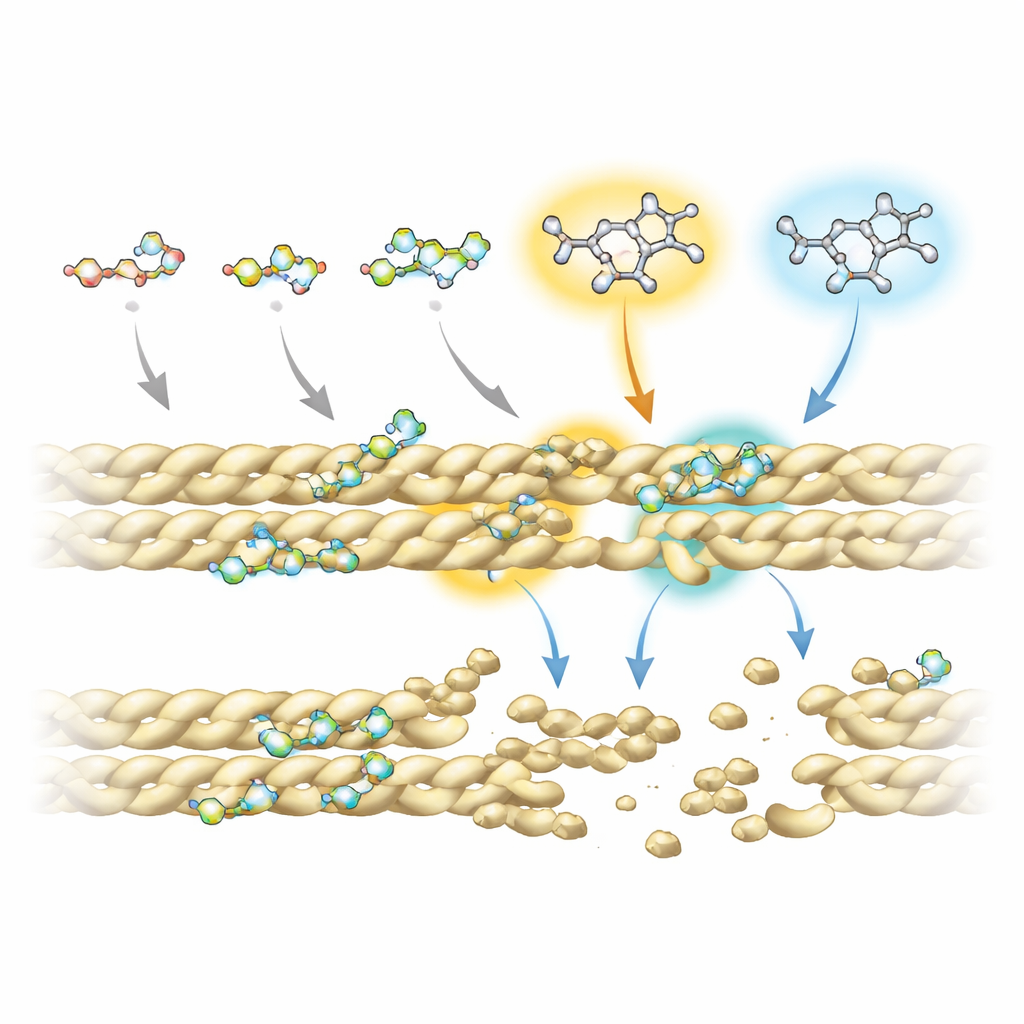
Maya Hücrelerinden Gelecek Terapilere
Araştırmacılar ayrıca doğal olarak aktin demetleri biriktiren bir maya suşunda ilaçları test etti; bu model, hasta hücrelerin bazı yönlerini taklit ediyor. Mikroskopta, tedavi edilmeyen mayalarda büyük, parlak aktin kümeleri görülürken; fluoro kinolonlara maruz kalan hücrelerde—özellikle sparfloksasin, moksifloksasin ve daha yüksek dozlarda nalidiksik asitte—daha dağınık, noktasal desenler gözlendi; bu, demetlerin parçalandığını gösteriyordu. Önemli olarak, ilaçların etkisi nispeten nazik görünüyordu: filament paketlemesini zayıflatıyor ancak aktinin temel şeklini ciddi şekilde bozmayıp, bağlanmaları klasik aktin toksinlerine göre daha zayıftı; bu da şiddetli yan etki riskini azaltabilir.
Daha Akıllıca Aktin Hedefli İlaçlar Tasarlamak
Genel olarak bu çalışma, iyi bilinen antibiyotiklerde yapılan küçük değişikliklerin hücrenin iç iskelesiyle nasıl etkileştiklerini dramatik şekilde değiştirebileceğini gösteriyor. R5 ve R7 pozisyonlarını hem aktin parçalanması hem de beyin penetrasyonu için ana “kontrol düğmeleri” olarak tanımlayarak yazarlar, zararlı aktin agregatlarını seçici olarak dağıtan yeni fluoro kinolon esinli moleküller yaratmak için bir taslak ortaya koyuyor. Bu bulgular laboratuvar düzeyinde erken bir ilke kanıtı olmakla birlikte, tanıdık antibiyotiklerden türetilen gelecekteki ilaçların sinir hücrelerindeki toksik iskeleti temizlemeye ve bazı nörodejenerasyon türlerini yavaşlatmaya ya da önlemeye yardımcı olma olasılığını gündeme getiriyor.
Atıf: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Anahtar kelimeler: aktin agregatları, fluoro kinolon antibiyotikleri, nörodejeneratif hastalık, ilaç yeniden kullanımı, sitokelet