Clear Sky Science · tr
Grafiklerde kendi kendine denetimli öğrenme, kodlamayan RNA ve hastalık ilişkilerini tahmin ediyor
Gizli RNA’lar sağlığımız için neden önemli
Çoğumuz RNA’nın temel görevinin protein üretimine yardımcı olmak olduğunu öğrenmiştik. Ancak son on yılda bilim insanları, proteine dönüşmeyen ama hücre işleyişini hâlâ kontrol eden çok sayıda “kodlamayan” RNA keşfettiler. Bu moleküllerin birçoğunun kanserleri ve diğer karmaşık hastalıkları tetiklediği veya baskıladığı artık biliniyor. Hangi kodlamayan RNA’ların hangi hastalıklarla ilişkili olduğunu belirlemek, hastalığı erken teşhis etmenin veya daha hedefli tedaviler tasarlamanın yeni yollarını açabilir—ama laboratuvarda her olasılığı test etmek imkânsız derecede yavaş olurdu. Bu çalışma, devasa biyolojik ağları tarayıp araştırmacıların deneylerde incelemesi için en umut verici RNA–hastalık bağlantılarını güvenilir biçimde öneren güçlü bir bilgisayar tabanlı yöntem sunuyor.
Çöplükten hücrenin kilit oyuncularına
Yıllarca kodlamayan RNA’lar, gen etkinliğinin anlamlı olmayan artıkları olarak reddedildi. Artık mikroRNA’lar, uzun kodlamayan RNA’lar ve dairesel RNA’lar gibi ailelerin DNA paketlenmesinden genlerin açılıp kapanmasına ve hücre içi sinyal iletimine kadar hayati süreçleri düzenlemeye yardımcı olduğunu biliyoruz. Bu RNA’lar birçok kontrol noktasında yer aldığından, küçük değişiklikler bile dengeyi kansere veya diğer hastalıklara doğru kaydırabilir. Klinik uzmanlar bunları potansiyel biyobelirteçler ve ilaç hedefleri olarak görmeye başladı. Sorun ölçek: binlerce farklı RNA ve yüzlerce hastalık var; her olası bağlantıyı test eden geleneksel deneyler pahalı ve zaman alıcı. İşte burada hesaplamalı tahmin devreye giriyor ve arama alanını daraltmanın bir yolunu sunuyor.
Bir biyolojik ağı nasıl okumalı
Önceki bilgisayar yöntemleri, RNA–hastalık bağlantılarını büyük veri tablolarını daha basit parçalara bölerek veya bilinen örnekler üzerinde makine öğrenmesi modelleri eğiterek tahmin etmeye çalıştı. Bu yaklaşımlar yardımcı oldu ancak genellikle RNA’ların ve hastalıkların ağlar halinde nasıl örüldüğünü göz ardı etti. Modern “graf sinir ağları” RNA’ları ve hastalıkları, bir sosyal ağ gibi düğümler ve bunları birleştiren bağlantılar olarak ele alır. Kim kiminle bağlıysa bunun kalıplarını öğrenebilirler. Bununla birlikte, bu grafik yöntemlerinin çoğu çok sayıda güvenilir eğitim örneğine ve özenle hazırlanmış giriş özelliklerine ihtiyaç duyar. Bu durum eksik verilere, gürültülü ölçümlere ve aşırı uyuma karşı hassas olmalarına—bilinen verilerde iyi performans gösterip yeni ilişkileri tahmin etmeye çalışıldığında başarısız olmalarına—neden olur.
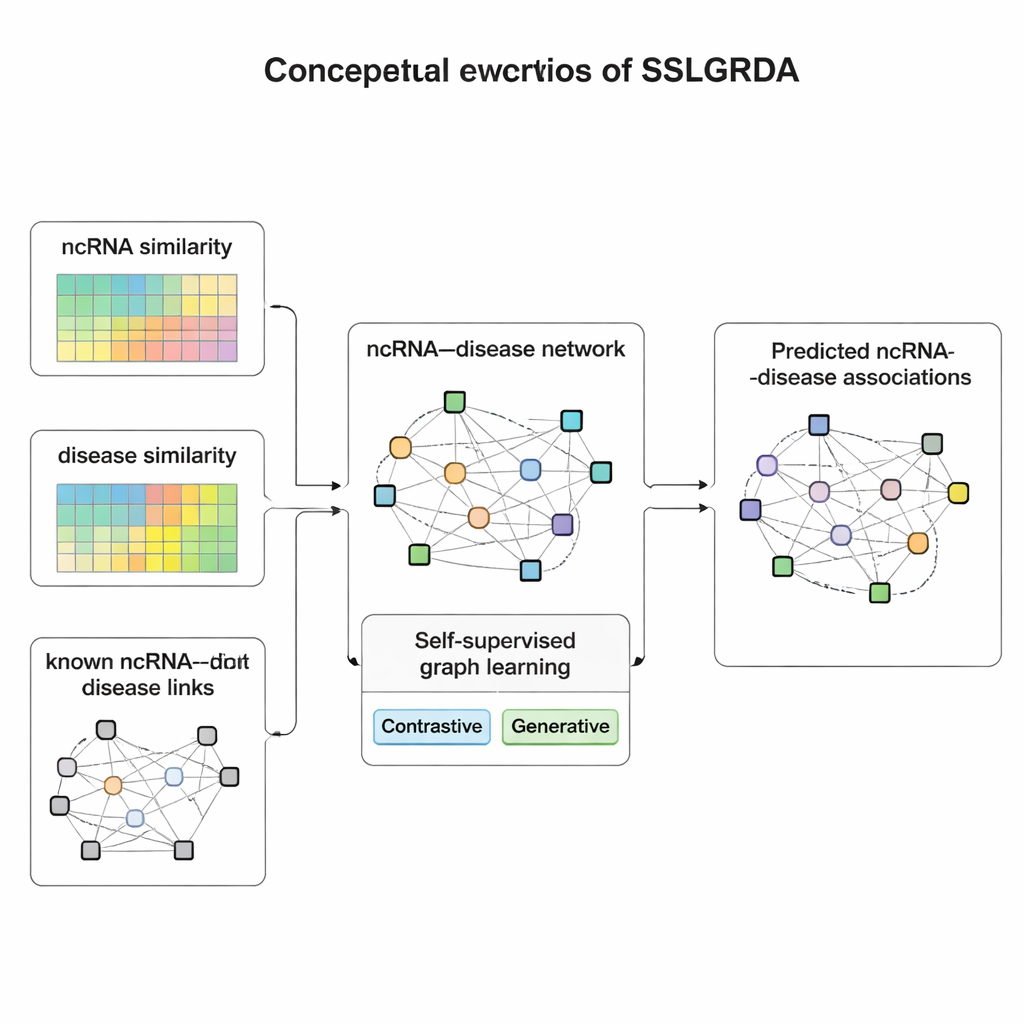
Verinin kendisinden öğrenmek
Yazarlar, etiketli eğitim verisine fazla dayanmak zorunda kalmadan bir grafik modelinin faydalı kalıpları öğrenmesini sağlayan yeni bir çerçeve olan SSLGRDA’yı sunuyor. Temel fikir “kendi kendine denetimli öğrenme”: modele hangi RNA’nın hangi hastalıkla eşleştiği söylenmek yerine, model yalnızca ağın yapısı ve özniteliklerine dayanarak kendi alıştırma görevlerini uydurur. Araştırmacılar iki tür grafik oluşturuyor. Biri RNA’ları ve hastalıkları farklı düğüm türleri olarak tutar ve bilinen bağlantılarla birleştirir. Diğeri, iki RNA veya iki hastalığın ne kadar benzer olduğunu gösteren benzerlik bilgisini de içeren tek bir büyük ağda bunları harmanlar—böylece seyrek bağlı öğeler bile destekleyici komşular kazanır. Bu grafiklerin üzerinde SSLGRDA iki tarz kendi kendine eğitimi kullanır. Kontrastif stratejiler, modelden aynı düğümün farklı “görünümlerinin” (örneğin bağlantıları ile öznitelikleri) benzer iç temsilere yol açması gerektiğini tanımayı, ilişkisi olmayan düğümleri ise net biçimde ayırmayı ister. Üretici stratejiler ise kasıtlı olarak giriş özelliklerinin parçalarını gizleyip modelin bunları yeniden inşa etmesini zorlayarak, modelin gürültüyü ezberlemek yerine daha derin yapıları yakalamasını teşvik eder.
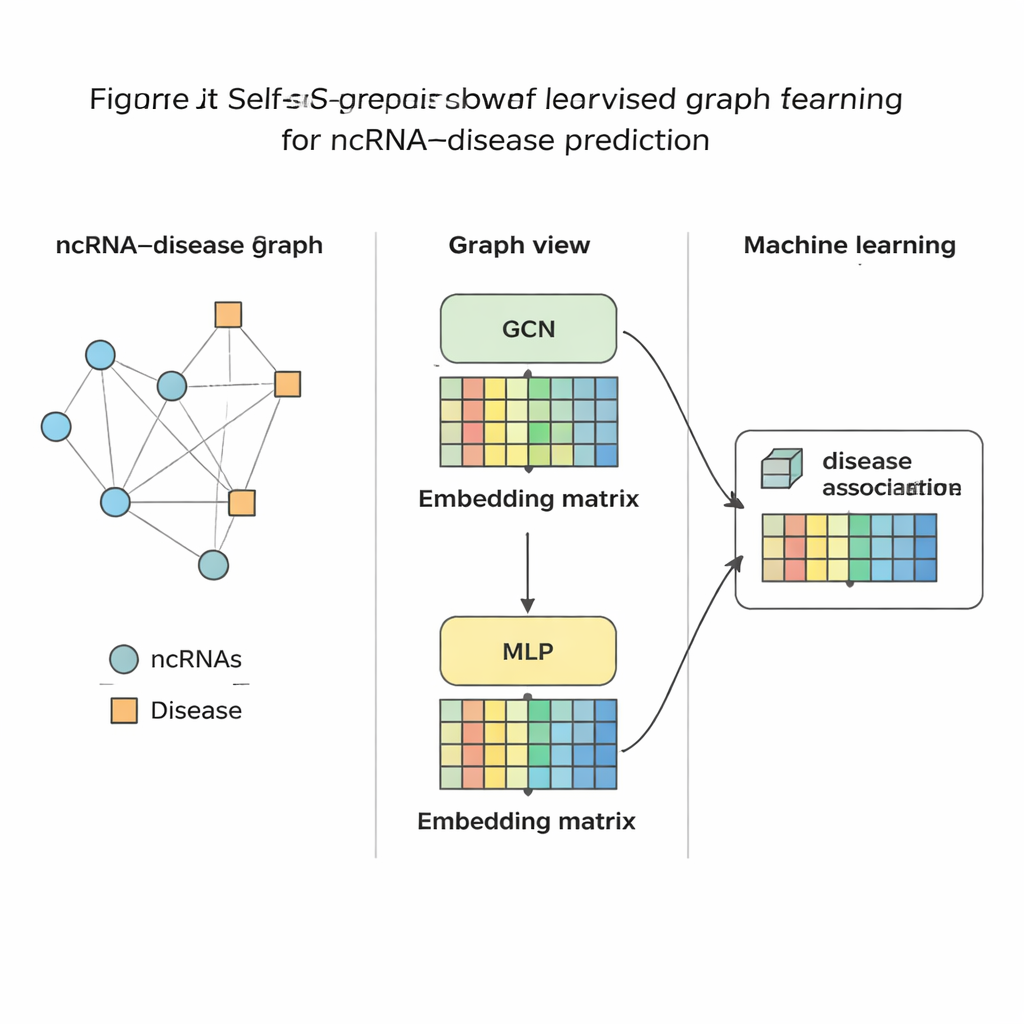
Yöntemi teste koymak
SSLGRDA her RNA ve hastalığı sıkıştırılmış sayısal bir parmak izine dönüştürdükten sonra, bu ikisi arasındaki bir bağlantının olası olup olmadığını değerlendirmek için standart bir makine öğrenmesi sınıflandırıcısı eğitilir. Yazarlar bu yaklaşımı üç ana RNA türünü ve yüzlerce hastalığı kapsayan dokuz farklı veri kümesinde değerlendirdi. Genel olarak, harmanlanmış (homojen) grafikteki kontrastif kendi kendine denetimli varyantları en iyi performansı gösterdi ve güçlü grafik tabanlı temel yöntemler dahil bir dizi mevcut aracı geride bıraktı. Yöntem yalnızca küresel testlerde daha yüksek doğruluk elde etmekle kalmadı, aynı zamanda tek bir RNA’ya veya tek bir hastalığa odaklandıklarında doğru eşleri üst sıralara yerleştirdi ki bu, bir biyoloğun tek bir kanser türünden başlayıp hangi RNA’ları incelemesi gerektiğini sorduğu gerçek dünya kullanımı için hayati önem taşır. Aynı fikirlerin mikroplar ile hastalıklar veya ilaçları birbirine bağlayan diğer biyomedikal ağlara da iyi aktarılabildiğini gösterdiler.
Tahminlerden potansiyel terapilere
Pratik değeri göstermek için ekip, SSLGRDA’yı meme kanseri, kolon kanseri ve birkaç diğer durumda rol alabilecek yeni kodlamayan RNA’ları aramak için uyguladı. En yüksek sıralamadaki önerilerin birçoğu daha sonra bağımsız veritabanlarında veya bilimsel raporlarda doğrulandı; bu da modelin biyolojik açıdan anlamlı kalıpları tespit etme yeteneğini destekliyor. Uzman olmayanlar için çıkarım şudur: bu çalışma, sürekli büyüyen biyolojik veri ağı içindeki gizli hastalık ipuçlarını kazımanın daha akıllı bir yolunu sunuyor. RNA’ların ve hastalıkların nasıl kümelendiğini ve etkileştiğini otomatik olarak öğrenen kendi kendine denetimli grafik yöntemleri, laboratuvar araştırmacılarını en umut verici hedeflere yönlendirerek ham veriden daha iyi tanı ve tedavilere giden yolu hızlandırabilir.
Atıf: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
Anahtar kelimeler: kodlamayan RNA, hastalık ilişkilendirmesi, graf sinir ağları, kendi kendine denetimli öğrenme, hesaplamalı biyoloji