Clear Sky Science · tr
Bir bakteri proteomunda moleküler sıkışıklığın protein kararlılığı üzerine etkileri
Proteinlerin kalabalık yaşamı neden önemli
Her canlı hücre içinde proteinler, neredeyse hacmin yarısını doldurabilecek kadar diğer moleküllerle dolu bir ortamda işlev görür. Oysa çoğu laboratuvar deneyi proteinleri seyreltilmiş, neredeyse boş çözeltilerde inceler. Bu makale basit ama önemli bir soruyu soruyor: bu kalabalık gerçeklik proteinlerin kararlılığını ve davranışını nasıl değiştiriyor ve bu moleküler ölçekte yaşamın nasıl işlediği açısından ne anlama geliyor?
Dolu bir hücresel dünyaya bakış
Bunu keşfetmek için araştırmacılar Cupriavidus necator adlı bir bakteriyle çalıştı; karbon yakalama ve biyoplastik üretimi gibi yeşil teknolojiler açısından ilgi çeken bir mikroorganizma. Hücreleri nazikçe parçalayarak yüzlerce farklı proteinin doğal formlarına yakın kalmasını sağladılar. Ardından hücre içinin yoğun yapısını taklit etmek için sıkça kullanılan büyük, suyu seven polimerlerden—PEG, dekstran ve Ficoll gibi—yüksek konsantrasyonlarda “sıkıştırıcı” maddeler eklediler.
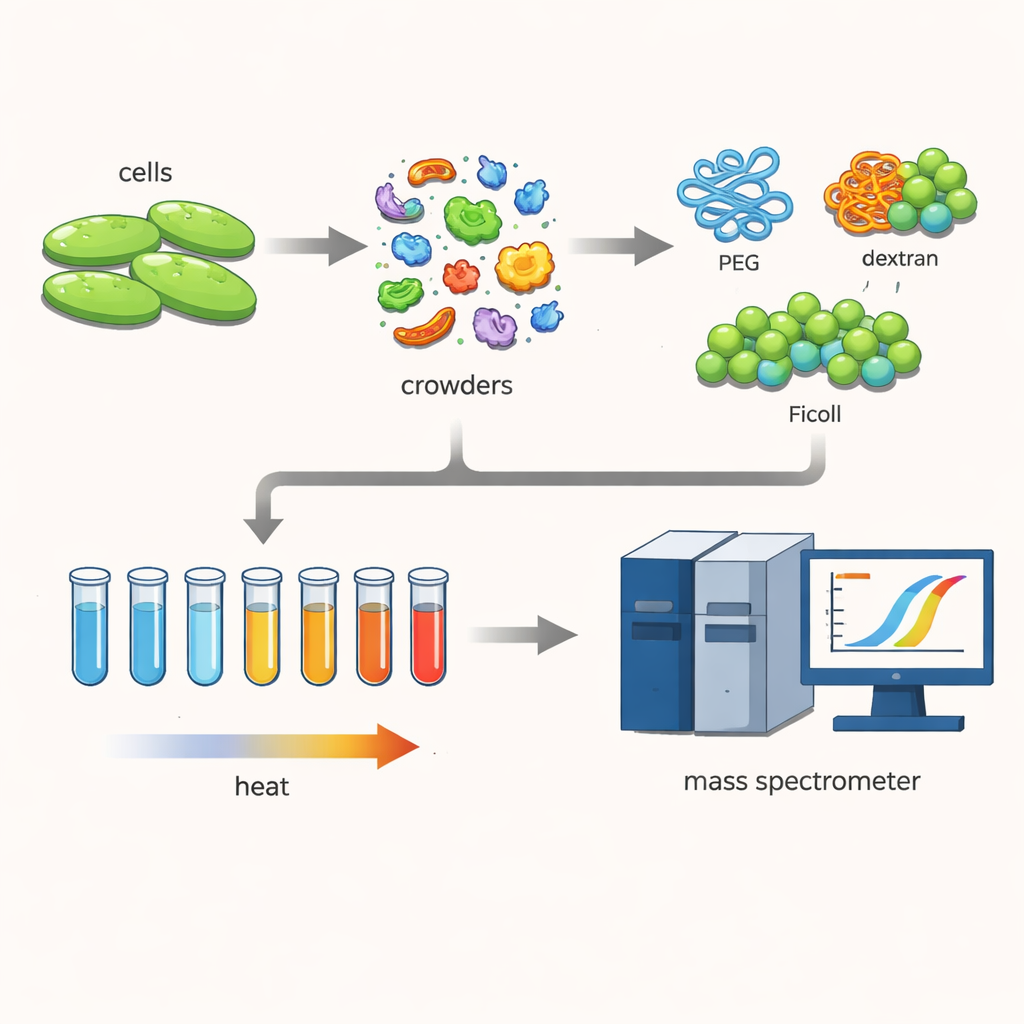
Proteinlerin erimesini izlemek
Ekip termal proteom profilleme adlı bir teknik kullandı. Protein karışımının çok sayıda küçük örneğini 30 ile 70 C arasında kademeli olarak ısıttılar. Sıcaklık yükseldikçe, daha az kararlı proteinler açılıp kümelenerek çözeltiden ayrıldı. Geriye kalan çözünür proteinleri etiketleyip hassas bir kütle spektrometresiyle ölçerek her protein için erime eğrilerini yeniden oluşturabildiler ve erime sıcaklığını—yarısının çözünür, işlevsel halini terk ettiği noktayı—belirlediler. Bu sıcaklıkları sıkıştırıcılar varken ve yokken karşılaştırmak, kalabalık ortamın protein kararlılığını nasıl kaydırdığını ortaya koydu.
Karışık bir tablo: bazı proteinler daha sağlam, bazıları daha hassas
Genel olarak, altı polimer sıkıştırıcının herhangi birinin eklenmesi bakteriyel proteomda erime sıcaklıklarını düşürdü; bu da hafif bir genel destabilize edici etkiye işaret ediyor. Ancak bu küresel eğilim çok daha nüanslı bir hikâyeyi gizliyordu. Onlarca bireysel protein için sıkıştırıcılar kararlılığı ya belirgin biçimde artırdı ya da azalttı, bazen birkaç dereceye varan değişikliklerle. Çoğu protein yalnızca bu altı reaktiften birine yanıt verirken, küçük bir grup birkaçına tepki verdi; ve bunların neredeyse tamamı ya tutarlı şekilde stabilize oldu ya da tutarlı şekilde destabilize oldu, bu da onların sıkıştırıcılarla nasıl etkileştiğine dair ortak özelliklerin varlığına işaret ediyor.
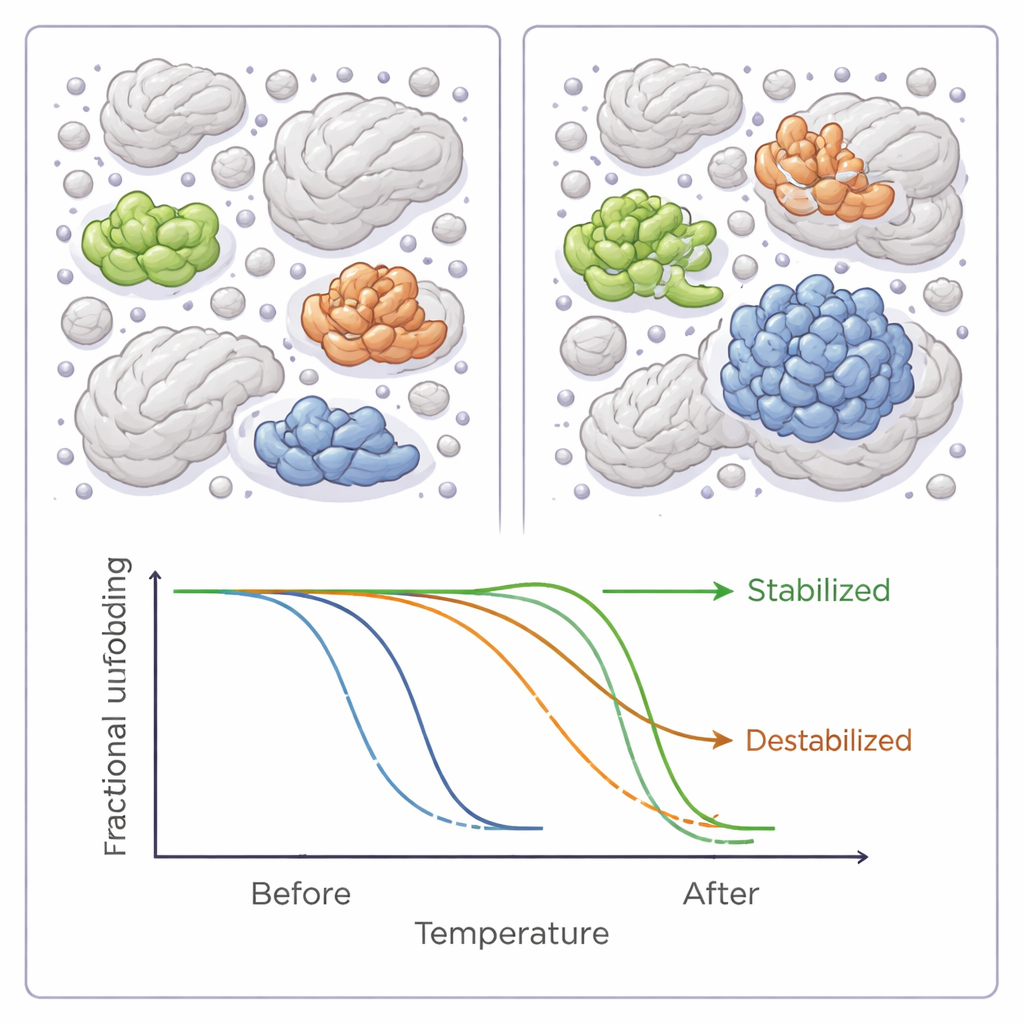
Bir proteini kalabalıkta kazanan veya kaybeden yapan nedir
Yazarlar bu hassas proteinlerin özelliklerini daha yakından incelediklerinde örüntüler ortaya çıktı. Kalabalık koşullarda daha stabil hale gelen proteinler genellikle daha hidrofobikti—yani suyu iten yüzeylere daha çok sahipti—ve iyi tanımlanmış aktif bölgeleri olan klasik enzimler olma eğilimindeydi. Ayrıca protein‑protein etkileşimlerine daha sık karışıyor veya işlevlerini ayarlayan kimyasal modifikasyonlar taşıyorlardı. Buna karşılık destabilize olan proteinler ortalama olarak daha küçük ve bu tür modifikasyonlarla daha az süslenmişti. Bu bulgular, sıkışıklığın boyut, şekil ve normalde ortaklarıyla nasıl etkileştiklerine bağlı olarak bazı proteinleri destekleyip diğerlerini daha hassas hale getirebileceğini öne süren bilgisayar modelleri ve diğer deneylerle uyumlu.
Basit sıkıştırmanın ötesinde: sıkıştırıcılar gerçekten nasıl çalışıyor
Moleküler sıkışıklık için geleneksel açıklamalar “hariç bırakılmış hacim”a odaklanır; büyük moleküller daha az yer bırakarak proteinleri katlanmış halde tutmaya zorlar. Eğer işin tamamı buysa, sıkıştırıcı maddelerin genellikle proteinleri stabilize etmesi ve polimerlerin hacimli ya da viskoz oluşuyla güçlü bağlantılar görülmesi beklenirdi. Bunun yerine yazarlar polimerlerin boyutu ve yoğunluğuyla yalnızca zayıf bağlantılar gözledi. Verileri daha iyi uyum gösterdiği model “tercihli dışlama” fikrine uyar: sıkıştırıcılar ve proteinler kimyasal olarak birbirinden kaçınır, bu da dolaylı olarak bazı katlanmış durumları destekler ama diğer proteinleri kararlı tutan hassas etkileşimleri bozabilir. Kısacası, protein davranışını şekillendiren sadece fiziksel sıkıştırma değil, ince kimyasal itme‑çekme etkileşimleridir.
Bu, yaşamın kimyasını anlamak açısından ne anlama geliyor
Uzman olmayanlar için ana mesaj şudur: hücre içindeki proteinler net bir tampon içinde izole halde incelenerek tam olarak anlaşılmaz. Etraflarındaki yoğun moleküler orman bazı proteinleri daha sağlam, bazılarını daha kırılgan hale getirerek tüm reaksiyon ağlarının nasıl davrandığını değiştirebilir. Bu çalışma yüzlerce proteinin aynı anda kararlılık değişikliklerini ölçerek gösteriyor ki sıkışıklık etkileri karmaşık ve proteine özgü; ve muhtemelen basit paketlemenin yanı sıra doğrudan etkileşimlerle de yönlendiriliyor. Araştırmacılar ilaç, endüstriyel enzimler veya tasarlanmış mikroplar geliştirirken bu kalabalık gerçeğini göz önünde bulundurmak, proteinlerin canlı sistemlerde gerçekten nasıl davrandığını tahmin etmek için kritik olacaktır.
Atıf: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Anahtar kelimeler: moleküler sıkışıklık, protein kararlılığı, termal proteom profillemesi, bakteriyel proteom, hücresel ortam