Clear Sky Science · tr
Entegre tek hücre ve makine öğrenimi çerçevesi, prognostik fibroblast alt tiplerini ortaya çıkarıyor ve akciğer adenokarsinomunda fibroblast ilişkili risk imzası oluşturuyor
Neden akciğer tümörlerinin etrafındaki “yardımcı” hücreler önemli
Akciğer adenokarsinomu, en yaygın ve ölümcül akciğer kanseri türlerinden biridir; yine de görünüşte benzer tümörlere sahip hastalar çok farklı sonuçlar ve tedavi yanıtları gösterebilir. Bu çalışmada araştırmacılar kanser hücrelerinin ötesine bakarak dokuyu inşa eden ve yeniden şekillendiren fibroblast adı verilen etrafındaki “yardımcı” hücrelere odaklanıyor. Bu hücreleri tek tek incelerken gelişmiş bilgisayar modellerini kullanan ekip, fibroblastların hastaların gidişatını ve tümörlerin güncel immünoterapilere nasıl yanıt verebileceğini öngörebilen farklı tiplerde olduğunu gösteriyor.
Tümör mahallesine yakından bakmak
En yeni tek hücre RNA dizilemesi yöntemlerini kullanarak ekip, tedavi edilmemiş akciğer adenokarsinom örneklerinden 140.000’den fazla bireysel hücreyi analiz etti. Bu teknik her hücrede hangi genlerin aktif olduğunu ortaya koyarak yazarların tümörü ana sakinlerine ayırmasına olanak verdi: bağışıklık hücreleri, kanser hücreleri, damar hücreleri ve fibroblastlar. Tümörlerin her hücre tipinin miktarı açısından geniş bir değişkenlik gösterdiği saptandı. Bazı tümörler bağışıklık hücreleriyle doluyken diğerleri fibroblastlar ve yapısal doku tarafından baskın olarak işgal ediliyordu. İzleyen analizler her bir hücre tipinin bağışıklık saldırılarını düzenlemekten tümörün yapısal iskelesini inşa etmeye kadar özel görevleri yerine getirdiğini gösterdi.
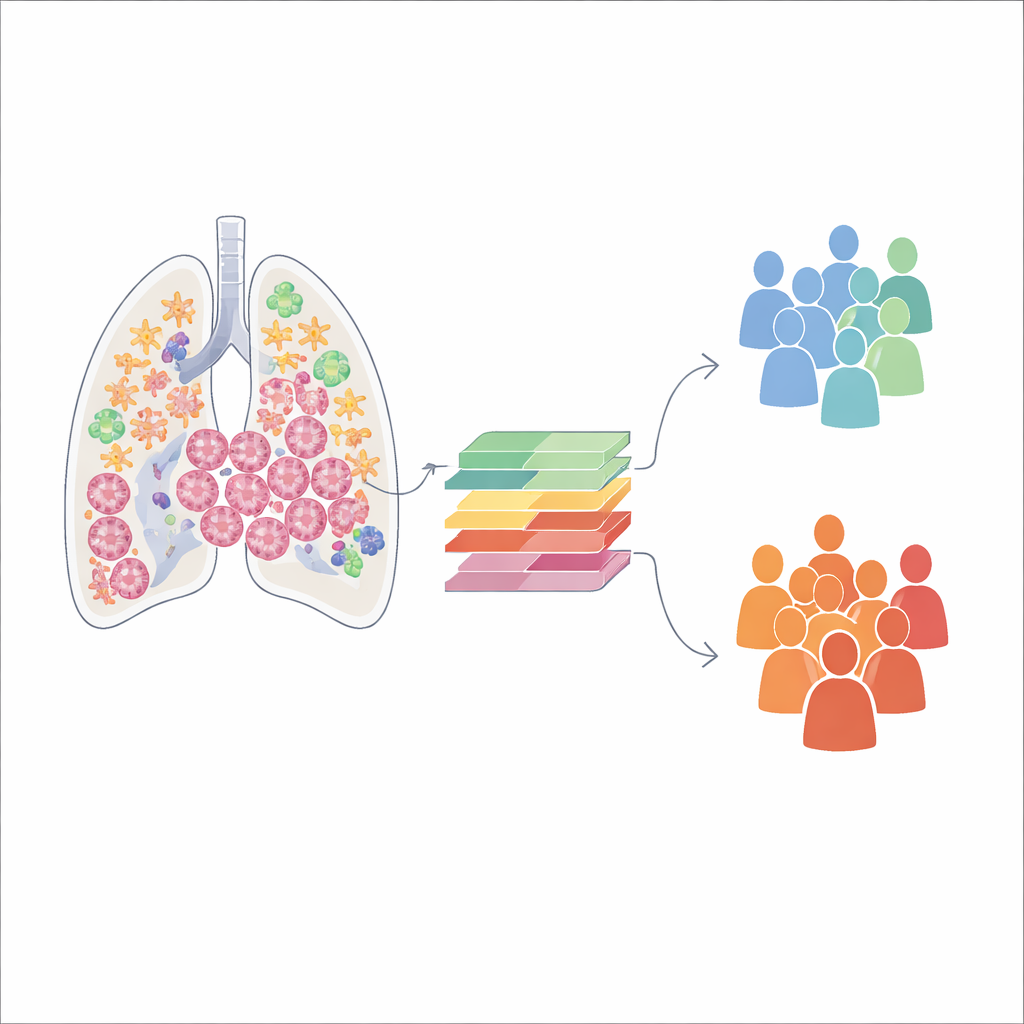
Tüm fibroblastlar aynı değil
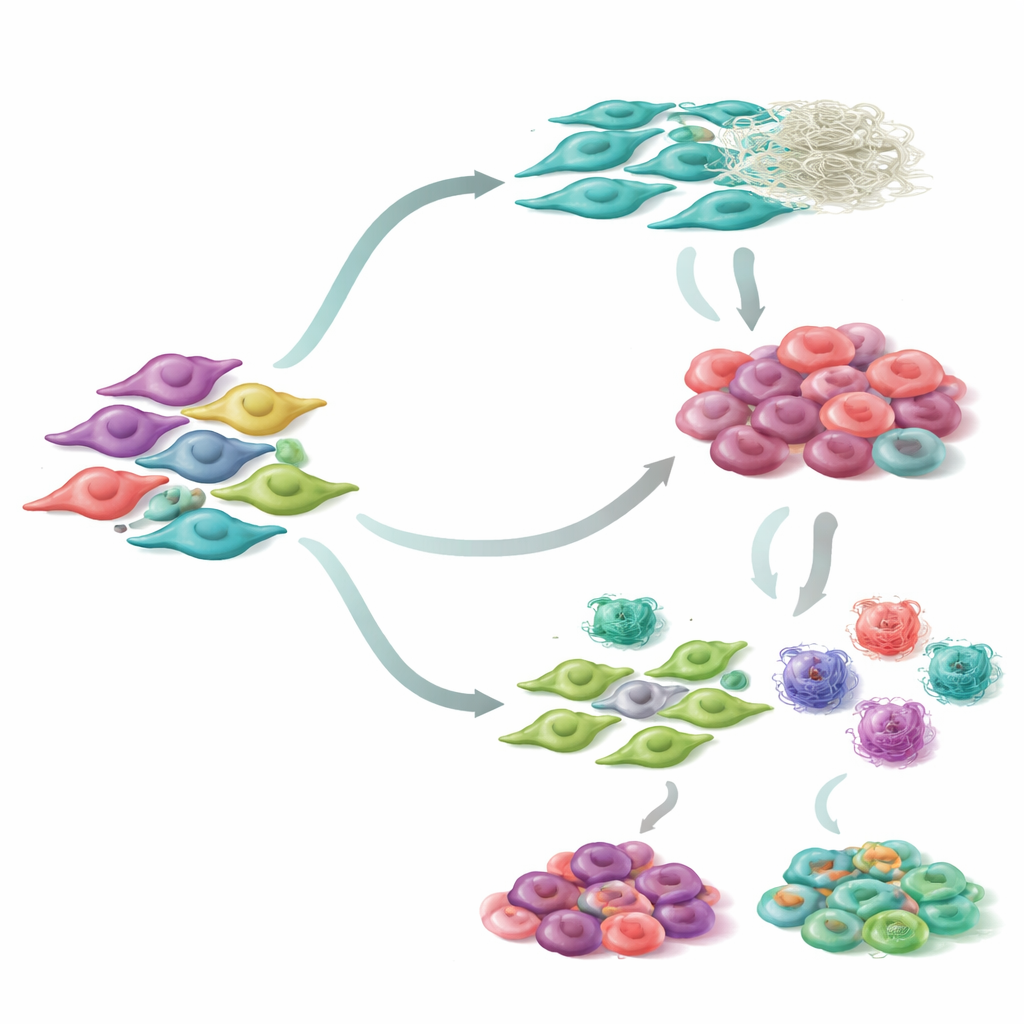
Araştırmacılar özel olarak fibroblastlara odaklandıklarında, akciğer tümörleri içinde yedi ayrı fibroblast alt grubu keşfettiler. Bu hücrelerin zaman içinde nasıl değiştiklerini yeniden yapılandırarak iki ana gelişim yolu gözlemlediler. Bir yolda fibroblastlar kademeli olarak tümör çevresini yeniden şekillendiren kasılıp dokuyu sertleştiren hücre özellikleri kazanıyor. Diğer yolda ise fibroblastlar bağışıklık sistemiyle etkileşimde daha fazla rol alıyor; ya bağışıklık hücrelerini çekiyor ya da baskılıyorlar. Her alt grup benzersiz gen aktivite desenleri gösterdi ve kas benzeri kasılma, hareket veya bağışıklık düzenlemesi gibi farklı biyolojik görevlerle ilişkilendirildi. Önemli olarak, belirli fibroblast alt tiplerinin zengin olduğu tümörlere sahip hastalar genellikle daha uzun yaşam gösterdi; bu da fibroblast durumlarının yalnızca bir merak değil—gerçek klinik sonuçlarla bağlantılı olduğunu gösteriyor.
Fibroblast sinyallerinden risk skoru oluşturmak
Bu biyolojik çıkarımları klinikte kullanışlı bir şeye dönüştürmek için ekip, tek hücre verilerinden elde edilen fibroblast işaretçi genlerini yüzlerce hastanın toplu tümör verileriyle birleştirdi. Ardından hangi fibroblast ilişkili gen karışımının hasta sağkalımını en iyi öngördüğünü bulmak için 10 farklı makine öğrenimi yöntemini içeren ve 101 model kombinasyonu test eden bir yaklaşım uyguladılar. Kazanan model, fibroblast ilişkili imza (FRS) adını taşıyan model, her hastaya risk puanı atamak için 29 gen kullanıyor. Ana veri seti ve altı bağımsız hasta kohortunda yüksek FRS puanına sahip olanların düşük puanlılara göre tutarlı şekilde daha kötü sağkalım gösterdiği görüldü. FRS, yaş, cinsiyet ve tümör evresi göz önüne alındığında bile güçlü bir öngörücü olmaya devam etti ve standart TNM evreleme sistemiyle birleştirildiğinde öngörüyü iyileştirdi.
Bağışıklıktan kaçış ve tedavi yanıtına dair ipuçları
Birçok hastanın artık immünoterapi aldığı düşünüldüğünde, yazarlar fibroblast tabanlı skorun tümörün bağışıklık ortamına dair özellikleri yakalayıp yakalamadığını sordular. Düşük FRS puanlı tümörlerin CD8 T hücreleri ve doğal öldürücü hücreler gibi kanserle savaşan bağışıklık hücreleri tarafından daha zengin bir şekilde işgal edildiğini ve tümör parçacıklarını bağışıklık sistemine sunmaya yardımcı genlerin daha yüksek ifade edildiğini buldular. Buna karşılık yüksek FRS’li tümörler daha az yararlı bağışıklık hücresi, daha yüksek tümör hücresi fraksiyonu, daha fazla genetik istikrarsızlık ve bağışıklık dışlanması belirtileri gösteriyordu; yani bağışıklık hücreleri uzak tutuluyor. İmmün kontrol noktası ilaçlarına olası yanıtı simüle eden ölçümler, düşük FRS puanlı hastaların bu terapilerden daha fazla fayda sağlayabileceğini, yüksek FRS’li hastaların ise daha dirençli olabileceğini öne sürdü.
Ümit veren hedef genin ön plana çıkarılması
FRS’yi oluşturan genler arasında ekip TIMP1 adını, kötü prognozun özellikle güçlü bir işareti olarak vurguladı. TIMP1 birçok kanser türünde yüksek düzeyde bulundu ve özellikle çevre normal akciğer dokusuna kıyasla akciğer adenokarsinom dokusunda yükselmişti. Laboratuvar deneylerinde, akciğer kanseri hücre hatlarında TIMP1 düzeylerinin azaltılması hücrelerin bir matriks içinde invazyon yapma ve yeni koloniler oluşturma yeteneğini azalttı; bu da TIMP1’in tümör büyümesi ve yayılmasını desteklediğini düşündürüyor. Bu sonuçlar TIMP1’i tümörün yapısal ve bağışıklığı şekillendiren mekanizmasını zayıflatmayı amaçlayan gelecekteki ilaçlar için potansiyel bir hedef olarak işaretliyor.
Hastalar için bunun anlamı
Bu çalışma, özellikle fibroblastlar olmak üzere bir akciğer tümörünün çevresindeki destekleyici hücrelerin hastalığın nasıl davranacağını ve tedaviye nasıl yanıt verebileceğini gösteren değerli bilgiler taşıdığını ortaya koyuyor. Tek hücre ölçümlerini makine öğrenimiyle birleştirerek yazarlar, hastaları daha yüksek ve daha düşük risk gruplarına ayırabilen ve hangi tümörlerin immünoterapiye direnç gösterebileceğine dair ipuçları sunan fibroblast tabanlı bir risk skoru oluşturdu. Böyle bir skorun günlük bakımda yol gösterici olabilmesi için daha fazla test gereklidir; yine de çalışma, akciğer kanserini etkili şekilde tedavi etmenin yalnızca kanser hücrelerine saldırmayı değil, tümörün büyümesine ve saklanmasına yardımcı olan çevresindeki fibroblastları da kontrol altına almayı gerektirdiğini vurguluyor.
Atıf: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
Anahtar kelimeler: akciğer adenokarsinomu, kansere bağlı fibroblastlar, tek hücre dizilemesi, tümör mikroçevresi, immunoterapi yanıtı