Clear Sky Science · tr
İnflamatuvar bölgelerde M2 makrofaj polarizasyonunu teşvik etmede α7 nikotinik asetilkolin reseptörünün rolü
Sinirler Kontrolden Çıkan İltihabı Nasıl Sakinleştirir
Parmağımızı kestiğimizde veya bir enfeksiyonla savaştığımızda vücudumuz bizi korumak için iltihap başlatır. Ancak bu tepki çok uzun sürerse sağlıklı dokuya zarar verebilir ve kronik hastalıklara yol açabilir. Bu çalışma, bağışıklık hücrelerindeki α7 nikotinik asetilkolin reseptörü (α7nAChR) olarak adlandırılan özel bir “sakinleştirici” reseptörün, iltihabı zarar vermekten ziyade iyileştirmeye yönlendirmeye nasıl yardımcı olduğunu araştırıyor; bu, sepsis, bağırsak hastalıkları ve artrit gibi durumlar için yeni tedavi ipuçları sunuyor.
Bağışıklığın İki Yüzü
Makrofajlar, temizlik ve onarım ekipleri görevi gören bağışıklık hücreleridir. İki ana moda geçiş yapabilirler. Genellikle M1 olarak adlandırılan “saldırı” modunda, mikropları öldürmek ve artık maddeleri temizlemek için agresif kimyasallar salarlar. “İyileştirici” mod olan M2’de ise iltihabı yatıştıran ve doku onarımını destekleyen sinyaller salgılarlar. Sağlıklı bir yanıt, önce daha fazla M1 hücresiyle başlayıp tehlike geçtikçe kademeli olarak M2’ye kayar. Yazarlar, sinir iletişimindeki rolü ve nikotinin beyin üzerindeki etkileriyle ünlü olan α7nAChR’nin, iltihap sırasında makrofajları bu iyileştirici M2 durumuna yönlendirmeye yardımcı olup olmadığını merak ettiler.
İyileştirmeye Doğru Sinir Bağlantılı Bir Anahtar
Bunu incelemek için araştırmacılar α7nAChR’ye sahip veya bu reseptörden yoksun fareleri kullandılar ve karın boşluğunda iki şekilde iltihap tetiklediler: bakteriyel bir bileşenle (enfeksiyonu taklit ederek) ve nazikçe bağırsak ellemesiyle (steril cerrahi yaralanmayı taklit ederek). M1 ile M2 davranışını ayırt eden moleküler belirteçleri ölçtüler ve akış sitometrisi ile her bir makrofaj tipinin oranlarını saydılar. Normal farelerde iltihabın erken evresi M1 sinyalleriyle baskındı, ancak izleyen bir ila iki gün içinde M2 hücre belirteçleri yükselerek onarıma doğal bir geçişi yansıttı. Ancak α7nAChR eksik farelerde, pro-inflamatuvar belirteçler daha yüksek, iyileştirici belirteçler daha düşük ve iltihaplı bölgede M2 makrofajların oranı sürekli olarak azalmıştı; bu da yerel dengeyi M1 ağırlıklı, daha zararlı bir duruma eğdi.
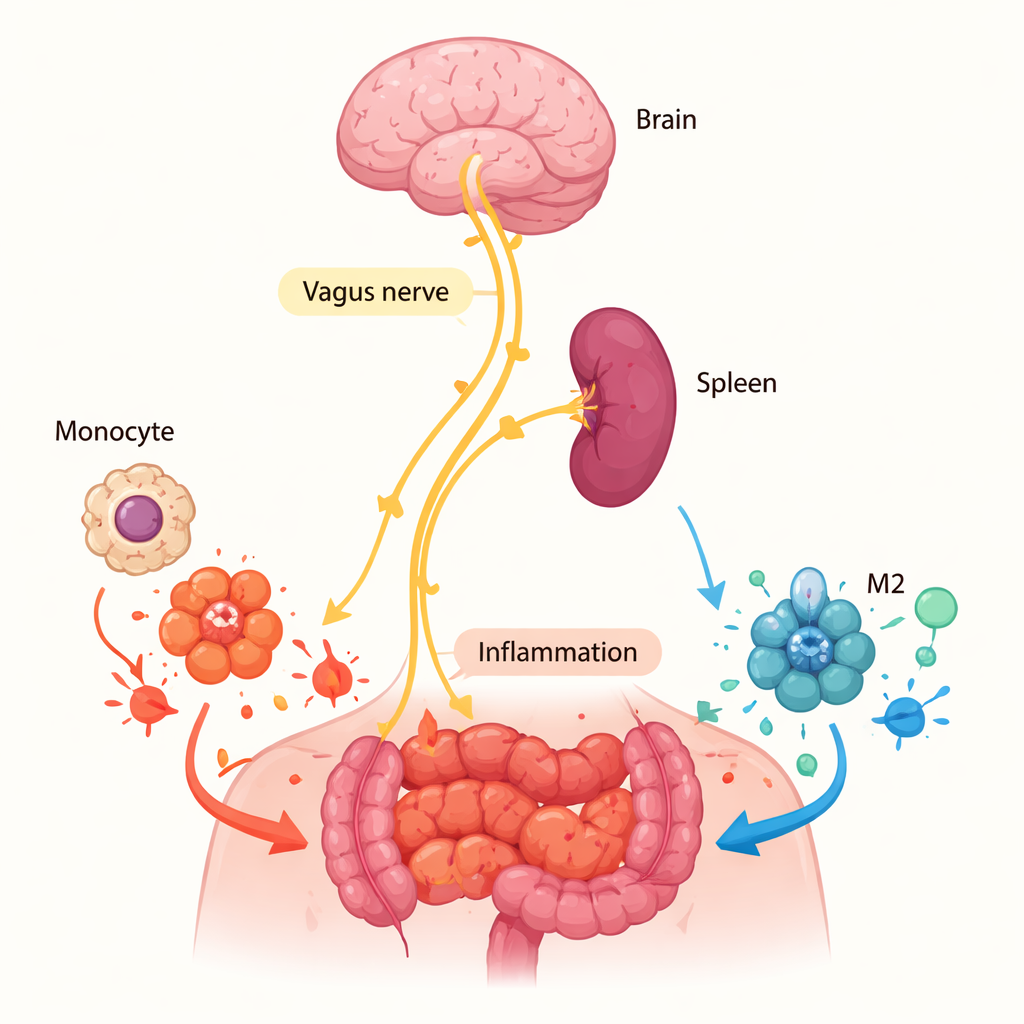
Dalak Yaradan Daha mı Önemli?
Ekip bir sonraki olarak α7nAChR’nin bu işi nerede yaptığını sordu. Reseptör, inflame bölgedeki hücreler asetilkolin salgılıyorsa doğrudan yerel olarak etkili olmuş olabilirdi; asetilkolin reseptörü harekete geçiren kimyasaldır. Ancak karın sıvısı ve inflame doku hücre kültürlerindeki asetilkolin ölçümleri neredeyse yoktu ve bu güçlü bir yerel sinyalin lehine değildi. Bunun yerine dikkat, vagus siniri tarafından denetlenen “kolinerjik anti-inflamatuvar yol”da rol oynadığı bilinen önemli bir bağışıklık organı olan dalağa döndü. Araştırmacılar normal farelerden dalağı cerrahi olarak aldıklarında ve ardından karın iltihabı oluşturduklarında, periton boşluğundaki M2 makrofaj oranı düştü ve toplam makrofaj sayısı azaldı. Bu desen, α7nAChR eksik farelerde gördükleriyle örtüştü; bu da sinir kaynaklı sinyallerin dalakta monositleri—makrofajların öncülerini—inflame dokuya varmadan önce M2 hücreleri olmaya hazırladığını düşündürüyor.
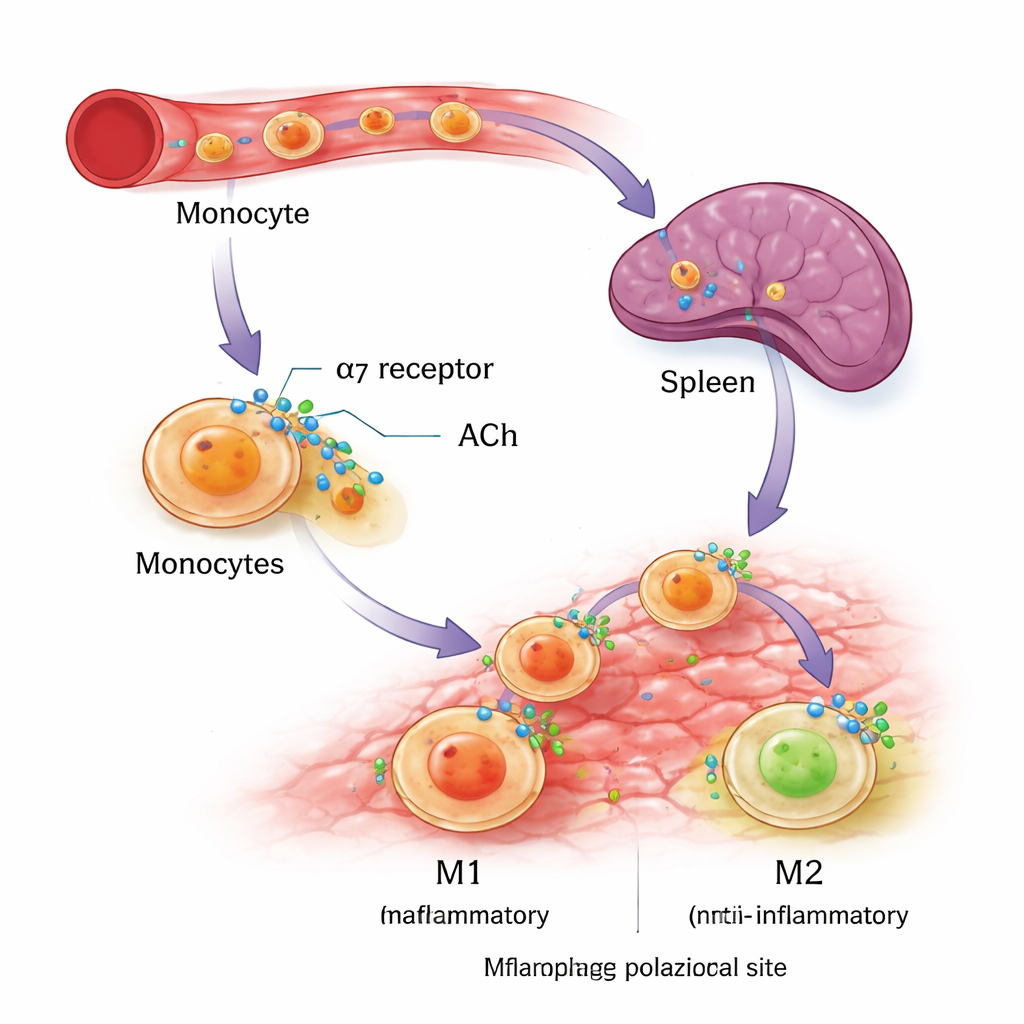
İnsan Hücrelerinde Anahtarı Test Etmek
Aynı reseptörün insan hücrelerini ayarlayıp ayarlamadığını görmek için bilim insanları laboratuvarda yetiştirilen lösemi hücre hattından (THP-1) ve bağışlanan insan kanından monositlere yöneldiler. Bu hücreleri standart bağışıklık sinyalleriyle ya M1 ya da M2 makrofajlara gelişmeleri için yönlendirdiler ve ardından spesifik bir α7nAChR aktive edici ilaç eklediler. Her iki insan hücre kaynağında da α7nAChR’yi açmak M1 belirteçlerini artırmadı, ancak yüzey proteini CD206 ve anti-inflamatuvar molekül interlökin-10 dahil olmak üzere M2 davranışının temel işaretlerini belirgin şekilde yükseltti. Bu deneyler, α7nAChR’nin bağışıklık yanıtını tamamen kapatmak yerine gelişmekte olan makrofajların iyileştirici bir kimliği benimsemelerini kolaylaştıran bir eğilim belirleyici anahtar gibi davrandığı fikrini destekliyor.
Nikotinden Gelen İpuçlarından Gelecek Tedavilere
Bu bulgular, vagus sinirinin uyarılmasının inflamatuvar hastalıkları neden iyileştirebildiği ve sigara içenlerin birçok sağlık riski olmasına rağmen belirli bağırsak durumları için neden biraz daha düşük bir risk taşıyor gibi göründüğü gibi birkaç şaşırtıcı gözlemi açıklamaya yardımcı oluyor—nikotin α7nAChR’yi aktive edebilir. α7nAChR, inflamatuvar kimyasalları yalnızca engellemek yerine, vücudun temizlik ekiplerini daha onarım odaklı M2 hücrelerine dönüştürmesine yardımcı oluyor gibi görünüyor; özellikle monositlerin dalakta eğitilmesi yoluyla. Bir okuyucu için bu, sinir sistemimizin sadece ağrıyı hissetmek veya kasları kontrol etmekten daha fazlasını yaptığı; aynı zamanda bağışıklık hücrelerine ne zaman savaşmaları, ne zaman iyileştirmeye odaklanmaları gerektiğini sessizce öğrettiği anlamına geliyor. Bu yerleşik anahtarı ilaçlarla veya hedefli sinir uyarımıyla güvenli şekilde çevirmeyi öğrenmek, vücudun savunma yeteneğini korurken zararlı iltihabı sakinleştirmenin yeni yollarını açabilir.
Atıf: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Anahtar kelimeler: makrofaj polarizasyonu, iltihap, vagus siniri, nikotinik asetilkolin reseptörü, bağışıklık düzenlemesi