Clear Sky Science · tr
Fizyolojik koşullarda bulunan Tc‑ ve Re‑pirofosfat radyoaktif izleyicilerin formları ve bunların transtiretin amiloid duyarlılığının temeli
Bu kalp görüntüleme hikâyesi neden önemli?
Birçok kişide yaşlanmayla birlikte kalpte amiloid adı verilen yanlış katlanmış protein birikintileri sessizce oluşur. Bu birikintilerden bazıları, özellikle transtiretin adı verilen bir kan proteininin oluşturdukları, kalbi sertleştirip ciddi hastalıklara yol açabilir. Hekimler giderek daha çok bu birikintileri görüntülemek için teknisyum‑99m pirofosfat (99mTc‑PYP) olarak bilinen radyoaktif izleyiciye dayanıyor. Buna rağmen, şaşırtıcı biçimde, bu izleyicinin vücutta tam olarak hangi formda bulunduğu ve neden belirli amiloid türlerine “tercih” gösterdiği net değildi. Bu makale, izleyicinin canlı koşullarda nasıl göründüğünü ve bu şeklin zararlı transtiretin fibrillerini nasıl hedefleyebileceğini teori ve deneyi birleştirerek ortaya koyuyor.
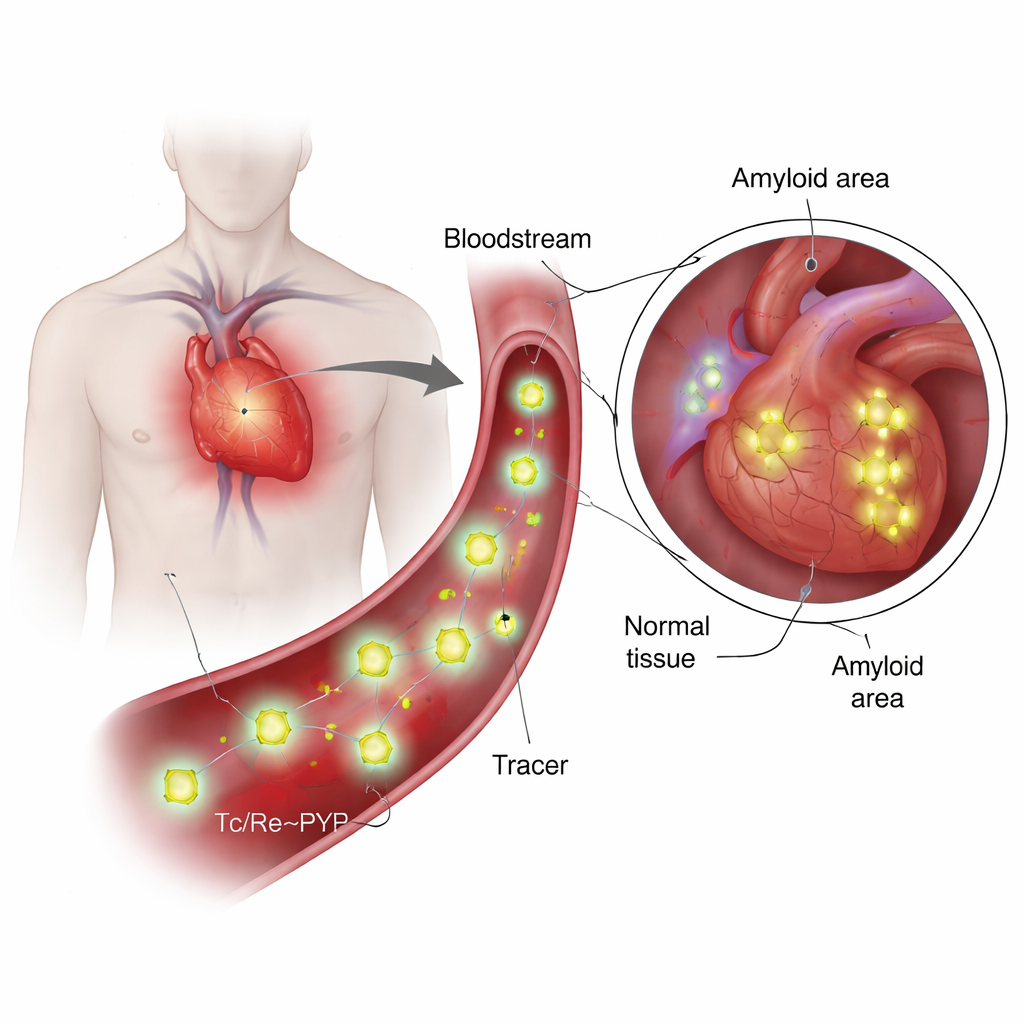
Bu izleyiciler nedir ve neden özel?
99mTc‑PYP onlarca yıldır kemiği görüntülemek için kullanıldı; çünkü kalsiyumun ve mineral dönüşümünün yüksek olduğu yerlerde birikme eğilimindedir. Daha yakın zamanda hekimler bunun ayrıca iki ana kardiyak amiloidoz türünü ayırt edebildiğini keşfettiler: antikor hafif zincirlerinden (AL) oluşan bir tür ve transtiretinden (ATTR) oluşan bir diğer tür. ATTR olgularında kalp PYP taramalarında genellikle güçlü bir şekilde ışıldarken, AL vakaları kalsiyum birikimi benzer görünse bile genelde sönük kalır. Bu uyumsuzluk önemli bir soruyu gündeme getirdi: izleyici yalnızca kalsiyuma mı yapışıyor, yoksa doğrudan amiloid proteiniyle mi etkileşiyor? Buna yanıt vermek, izleyicinin kan benzeri koşullar altındaki gerçek kimyasal yapısının bilinmesini gerektirir; önceki çalışmalar bunu sadece kaba hatlarıyla tasvir etmişti.
Görünmeyeni görmek için daha güvenli bir yerine koyma kullanmak
Teknezyum radyoaktiftir ve medikal hazırlıklarda yalnızca çok küçük miktarlarda bulunduğundan, birçok laboratuvar tekniğiyle doğrudan çalışmak zordur. Bu nedenle yazarlar, benzer boyut ve bağlanma tercihleri olan ama daha elverişli kimyası sayesinde rutenyum yerine rheniumu kullandılar. Klinik PYP kitlerini taklit eden koşullar altında rhenium‑pirofosfat karışımları hazırladılar ve ardından bunları yüksek düzey kuantum kimyası hesaplamaları, UV‑görünür ışık absorbsiyonu, çeşitli titreşim spektroskopileri (kızılötesi ve Raman), nükleer manyetik rezonans, kütle spektrometrisi ve kalay Mössbauer spektroskopisi gibi çok sayıda araçla incelediler. Bu yöntemlerin birleşimi, çok sayıda aday yapıyı test etmelerine ve kanın nötr pH’sına benzer koşullarda hangi türlerin bulunma olasılığının yüksek olduğunu daraltmalarına izin verdi.
Esnek ama tanınabilir bir moleküler şekil
Bütünleşik kanıtlar ortak bir “çekirdek” yapıya işaret ediyor: +4 yükseltgenme durumunda bir teknezyum ya da rhenium atomunun iki pirofosfat grubu ve iki su molekülüne bağlandığı oktahedral bir kompleks. Basitçe söylemek gerekirse, metal oksijen atomlarının oluşturduğu neredeyse oktahedral bir kafesin merkezinde oturuyor; pirofosfatlar çok dişli çapa görevi görürken su molekülleri kalan pozisyonları dolduruyor. Bu temel diaqua dipirofosfat birimi katı değil. Pirofosfat kollarının dönmesi ve bağlanmış sularla içsel hidrojen bağları oluşturabilmesi nedeniyle molekül çözeltide birçok hafif farklı şekil örnekliyor. Hesaplamalar ve spektrumlar bu farklılıkların ışık absorbsiyonunu ve titreşimsel parmak izlerini kaydırdığını, bunun da deneysel bantların geniş olmasını ve önceki çalışmaların tek, temiz bir yapı tespit etmekte zorlanmasını açıkladığını gösteriyor.
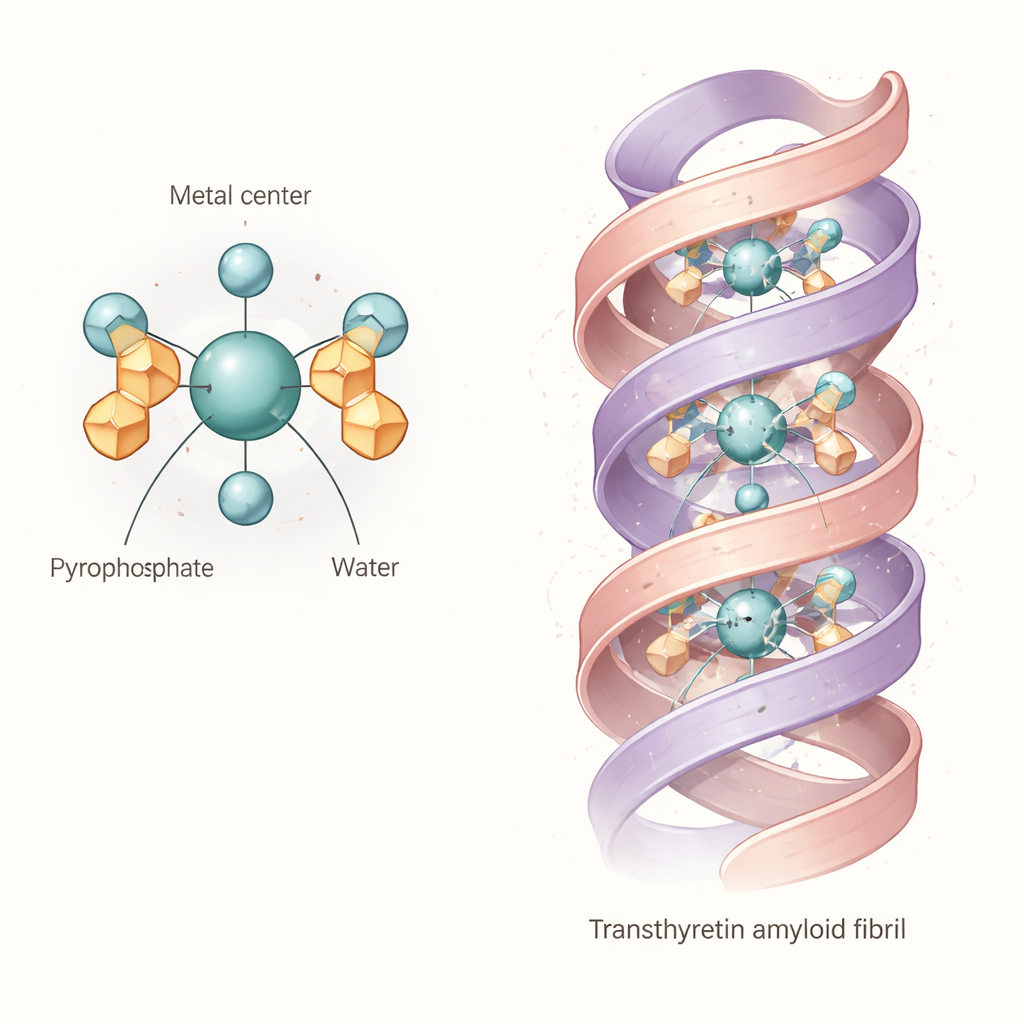
Kalp amiloidine bağlanma için ne anlama geliyor?
Yazarlar daha sonra bu esnek kompleksin transtiretin amiloid fibrillerine doğrudan yerleşip yerleşemeyeceğini sordular. İnsan transtiretin fibrilinin ayrıntılı bir kriyo‑elektron mikroskopisi yapısını kullanarak, modellenmiş teknezyum‑pirofosfat kompleksi ile bilgisayar destekli yerleştirme (docking) aramaları yaptılar. Sonuçlar, diaqua dipirofosfat biriminin fibril boyunca uzanan merkezi bir kanala sığıp kanalın iç yüzünü döşeyen yüklü yan zincirlerle çoklu hidrojen bağları ve tuz köprüleri kurabildiğini gösteriyor. Bu, en azından bazı transtiretin fibril şekilleri için izleyicinin yalnızca yakındaki mineral birikimlerini etiketlemediğini; aksine protein iskeleti tarafından doğrudan kavranıyor olabileceğini öne sürüyor. İzleyicinin yapısal esnekliği, gerçek hasta fibrillerindeki hafif farklı cep ve yük desenlerine uyum sağlamasına yardımcı oluyor olabilir.
Tanı ve gelecekteki izleyiciler için çıkarımlar
Halk için çıkarım şu: yaygın olarak kullanılan PYP kalp taraması, daha önce anlaşıldığından daha ince ve proteine duyarlı bir izleyiciye dayanıyor. Fizyolojik koşullar altında, bunu esneyebilen ve transtiretin amiloid kanallarına birden çok temas noktası kurabilen küçük, su taşıyan bir metal‑pirofosfat kafesi olarak düşünmek en doğru yaklaşımdır. Bu içgörü, izleyicinin bazı amiloid hastalıklarında neden güçlü sinyaller verdiğini ama diğerlerinde vermediğini ve proteindeki ya da çevresindeki küçük değişikliklerin duyarlılıkta neden kafa karıştırıcı kayıplara yol açabileceğini açıklamaya yardımcı olur. İzleyicinin çalışma şekli ve yük desenini netleştirerek çalışma, kalpte ve ötesinde hastalık yapıcı fibrilleri daha seçici tanıyan veya hedefleyen yeni nesil görüntüleme ya da terapötik ajanların tasarımı için bir temel oluşturuyor.
Atıf: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Anahtar kelimeler: kardiyak amiloidoz, transtiretin, teknezyum pirofosfat, moleküler görüntüleme, radyotracer kimyası