Clear Sky Science · tr
Sayısal graf tabanlı belirteçler ve makine öğrenimi kullanılarak sitotoksik bileşiklerin nicel bir çalışması
Gelecekteki kanser ilaçları için bu araştırma neden önemli
Tümör hücrelerini öldüren kanser ilaçları, yani sitotoksik ilaçlar, sıklıkla yaşam kurtarmak ile ciddi yan etkilere yol açmak arasında ince bir çizgide yürür. Daha güvenli ve daha etkili tedaviler tasarlamak için bilim insanlarının bu ilaçların vücutta nasıl hareket ettiğini —ne kadar iyi emildiklerini, hücre zarlarını ne kadar kolay geçtiklerini ve nerede birikme eğiliminde olduklarını— hızlı ve güvenilir biçimde tahmin etmeleri gerekir. Bu çalışma, ilaç moleküllerinin matematiksel tanımlarıyla modern makine öğrenimini birleştirmenin, bu davranışı kontrol eden temel bir özelliği yüksek doğrulukla tahmin edebildiğini gösteriyor; bu da daha iyi kanser tedavileri arayışını hızlandırabilir.
İlaçların nereye gidebileceğini belirleyen ana bir yüzey
Makalenin merkezindeki fikirlerden biri topolojik polar yüzey alanı, yani Top_PSA’dır. Basitçe söylemek gerekirse bu, bir molekülün yüzeyinin ne kadarının suyu seven ve hidrojen bağı oluşturabilen “polar” bölgelerden oluştuğunu yansıtan bir sayıdır. Çok yüksek polar yüzey alanına sahip moleküller genellikle yağlı hücre zarlarını geçmekte zorlanır ve ağızdan alındıklarında kötü emilebilir. Çok düşük polar yüzey alanına sahip moleküller ise birçok engeli çok kolay aşarak bazen beyin gibi hassas dokularda istenmeyen yan etkilere yol açabilir. Top_PSA, bir molekülün 2B çiziminden yavaş 3B simülasyonlara ihtiyaç duymadan hızlıca hesaplanabildiği için bu taşıma özelliklerini kestirmek adına popüler bir kestirim olmuştur.
Moleküler çizimleri sayılara dönüştürmek
Araştırmacılar, gerçek antikanser ilaçlardan ve deneysel ajanlardan derlenen özenle seçilmiş 156 farklı sitotoksik bileşikseti topladılar. Ardından her molekülü 58 sözde belirtece dönüştürdüler — bu sayılar bir molekülün kaç atom içerdiği, kaç halkası olduğu, bağlarının ne kadar esnek olduğu, kaç atomun hidrojen bağı oluşturabildiği ve farklı kısımların ne kadar polar veya elektronegatif olduğu gibi özellikleri yakalar. Bu belirteçlerin çoğu, bir molekülün bağlı düğümler ve bağlantılar ağları olarak ele alındığı grafik kuramından gelir. Her molekülün bu zengin sayısal portresi, yaygın olarak kullanılan kimya araç takımları tarafından hesaplanan Top_PSA değerlerini tahmin etmeye çalışan bilgisayar modelleri için giriş verisi olarak kullanıldı.
Doğru tahmine giden birden çok yolu test etmek
Bu belirteçleri Top_PSA ile ilişkilendirmenin en iyi yolunu bulmak için ekip birkaç modelleme stratejisini karşılaştırdı. Standart doğrusal regresyonun yanı sıra ridge ve LASSO olarak adlandırılan iki “düzenlenmiş” versiyonunu denediler; bu yöntemler gürültülü, örtüşen bilgilerle daha iyi başa çıkmak üzere tasarlanmıştır. Ayrıca farklı veri hazırlama şemalarını da incelediler: modelleri ham belirteçlere doğrudan uydurmak, temel bileşen analizi (PCA) ile sıkıştırmak, uç değerlerin etkisini azaltan (robust) ölçekleme uygulamak, aykırı değerleri düzeltmek ve varyans enflasyon faktörü adı verilen bir ölçü kullanarak yüksek korelasyonlu özellikleri budamak. Her yaklaşım, aşırı uyumu engellemek için veriyi tekrar tekrar eğitim ve test alt gruplarına bölen k‑fold çapraz doğrulama yöntemiyle dikkatle değerlendirildi.
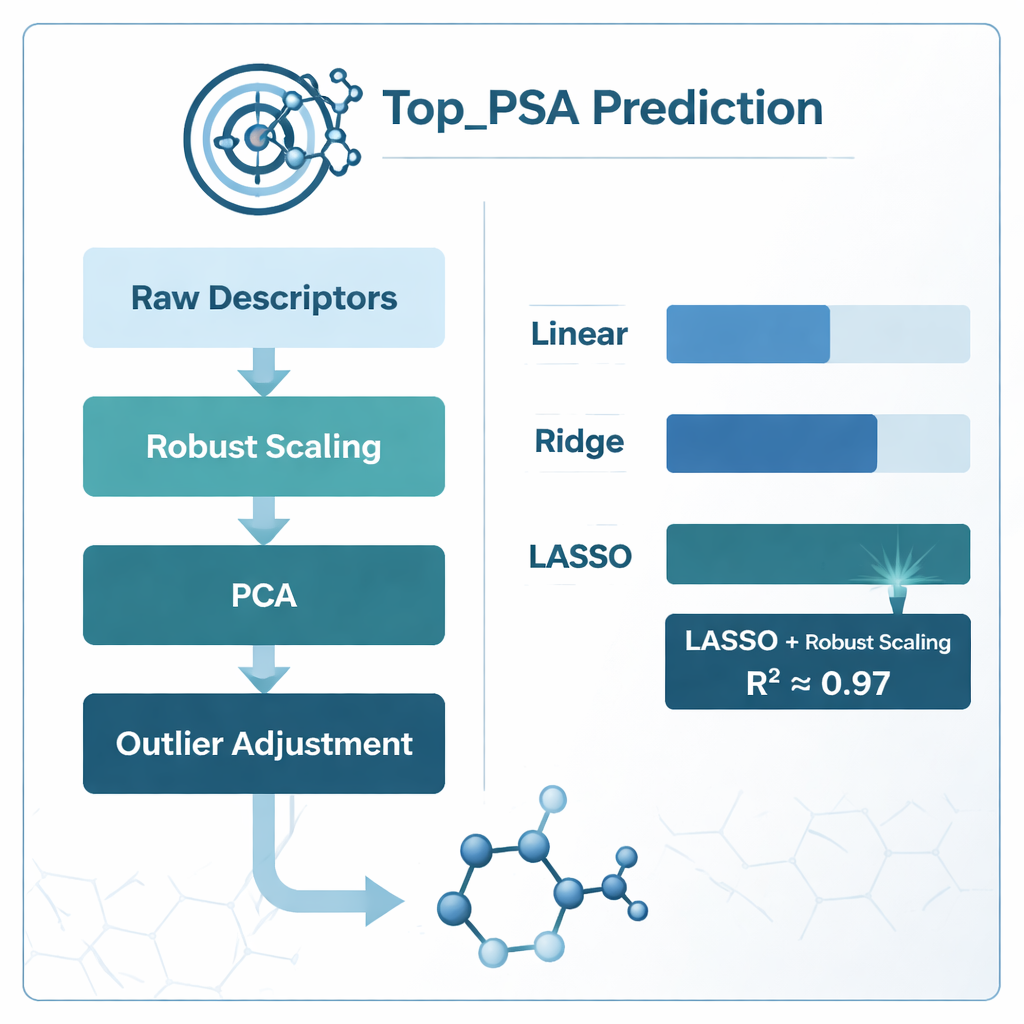
En iyi çalışan yöntem ve modellerin öğrendikleri
Net kazanan, robust ölçekleme ile LASSO regresyonunun kombinasyonu oldu; bu yaklaşım yaklaşık 0,97 katsayısıyle belirlenen kararlılık (R²) elde etti — bu da 156 ilaç arasındaki Top_PSA varyasyonunun yaklaşık %97’sini açıklayabildiği anlamına geliyor. PCA tabanlı modeller ham doğrulukta yaklaşsa da, orijinal belirteçler soyut bileşenler içinde karıştığı için kimyasal olarak yorumlanmaları daha zordu. Varyans enflasyon faktörü ile korelasyonlu belirteçlerin basitçe budanması performansı aslında düşürdü; bu, bazı örtüşen ölçümlerin hâlen faydalı kimyasal bilgi taşıdığını düşündürüyor. LASSO’nun sıfır olmayan ağırlıklarını inceleyerek yazarlar, en önemli faktörlerin azot ve oksijen gibi heteroatomların varlığı, hidrojen bağı verme veya kabul etme yeteneği ve moleküler graf üzerindeki elektronegatif atomların düzenini izleyen indeksler olduğunu buldular — bunların hepsi polar yüzey alanının kimyasal sezgisiyle örtüşen özelliklerdir.
Bu çalışmanın daha iyi ilaç tasarımına rehberlik etmesi
Alanın dışındaki okuyucular için kilit mesaj, özenle hazırlanmış moleküler matematiksel parmak izlerinin uygun makine öğrenimi yöntemleriyle eşleştirildiğinde, kanser ilaçlarının vücutta ilerlerken ne kadar “yapışkan” veya “kaygan” olacaklarına dair hızlı ve güvenilir tahminler sağlayabileceğidir. Çalışma, diğer araştırmacılara belirteç verilerini nasıl ön işleyecekleri, hangi modelleme yaklaşımlarını tercih edecekleri ve hangi kestirmelerden kaçınacakları konusunda pratik rehberlik sunuyor. Uzun vadede, Top_PSA’nin böyle sağlam ve yorumlanabilir modelleri, kimyagerlerin potansiyel ilaçların devasa sanal kütüphanelerini süzerek zararı azaltılacak ve zararlı etkileri dengede tutacak bileşiklere odaklanmalarına yardımcı olabilir — bu da daha etkili ve daha az toksik kanser tedavilerine doğru atılmış önemli bir adımdır.
Atıf: Ahmad, S., Javed, S., Khalid, S. et al. A quantitative study of cytotoxic compounds using graph based descriptors and machine learning. Sci Rep 16, 5076 (2026). https://doi.org/10.1038/s41598-026-35728-7
Anahtar kelimeler: sitotoksik ilaçlar, polar yüzey alanı, moleküler belirteçler, makine öğrenimi, ilaç geçirgenliği