Clear Sky Science · tr
DENV-1 ve DENV-3 hedefleyen çok-epitop aşısının bilgisayar ortamında tasarımı
Neden dang humması aşıları hâlâ önemli
Dang humması artık nadir bir tropik hastalık değil; 100’den fazla ülkede milyarlarca insanı tehdit ediyor ve Asya, Latin Amerika ve ötesindeki bazı bölgelerde hastaneleri düzenli olarak zor durumda bırakıyor. Piyasada iki onaylı aşı bulunmasına rağmen koruma düzensiz; özellikle daha önce dengue geçirmemiş kişilerde ve aynı anda birden fazla viral serotipin dolaştığı bölgelerde bu sorun belirgin. Bu çalışma güncel bir soruyu gündeme getiriyor: bilgisayar destekli tasarım, genellikle birlikte görülen ve tehlikeli olabilen iki dengue tipine özel, daha güvenli ve daha hedeflenmiş bir aşı geliştirmemize yardımcı olabilir mi?
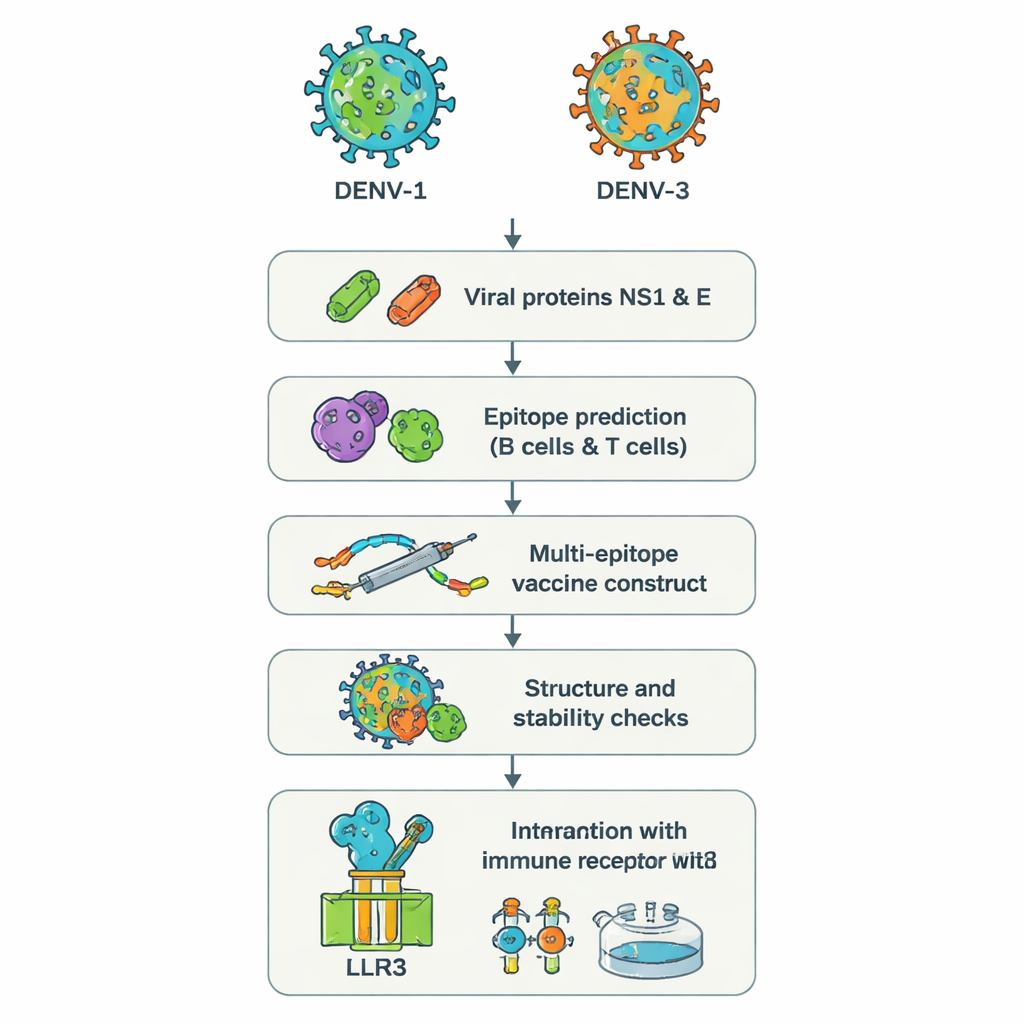
İki sinsi viral tip ve neden sorun yaratıyorlar
Dang virüsü dört çeşitte bulunur; DENV‑1’den DENV‑4’e kadar serotipler olarak adlandırılır. Herhangi biri yüksek ateş, şiddetli ağrı ve bazı durumlarda yaşamı tehdit eden kanama veya şokla sonuçlanabilir. Endişe verici şekilde, farklı bir serotip ile ikinci kez enfekte olmak bazen hastalığı daha kötüleştirebilir; çünkü önceden var olan antikorlar yeni virüsün hücrelere daha kolay girmesine yardımcı olabilir — buna antikor-bağımlı kuvvetlendirme denir. Son salgınlarda, doktorlar aynı anda DENV‑1 ve DENV‑3 ile enfekte olmuş hastalar bildirdi; bu kombinasyon daha şiddetli hastalık ve yanıltıcı test sonuçlarıyla ilişkilendirildi. Mevcut aşılar tüm yaş gruplarını ve tüm serotipleri güvenilir şekilde korumuyor; özellikle daha önce maruz kalmamış kişilerde savunmada tehlikeli bir boşluk kalıyor.
Molekülden başlayarak aşı tasarlamak
Araştırmacılar bütün virüsleri laboratuvarda çoğaltmak yerine bazen “ters aşıbilim” olarak adlandırılan bir yaklaşım kullandılar. DENV‑1 ve DENV‑3’ün NS1 ve E proteinlerinin genetik dizilerinden başladılar. Bu proteinler virüsün hücreleri işgal etme şekli ve bağışıklık sisteminin onu algılaması açısından kritik öneme sahip. Güçlü web tabanlı araçlar, protein dizilerini tarayarak insan B hücreleri (antikor üreten) ve T hücreleri (enfekte hücreleri öldüren ve yanıtları koordine eden) tarafından tanınması muhtemel kısa dizileri — epitopları — tespit etti. Yüzlerce aday arasından ekip, bağışıklık sistemi tarafından güçlü biçimde görülebileceği, iki serotip arasında paylaşılan ve interferon‑gamma gibi faydalı antiviral sinyalleri tetikleme potansiyeli olan küçük bir set seçti.
Tek çok amaçlı aşı molekülü oluşturmak
Seçilen epitoplar daha sonra dijital olarak bir uzun yapay proteinde birleştirildi; bu bir "çok‑epitop" aşıydı. Kısa amino asit bağlayıcılar, her epitopun şeklini koruması ve bağışıklık hücreleri tarafından erişilebilir kalması için esnek aralayıcılar görevi gördü. Beta‑defensin adı verilen doğal bir insan antimikrobiyal peptide dayanan ekstra bir parça, adjuvan olarak eklenerek genel yanıtı güçlendirmek üzere kullanıldı. Bilgisayar analizleri, nihai yapının 575 amino asit içerdiğini, kararlı, suda çözünebilir (dolayısıyla çözünmesi daha kolay) ve alerjen olma olasılığının düşük olduğunu öngördü. Daha ileri yapı tahmin araçları üç boyutlu bir model oluşturdu ve yapı taşlarının çoğunun bilinen protein yapılarıyla benzer gerçekçi pozisyonlarda yer aldığını kontrol etti.
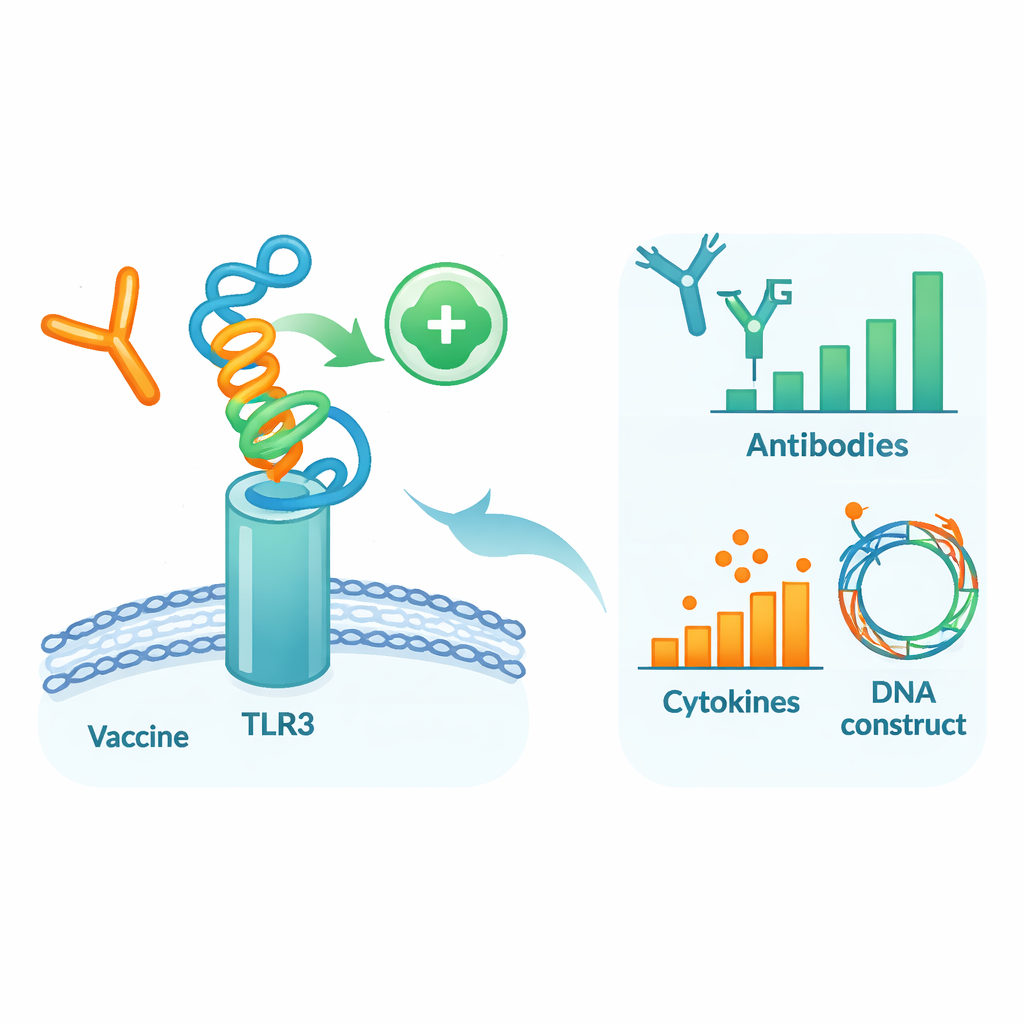
Adayı sanal bir vücutta test etmek
Bu tasarlanmış proteinin insan‑benzeri bir ortamda nasıl davranabileceğini görmek için yazarlar ayrıntılı bir dizi bilgisayar simülasyonu çalıştırdı. Önce aşı modeli, viral materyali algılayan ve erken savunmaları başlatmaya yardımcı olan immün hücrelerdeki bir sensör proteini olan TLR3’e bağlandı (docking). Moleküler dinamik simülasyonlar — atomların hareketinin sanal filmleri — aşı ile TLR3’ün stabil bir kompleks oluşturduğunu, bunun da elverişli bağlanma enerjileri ve çok sayıda hidrojen bağıyla desteklendiğini gösterdi. Hareket ve enerji analizlerinin ek incelemeleri, her iki molekülün temas "sıcak noktaları" olarak işlev gören belirli bölgelerini işaret etti. Ardından bağışıklık sistemi simülatörü, birkaç aylık süre boyunca üç aşı dozu taklit ederek kullanıldı. Sanal bağışıklık sistemi güçlü koruyucu IgG antikor dalgaları, uzun ömürlü B ve T hücre bellekleri ve güçlü antiviral yanıta uygun sinyal molekülleri üretti.
Bilgisayar modelinden laboratuvar için hazır plana
Son olarak, araştırmacılar aşının genetik kodunu yaygın laboratuvar mikroorganizmalarında verimli üretim için uyarladı ve bu optimize edilmiş DNA dizisini standart bir ekspresyon plazmidine başarıyla yerleştirerek gelecekteki deneysel testler için hazır hale getirdi. Basitçe söylemek gerekirse, bu çalışma DENV‑1 ve DENV‑3’ün dikkatle seçilmiş parçalarını hedefleyen, kararlı ve güvenli olması öngörülen ve bağışıklığın her iki kolunu güçlü şekilde harekete geçirmesi beklenen yeni bir dengue aşısı için ayrıntılı bir plan sunuyor. Bu sonuçlar tamamen hesaplamalı olup hücrelerde, hayvanlarda ve nihayetinde insanlarda doğrulanmalıdır; yine de modern biyoinformatik yöntemlerinin dengue eşzamanlı enfeksiyonu gibi karmaşık sorunlara yönelik hızlı, hedefe yönelik aşı adayları üretebildiğini gösteriyor.
Atıf: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Anahtar kelimeler: dengue aşısı, çok-epitop, DENV-1, DENV-3, immünoinformatik