Clear Sky Science · tr
Proteomik ve metabolomik entegratif analizi, adriamisin direncine sahip akut miyeloid lösemi hücrelerinde amino asit metabolizması bozukluğunu ortaya koyuyor
Bazı lösemi ilaçları neden etkisini yitirir
Kemoterapi, hızlı ilerleyen bir kanser olan akut miyeloid löseminin (AML) tedavisinde devrim yarattı. Yine de birçok hastada hastalık geri dönüyor çünkü kanser hücreleri, onları öldürmek için tasarlanmış ilaçlara karşı hayatta kalmayı öğreniyor. Bu çalışma basit ama kritik bir soruyu soruyor: Standart kemoterapi ilaçlarından biri olan adriamisine direnç geliştiren lösemi hücrelerinin içinde ne değişiyor ve bu değişiklikler ilacın etkisini geri kazandırmaya işaret edebilir mi?
Lösemi hücrelerinin içini gözetlemek
Bunu incelemek için araştırmacılar, HL60 adlı yaygın bir insan AML hücre hattını adriamisine dirençli hale getirilmiş bir kardeş hattla (HL60/R) karşılaştırdı. Tek tek gen veya proteinlere bakmak yerine, iki geniş ve tamamlayıcı yaklaşım kullandılar. Proteomik, hücredeki görevlerin çoğunu yürüten binlerce farklı proteini ölçtü. Metabolomik ise yağlar, şekerler ve amino asitler dahil olmak üzere hücre metabolizmasını oluşturan yüzlerce küçük molekülü ölçtü. Bu “omik” katmanları birleştirerek ekip, dirençli hücrelerin duyarlı kuzenlerinden nasıl farklı olduğuna dair ayrıntılı bir resim oluşturdu.
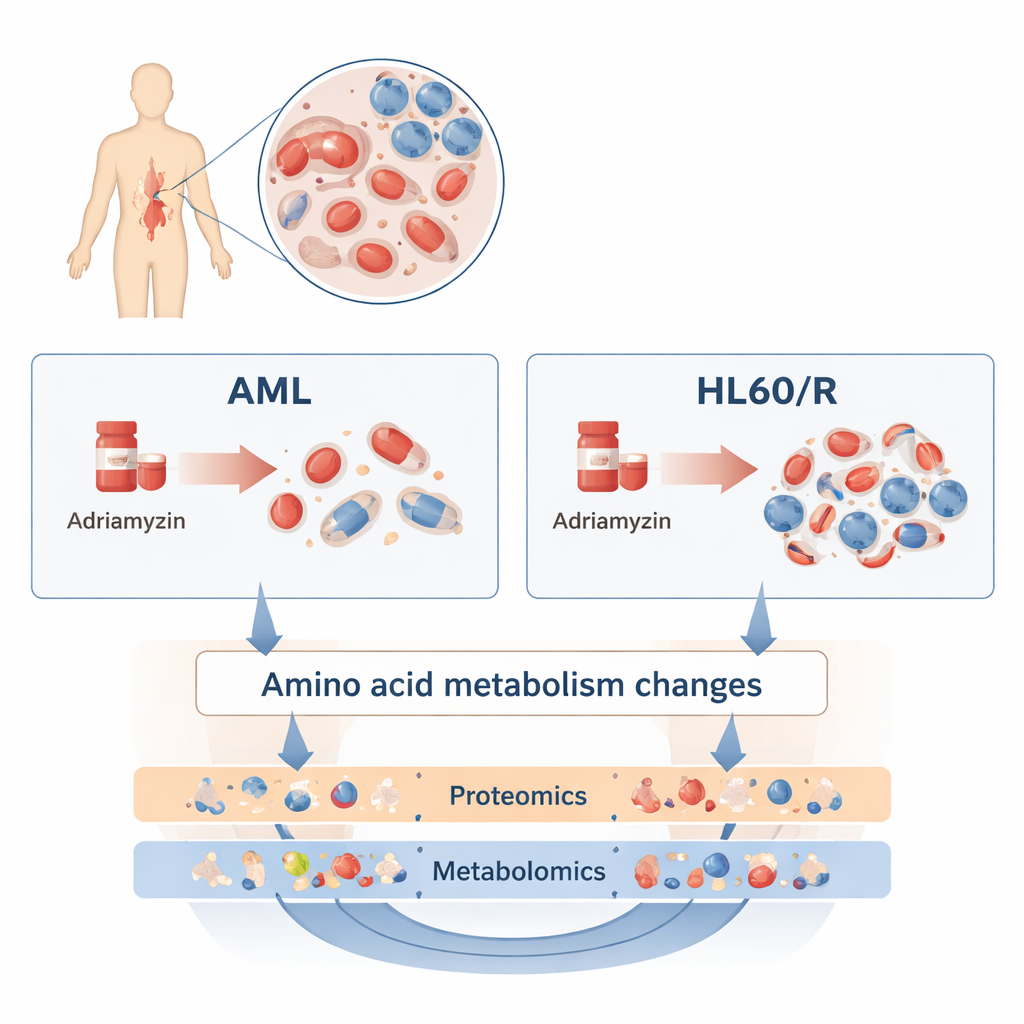
Hücresel mekanizmanın büyük ölçekli yeniden düzenlenmesi
Proteomik tarama geniş çaplı değişiklikler ortaya koydu: adriamisine dirençli hücrelerde normal HL60 hücrelerine kıyasla 3.200’den fazla proteinin seviyeleri artmış veya azalmıştı. Bu proteinlerin birçoğu, hücrelerin enerjiyi nasıl kullandığını ve strese nasıl yanıt verdiğini kontrol eden yolaklarda kümeleniyordu. Özellikle cAMP sinyal yolu, düşük oksijen koşullarında hücrelere yardımcı olan HIF‑1 yolu ve mitokondride enerji üreten temel bir süreç olan oksidatif fosforilasyonla ilişkili proteinlerde değişiklikler görüldü. Bu kaymalar, dirençli lösemi hücrelerinin kemoterapiye dayanabilmek için solunum, büyüme ve hücreler arası sinyalleşme biçimlerini yeniden programladığını gösteriyor.
Metabolizma amino asitlere kayıyor
Metabolomik analizi tamamlayıcı bir hikâye anlattı. Yaklaşık 1.400 tespit edilen metabolitin içinde, 260’ı dirençli hücrelerde anlamlı şekilde değişmişti. İstatistiksel modeller dirençli ile dirençsiz hücreleri net şekilde ayırdı; bu da direnç için tutarlı bir metabolik imza olduğunu gösteriyor. Değişmiş metabolitler bilinen biyokimyasal yollar üzerine haritalandığında, birkaç yol öne çıktı. En güçlü etkilenen yolların birçoğu amino asitlerle—proteinlerin yapı taşları—ilişkiliydi; özellikle alanin, aspartat, glutamat, sistein, metionin ve glutatyon içeren yollar. DNA ve RNA için önemli olan purin ve pirimidin metabolizması ile bazı yağların işlenmesi gibi diğer ağlar da bozulmuştu; bu da direncin geniş bir metabolik yeniden şekillenmeyle bağlantılı olduğunu vurguluyor.
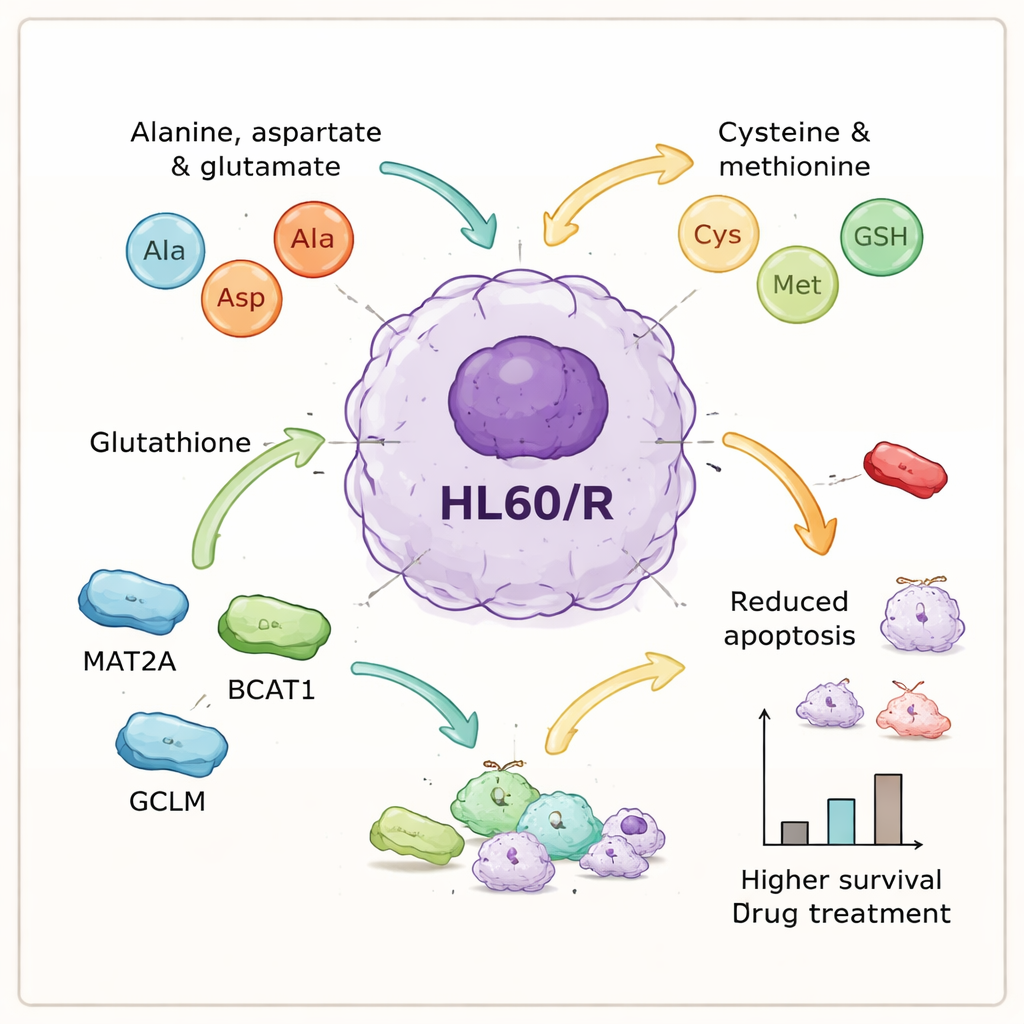
Kanser hücrelerinin dayanmasına yardımcı olan kilit moleküler oyuncular
Protein ve metabolit verilerini bütünleştirerek yazarlar, dirençte merkezi görünen amino asit ilişkili süreçlerin bir kümesine odaklandılar. Bu yolaklarla bağlantılı altı proteini—GOT1, GPX1, AHCY, MAT2A, BCAT1 ve GCLM—daha yakından incelediler. Laboratuvar testleri, beşinin dirençli hücrelerde daha bol bulunduğunu doğruladı; bu, amino asit işleme faaliyetinin artmış olduğu fikriyle tutarlıydı, oysa bir antioksidan enzim olan GPX1 azalmıştı. Nedensellik ilişkisini araştırmak için ekip, dirençli hücrelerde yukarı düzenlenmiş üç proteini—MAT2A, BCAT1 ve GCLM—küçük girişimli RNA’lar kullanarak azalttı. Bu proteinler baskılandığında, hücreler tedavi sonrası anlamlı ölçüde daha fazla programlı hücre ölümü geçirdi; yani adriamisine karşı kazandıkları büyük orandaki korumayı kaybettiler.
Gelecekteki tedaviler için anlamı
Bir arada değerlendirildiğinde, bu bulgular adriamisine dirençli AML hücrelerinin yalnızca tekil mutasyonlardan dolayı değil, iç kimyalarını yeniden şekillendirerek hayatta kaldığını; amino asit metabolizmasının bu yeniden programlamanın merkezi bir düğümü olduğunu gösteriyor. Hücreler belirli amino asit ve glutatyon yollarına daha fazla kaynak yönlendirerek strese daha iyi göğüs geriyor, hasarı onarıyor ve kemoterapiye maruz kaldıklarında ölmekten kaçınıyor gibi görünüyor. Uzman olmayanlar için ana mesaj şu: direnç rastgele değildir; ölçülebilir ve potansiyel olarak hedeflenebilir örüntüler izler. Uzun vadede MAT2A, BCAT1 veya GCLM gibi belirli amino asit işleyen proteinleri hedef alan ilaçlar adriamisin veya benzeri ajanlarla eşleştirilerek, akut miyeloid lösemili hastalarda direncin önlenmesi veya aşılması için klinisyenlere yeni araçlar sunabilir.
Atıf: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Anahtar kelimeler: akut miyeloid lösemi, ilaç direnci, adriamisin, amino asit metabolizması, çoklu omikler