Clear Sky Science · tr
Üçlü negatif meme kanseri hücre hatlarında anjiyogenez ve matriks metalloproteinaz sinyalini hedef alan gümüş nanoparçacıkların radyo-hassaslaştırıcı etkileri
Zorlu Meme Kanserlerini Daha Savunmasız Hale Getirmek
Üçlü-negatif meme kanseri, tedavisi en zor meme kanserlerinden biridir. Genellikle hızlı büyür, erken yayılır ve birçok modern ilacın hedef aldığı tipik moleküler “tutamaklardan” yoksundur. Radyasyon sıklıkla tedavinin bir parçasıdır, ancak bu tümörler dirençli olabilir. Bu çalışma basit ama ilgi çekici bir soruyu gündeme getiriyor: çok küçük gümüş parçacıkları, radyasyonun etkisini artırırken tümörün yeni kan damarları oluşturma ve yayılma yeteneğini de yavaşlatabilir mi?
Radyasyona Yardımcı Minik Gümüş Parçacıklar
Araştırmacılar, milyarda bir metre ölçeğinde ultra-küçük gümüş küreleri olan gümüş nanoparçacıklara odaklandı. Gümüş yoğun olduğundan ve X ışınlarıyla güçlü etkileşime girdiğinden, bu parçacıklar biriktikleri yerde radyasyonun etkisini yoğunlaştırabilir. Ekip, iki yaygın laboratuvar modeli olan üçlü-negatif meme kanseri hücreleriyle çalıştı ve bunları kanserli olmayan bir meme hücre hattıyla karşılaştırdı. Önce gümüş nanoparçacıkların tek başına ne kadar toksik olduğunu test ettiler ve kanser hücrelerinin normal hücrelere göre çok daha düşük dozlarda öldüğünü buldular; bu da kullanışlı bir tedavi penceresi olduğunu düşündürüyor. Parçacıklar ve radyasyonun nasıl etkileştiğini matematiksel yöntemlerle analiz ederek, ikisinin birlikte uygulanmasının tek başına uygulanan her bir tedaviden belirgin şekilde daha güçlü bir kanser öldürücü etki ürettiğini gösterdiler.
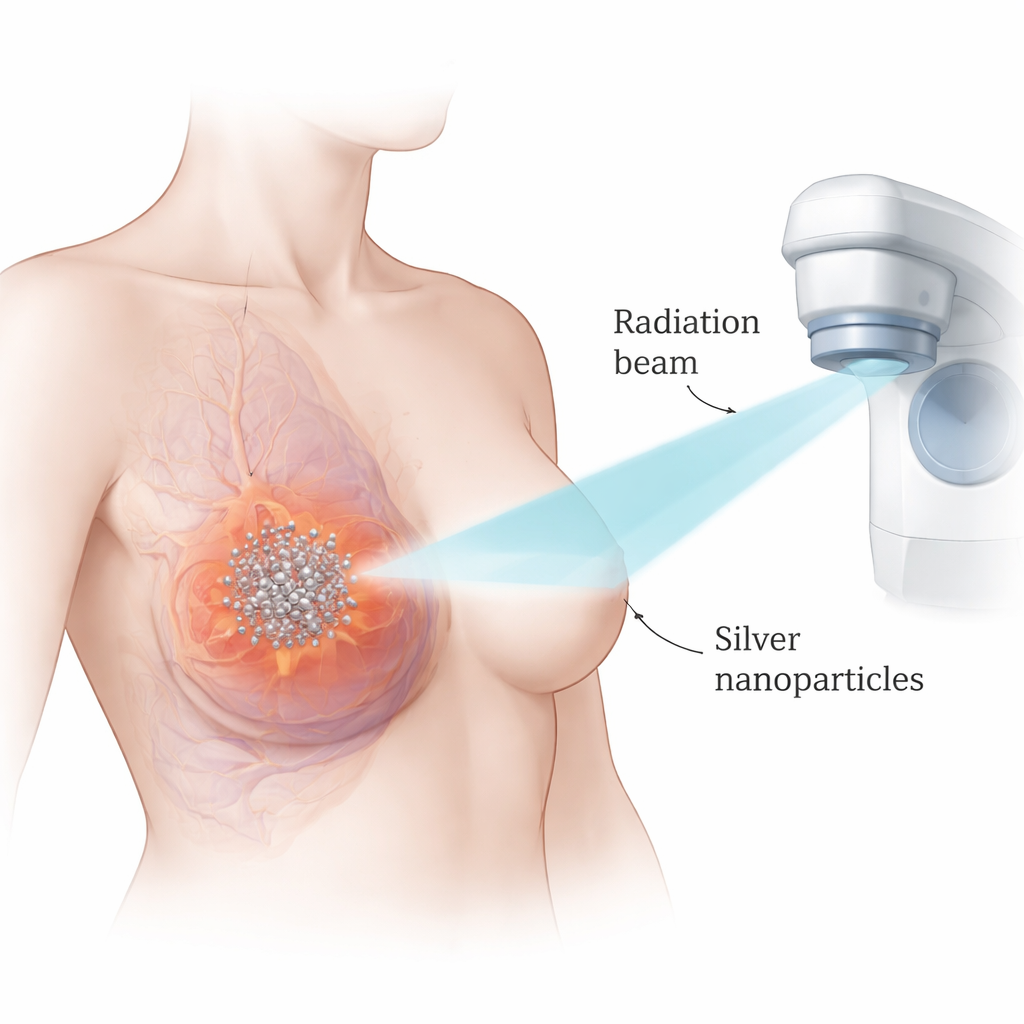
Kanser Hücrelerini Kendini İmha Etmeye Zorlama
Sırada, birleşik tedavinin hücreleri nasıl öldürdüğünü incelediler. Programlı hücre intiharı biçimi olan apoptozu ölçtüler ve reaktif oksijen türleri (ROS) olarak bilinen yüksek derecede reaktif moleküllerin birikimini izlediler. Radyasyonun kısmen DNA’ya zarar vererek ROS ürettiği zaten bilinmektedir. Her iki üçlü-negatif hücre hattında da gümüş nanoparçacıklar tek başına apoptozu ve ROS seviyelerini yükseltti; radyasyon da aynı şekilde artırdı—ancak birlikte kullanıldıklarında her iki ölçütü de dramatik biçimde daha yüksek seviyelere taşıdılar. Bu, daha fazla kanser hücresinin düzensiz hasarlı bir durumda kalıp bazen nüks veya direnci teşvik etmesi yerine, düzenli bir kendini yok etme moduna itilmesi demektir.
Kan Damarını Kesme ve Yayılmayı Yavaşlatma
Tümörler oksijen ve besin sağlamak için kan damarlarına güvenir ve agresif kanserler bazen kendileri de damar benzeri yapılar taklit edebilir. Ekip, tümör damarlarını oluşturup stabilize etmede rol oynayan iki önemli moleküler anahtarı, VEGFR2 ve Tie2’yi inceledi. Her iki hücre hattında da gümüş nanoparçacıklar bu genlerin aktivitesini azalttı ve radyasyonla kombinasyonları onları daha da baskıladı. Ayrıca, kanser hücrelerinin çevre dokuyu parçalayarak göç etmesine yardımcı olan iki enzim olan MMP-2 ve MMP-9’u incelediler. Hücre modellerinden birinde hem radyasyon hem de gümüş nanoparçacıklar bu enzimleri düşürdü; birleşik tedavi ise en güçlü etkiye sahipti. Araştırmacılar, hücrelerin bir kültür kabında oluşturulmuş yapay bir “çizik”e doğru hareketini izlediklerinde ve eş-kültürde damar benzeri tüplerin ne kadar iyi oluştuğunu test ettiklerinde, kombinasyon tedavisi göçü ve tüp oluşumunu en açık şekilde yavaşlattı.
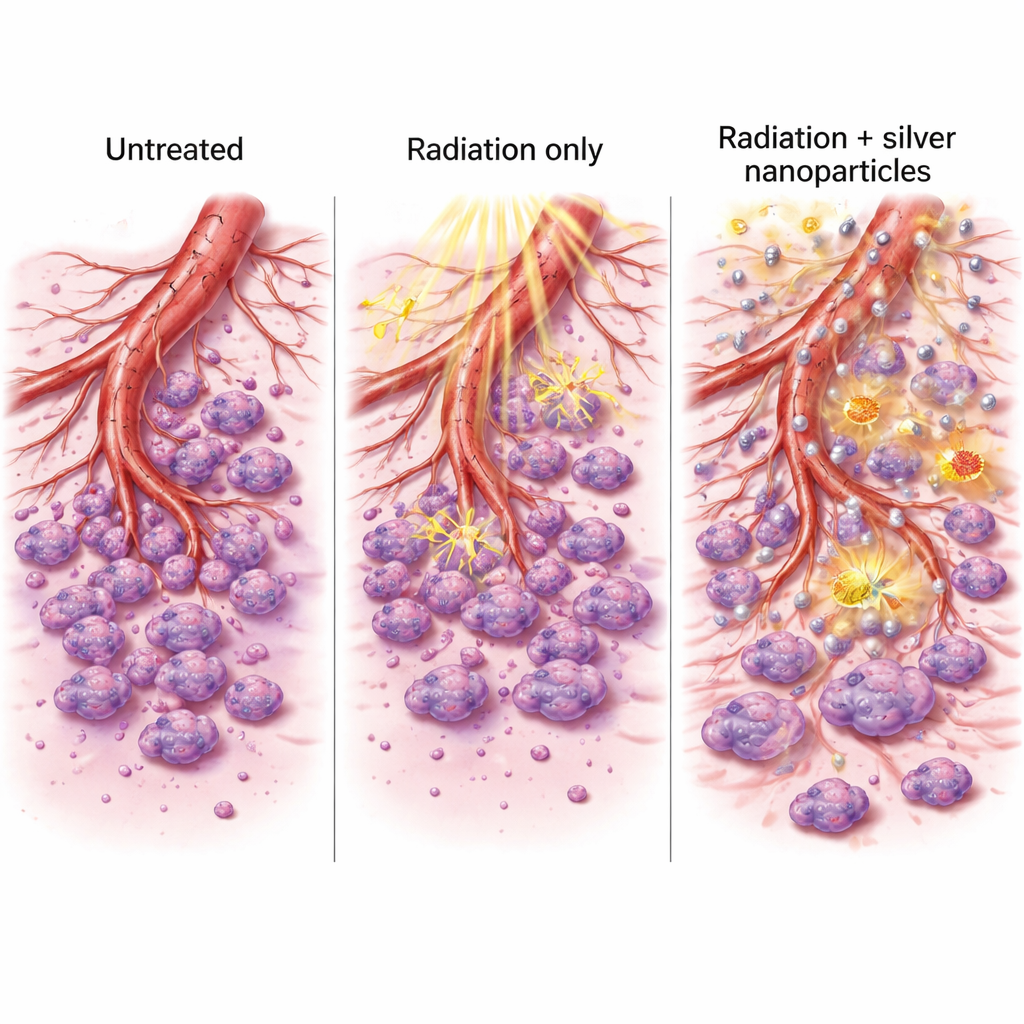
Bu Değişiklikler Neden Önemli
Yeni kan damarı oluşumunu teşvik eden genleri ve hücrelerin istila etmesine yardımcı olan enzimleri baskılayarak, gümüş artı radyasyon kombinasyonu yalnızca kanser hücrelerini öldürmekle kalmadı. Aynı zamanda tümörlerin büyüme ve yayılma için kullandığı destek sistemlerini de bozdu. Tedavi edilen hücreler laboratuvar kaplarındaki yaraları kapatma yeteneğinde azalma ve erken damarları andıran dallanmış ağlar oluşturma kapasitesinde gerileme gösterdi. Hücre ölümünde ve ROS üretimindeki güçlü artışla birlikte bu etkiler iki yönlü bir fayda öneriyor: tümöre yönelik daha güçlü doğrudan saldırı ve gelecekteki büyüme ile metastaz için daha zayıf araçlar.
Bu Hastalar İçin Ne Anlama Gelebilir
Şu an için bu sonuçlar hastalardan değil, laboratuvarda yetiştirilen kanser hücrelerinden geliyor. Yine de umut verici bir tablo çiziyorlar. Gümüş nanoparçacıklar radyosensitizatör görevi görerek standart radyasyon terapisini üçlü-negatif meme kanseri hücrelerine karşı daha etkili hale getirdi. Aynı zamanda, tümörün kan temin hatları kurma ve yakın dokuyu istila etme yeteneğini kısmen boğuyormuş gibi görünüyordu. Gelecekte yapılacak hayvan ve klinik çalışmalar, bu parçacıkların tümörlere güvenli ve seçici şekilde verilebileceğini doğrularsa, doktorların daha düşük radyasyon dozları kullanırken daha iyi sonuç almalarına yardımcı olabilir ve meme kanserinin en zorlu formlarından biriyle mücadelede yeni bir yol sunabilir.
Atıf: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Anahtar kelimeler: üçlü-negatif meme kanseri, gümüş nanoparçacıklar, radyasyon terapisi, anjiyogenez, metastaz