Clear Sky Science · tr
Acı tat reseptörleri aracılığıyla in vitro Pt-tabanlı kemoterapötiklere chemosensör yanıtları, acı tat bozuklukları için yeni bir mekanizmayı ortaya koyuyor
Neden kanser ilaçları aniden her şeyin kötü tadını aldırabilir
Kanser hastaları genellikle kemoterapi başladıktan kısa süre sonra yiyeceklerin garip şekilde acı veya metalik tadı olduğunu bildirir. Bu yalnızca yemekleri bozmakla kalmaz: iştahı azaltabilir, kilo kaybını teşvik edebilir ve hastaların en çok güce ihtiyaç duydukları dönemde yaşam kalitesini düşürebilir. Bu çalışma, görünüşte basit ama büyük pratik sonuçları olan bir soruyu soruyor: yaygın platin-tabanlı kemoterapi ilaçları tadımızı tam olarak nasıl etkiliyor ve bu etki tedavinin etkinliğini zayıflatmadan güvenli bir şekilde azaltılabilir mi?
Ağız ve bağırsaktaki “acı algılayıcıların” gizli rolü
Dilimiz ve sindirim sistemimiz, potansiyel olarak zararlı maddeler hakkında bizi uyarmak için tasarlanmış acı tat reseptörleriyle kaplıdır. TAS2R olarak bilinen bu sensörler yalnızca tat tomurcuklarıyla sınırlı değildir; mide hücrelerinde de bulunurlar. Araştırmacılar, acılığı in vitro algılayan bir sistem gibi davranan insan gastrik hücre hattı (HGT-1) kullandılar: acı reseptörler aktive edildiğinde hücreler daha fazla proton (asit) pompalıyor ve bu, hücre içi proton indeksi adlı bir okumada ölçülebiliyor. Bu hücreleri yaygın kullanılan iki platin-tabanlı kanser ilacı—karboplatin ve sisplatin—ile temas ettirerek, ekip insanlar toksik bir bileşiği tatmaya zorlamadan bu ilaçların insan hücreleri için ne kadar “acı” göründüğünü güvenli şekilde araştırabildi. 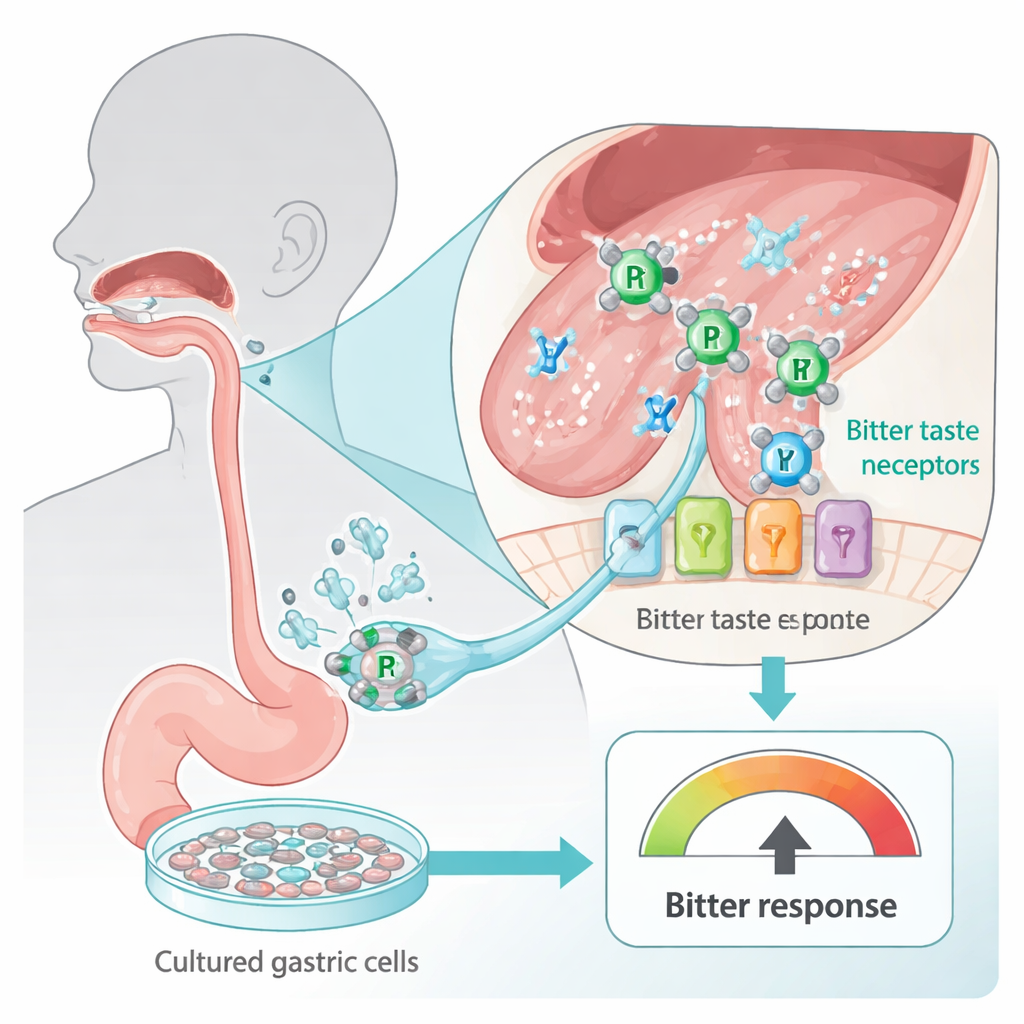
Hücrelere acı gelen kemoterapi ilaçları
Gastrik hücreler klinikteki ilgili konsantrasyonlarda karboplatin ve sisplatine maruz bırakıldığında, her iki ilaç da belirgin, doz-bağımlı bir acı benzeri yanıt tetikledi: doz arttıkça hücresel reaksiyon güçlendi. Bununla birlikte sisplatin, yaygın terapötik doz oranları (yaklaşık 1:4) göz önüne alındığında karboplatinden daha yoğun bir yanıt üretti; bu da hastalardaki acı tat sorunlarına daha fazla katkıda bulunabileceğini düşündürüyor. Genetik düzeyde bu ilaçlara maruz kalma, hücrelerde birden fazla acı reseptör geninin aktivitesini değiştirdi; bu, platin ilaçlarının tek bir “acı anahtarı” üzerinde etkili olmayıp acı algılama sistemini geniş ölçüde yeniden şekillendirdiğini gösteriyor. Bu reseptörler arasında TAS2R4 ve TAS2R5, hem yüksek etkinlikleri hem de tedaviden güçlü şekilde etkilenmeleriyle öne çıktı.
Acı sinyallerini kapatmak ve doğal bir acı bloke ediciyi test etmek
Hangi reseptörlerin en önemli olduğunu belirlemek için ekip belirli acı reseptörlerini seçici olarak devre dışı bıraktı. TAS2R4'ün ortadan kaldırılması (knockout) veya TAS2R5'in susturulması (knockdown) her biri karboplatin ve sisplatine karşı acı benzeri yanıtı azalttı ve bu reseptörlerin ilaçları algıladığını doğruladı. Bilim insanları ardından ümit verici bir karşı önlem test ettiler: Kuzey Amerika bitkisi Herba Santa’dan izole edilmiş olan ve diğer bileşiklerin acılığını gizlediği bilinen bir flavanon olan homoeriodictyolün sodyum tuzu (Na-HED). Na-HED platin ilaçlarla birlikte eklendiğinde, hücresel acı yanıtını belirgin şekilde baskıladı—karboplatin ve sisplatin için yaklaşık olarak dörtte üç oranında—ve kendi başına hücrelere zarar vermedi. Bu, Na-HED’in acı reseptörleri üzerinde doğrudan etki ederek kemoterapi ilaçlarının tetiklediği sinyali zayıflatabileceğini gösteriyor.
Acı algılama ve ilaç alınımının kesiştiği nokta
Platin kemoterapinin neden acı tadı verebileceğini açıklamanın ötesinde, çalışma beklenmedik bir dönemeç ortaya koyuyor: aynı acı reseptörler ayrıca bu ilaçların hücrelere ne kadar girdiğini de etkiliyor gibi görünüyor. Araştırmacılar, tedavi sonrası hücre içindeki platin içeriğini yüksek duyarlılıklı kütle spektrometrisi ile ölçtüler. TAS2R4 veya TAS2R43 gibi belirli reseptörlerden yoksun hücreler normal hücrelerden daha fazla platin biriktirdi; bu, sağlam reseptörlerin bu toksik ajanların hücre girişini veya tutulmasını sınırlamaya yardımcı olduğunu düşündürüyor. Na-HED karboplatin alınımını değiştirmedi, ancak sisplatinin hücreye girişini azalttı ve çözeltide sisplatin ile doğrudan moleküler etkileşim gösterdi. Bu, bir acı gizleyici bileşiğin bazı durumlarda tadı alan hücreler veya tükürük bezleri gibi lokal dokular üzerindeki ilacın etkisini de değiştirebileceğini ima ediyor. 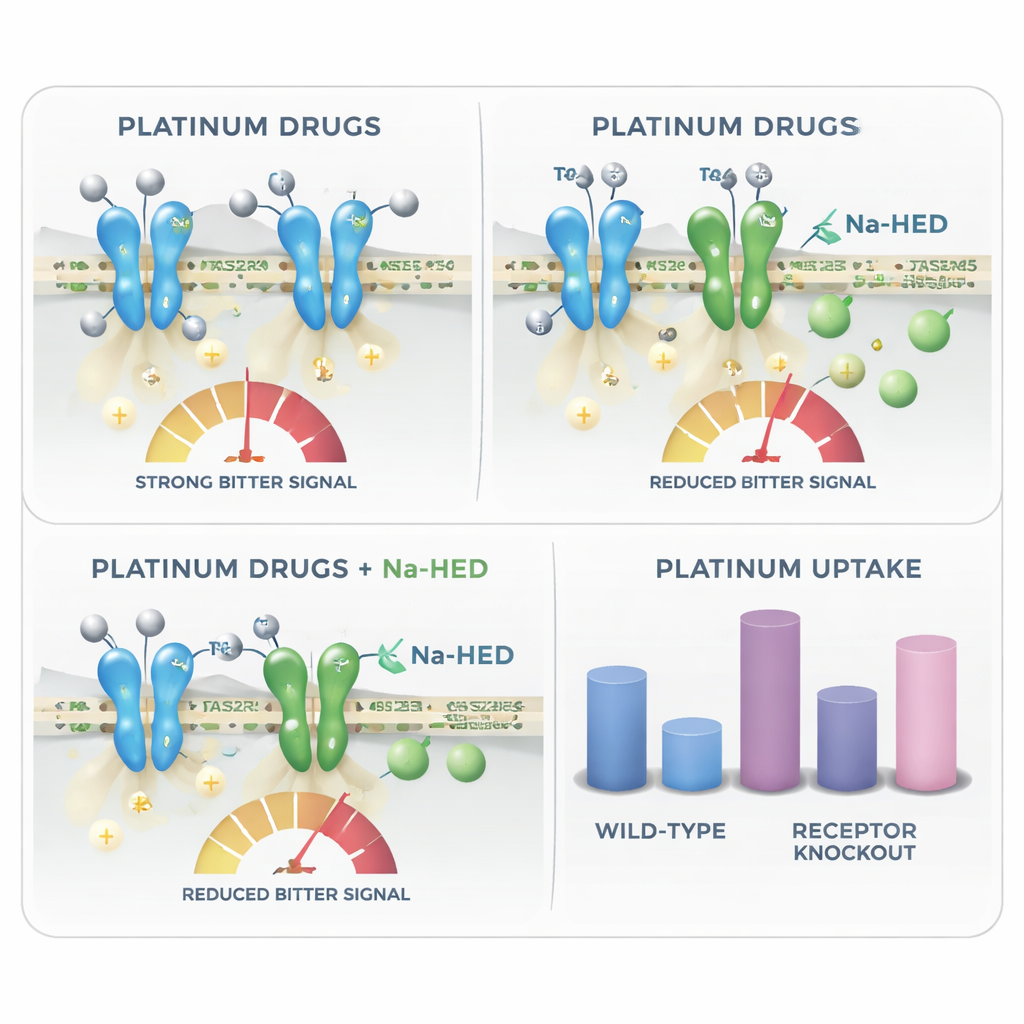
Kemoterapi sırasında daha nazik tat deneyimlerine doğru
Hastalar için ana çıkarım ümit verici: platin-tabanlı kemoterapi, yalnızca dilde değil bağırsak benzeri hücrelerde de bulunan acı reseptörlerini doğrudan aktive ederek acı tat sorunlarını tetikliyor gibi görünüyor. Bu açıdan sisplatin özellikle güçlü görünüyor. Çalışma, Na-HED’in kontrollü bir hücre sisteminde bu acı sinyalini önemli ölçüde azaltabildiğini ve sisplatinin lokal alınımını sınırlayabileceğini gösteriyor. Bu bulguların insanlarda doğrulanması gerekmekle birlikte, vücut genelindeki kanserle savaşan ilaçların etkisini bozmayacak şekilde, Na-HED içeren gelecekteki “çıkar-çalkala” ağız uygulamalarına doğru bir yol gösteriyor; bu tür uygulamalar sert acı ve metalik hisleri yumuşatabilir.
Atıf: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Anahtar kelimeler: kemoterapi tat değişiklikleri, acı tat reseptörleri, sisplatin ve karboplatin, acı gizleyici bileşikler, kanser hastası beslenmesi