Clear Sky Science · tr
Presenilin-1 mutasyonu taşıyan insan iPSC kaynaklı nöronlarda mitokondriyal disfonksiyon ve Ca2+ düzensizliği stres altında MCU-1 bağımsız bir mekanizma ile ortaya çıkıyor
Alzheimer hastalığı açısından neden önemli
Alzheimer hastalığı sıklıkla beyindeki yapışkan protein plaklarıyla tanımlanır, ancak hafıza zayıflamadan çok önce sinir hücrelerinin içindeki küçük “enerji santralleri” — mitokondriler — ve kalsiyum iyonlarının yönetimi bozulmaya başlamış olabilir. Bu çalışma, iyi bilinen ailesel bir Alzheimer mutasyonunu taşıyan bir kişinin deri hücrelerinden türetilen insan nöronlarını kullanarak basit ama kritik bir soruyu soruyor: enerji üretimi ve kalsiyum dengesi ne kadar erken ve hangi biçimlerde bozulmaya başlıyor?
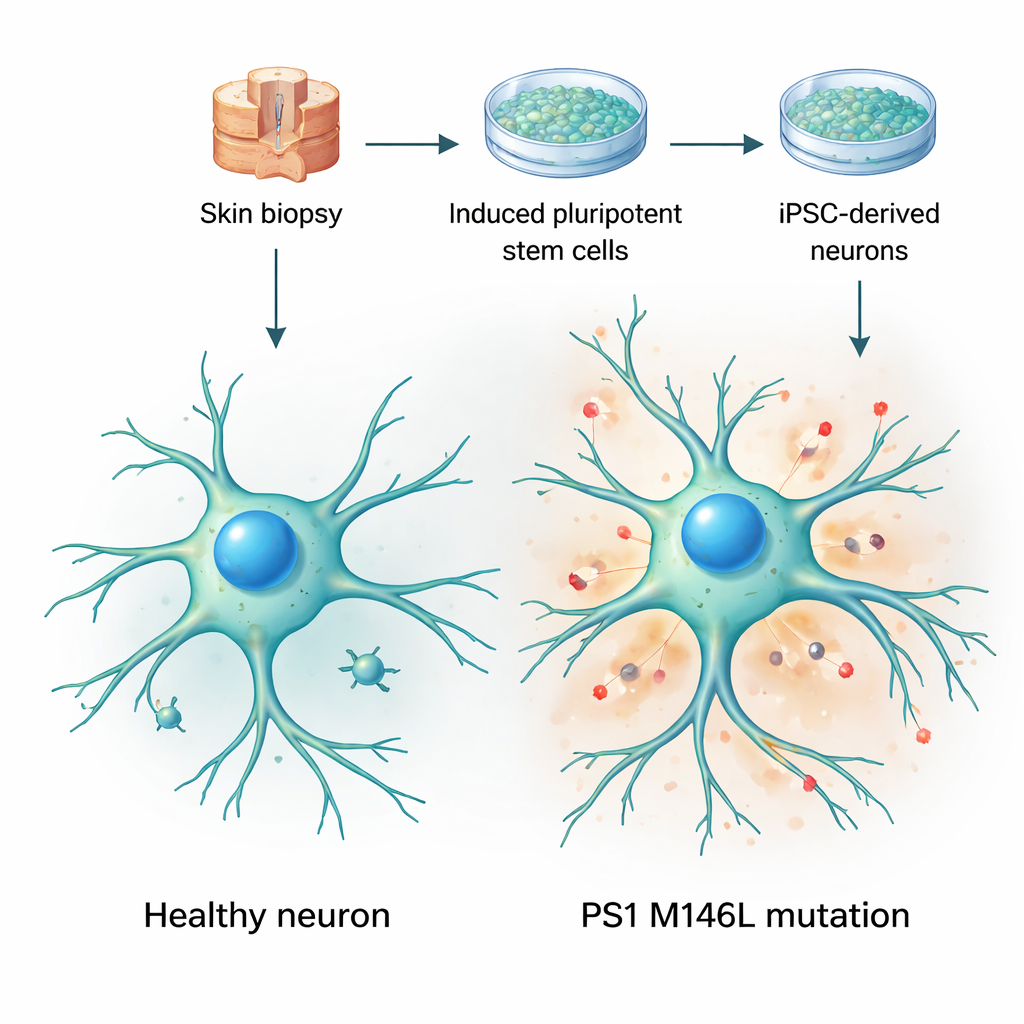
Deri hücrelerini canlı beyin modellerine dönüştürmek
Araştırmacılar iki kadından alınan deri biyopsileriyle başladılar: biri sağlıklı bir gönüllü, diğeri ise Arjantinli erken başlangıçlı Alzheimer geçmişi olan bir ailede görülen M146L adlı presenilin‑1 mutasyonunu belirti göstermeyen taşıyıcı. Deri hücrelerini indüklenmiş pluripotent kök hücrelere (iPSC) dönüştürdüler — neredeyse herhangi bir dokuya dönüşebilen hücreler — ve sonra bunları nöronlara yönlendirdiler. Kültürde birkaç hafta içinde bu hücreler tipik nöronal morfolojiler kazandı, uzun dallanan uzantılar geliştirdi ve standart nöronal belirteçleri ifade etti. Önemli olarak, kontrol ve mutasyonlu hücreler benzer hızlarda olgunlaştı ve genel olarak sağlıklı göründü; bu da ekibin belirgin hücre kaybı veya hasarı yerine ince işlevsel değişikliklere odaklanmasına olanak tanıdı.
Elektriksel sinyaller ve kalsiyum baskı altında
Sinir hücreleri birçok hücresel süreç için hızlı bir aç‑kapa anahtarı gibi davranan yüklü bir atom olan kalsiyumun sıkı kontrolüne dayanır. Araştırmacılar, floresan boyalar kullanarak hücreler elektriksel olarak potasyumla uyarıldığında veya sinyalleştirici moleküllerle aktive edildiğinde kalsiyum düzeylerinin nasıl değiştiğini izlediler. Basit depolarize edici uyarı altında M146L mutasyonunu taşıyan nöronlar kontrol nöronlarına göre daha zayıf kalsiyum artışları sergiledi; bu durum normalde kalsiyum girişini yönlendiren elektriksel ve iyonik gradyanların sürdürülmesinde sorunlara işaret ediyor. Ancak araştırmacılar daha stresli bir durumu tetiklediklerinde — endoplazmik retikulumdaki iç depolardan kalsiyumun sızdırılmaya zorlanması — fark daha belirgin hale geldi. Bu strese yanıt olarak mutasyonlu nöronlardaki mitokondriler, kontrol hücrelerindekine göre belirgin biçimde daha az kalsiyum aldı; bu da tehlikeli kalsiyum dalgalanmalarını tamponlama yeteneğinin azaldığını gösteriyor.
Enerji kullanımını kalsiyum dengesinden ayırmak
Bu değişmiş kalsiyum yönetiminin hücre metabolizmasını nasıl etkilediğini anlamak için araştırmacılar nöronların ne kadar oksijen tükettiğini ölçtüler — mitokondriyal aktivitenin doğrudan bir göstergesi. Şaşırtıcı bir şekilde, M146L mutasyonlu nöronlar daha fazla soluk aldı: bazal ve maksimum oksijen tüketim oranları ile ATP üretimine bağlı oksijen miktarı kontrol hücrelerinden daha yüksekti. Buna karşın oksijen kullanımının ATP üretimine bağlanma verimliliği benzer görünüyordu ve mitokondri sayısında ya da ana ATP üreten enzimlerde artış yoktu. Bunun yerine mutasyonlu nöronlardaki mitokondriler daha uzun ve tübülerdi ve mitofusin‑1 adlı bir füzyon proteininde artmış düzeyler vardı; bu desen genellikle kronik, düşük düzeyli stres altındaki hücrelerde görülür. Bu hiperaktif, uzamış mitokondriler aynı zamanda daha fazla reaktif oksijen türü üretiyordu — düzgün kontrol edilmezse proteinlere ve DNA'ya zarar verebilecek kararsız moleküller.
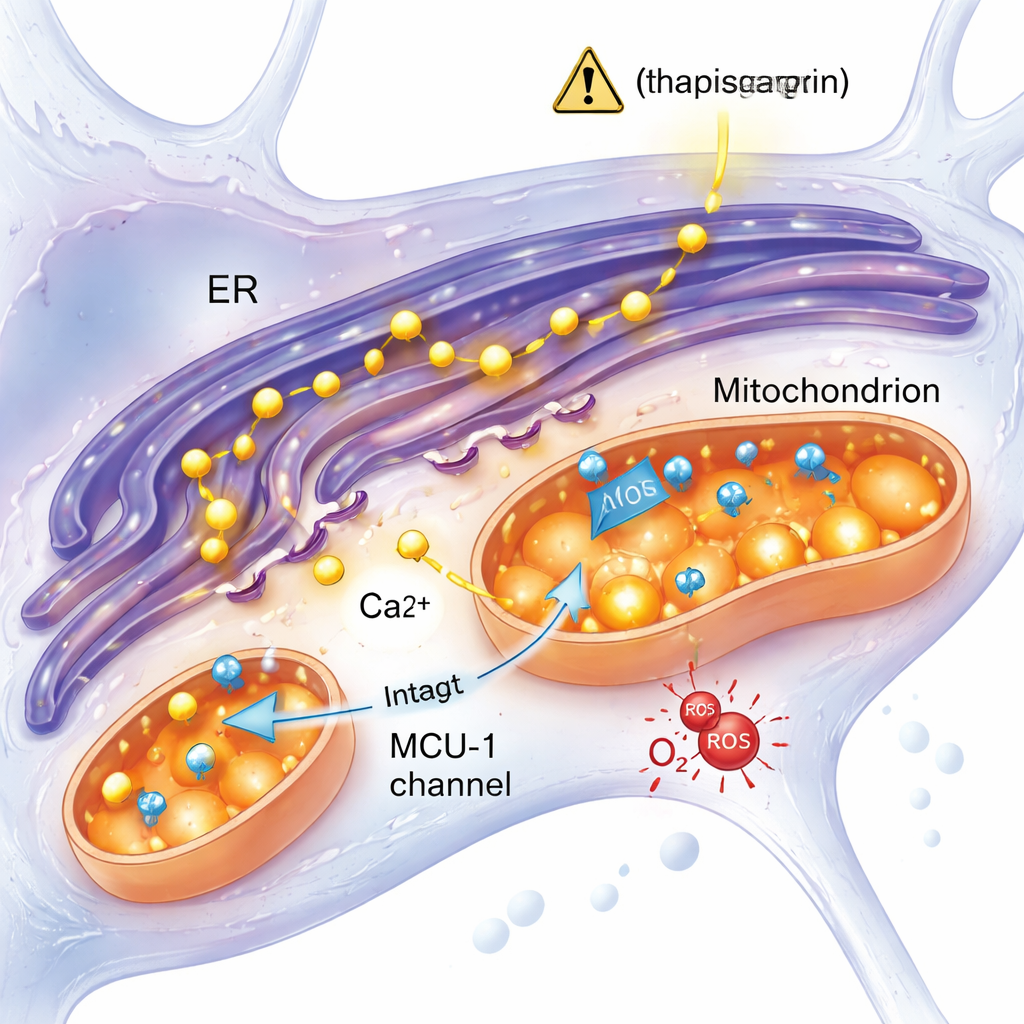
Önemli bir kalsiyum kanalından bağımsız bir stres yanıtı
Alzheimer araştırmalarında öne çıkan bir fikir, endoplazmik retikulumdan aşırı kalsiyumun mitokondrilere mitokondriyal kalsiyum uniportörü (MCU‑1) adlı bir kanal üzerinden akarak onları aşırı yüklediği ve disfonksiyona yol açtığıdır. Bu çalışma bu fikri doğrudan test etti. Ekip MCU‑1'i spesifik bir inhibitörle bloke ettiğinde, hem kontrol hem de mutasyonlu nöronlarda mitokondriyal kalsiyum alımında güçlü azalmalar görüldü; bu da kanalın her iki grupta da çalıştığını doğruladı. Dahası, kalsiyum salımı IP3 reseptörünü içeren daha fizyolojik bir yol aracılığıyla tetiklendiğinde — başka bir önemli kalsiyum kapısı — mutasyonlu ve kontrol hücreleri benzer yanıtlar verdi. Bu sonuçlar kırık bir MCU‑1 kanalından ziyade endoplazmik retikulum ile mitokondriler arasındaki fiziksel ve fonksiyonel temasların veya etkileşimlerinin diğer yönlerinin mutasyonlu nöronlarda değiştiğini düşündürüyor.
Hastalıkın anlaşılması ve tedavisi için ne anlama geliyor
Bir araya getirildiğinde bulgular, PS1 M146L Alzheimer mutasyonunu taşıyan insan nöronlarının dinlenme halinde normal göründüğü ancak stres altında anormal tepki verdiği bir tablo ortaya koyuyor. İç depolar ani olarak salındığında mitokondrileri yeterince kalsiyum almıyor, buna karşın daha fazla oksijen tüketip daha çok reaktif oksijen türü üreterek daha sıcak çalışıyorlar — sanki maliyetli bir telafi moduna kilitlenmiş gibiler. Bu durum klinik semptomlardan önce yaşayan insan kaynaklı nöronlarda ortaya çıktığı için çalışma, bozulmuş kalsiyum sinyalleşmesi ve erken mitokondriyal aşırı çalışma olaylarının Alzheimer’da yalnızca geç dönemde ortaya çıkan yan ürünler değil, başlangıçtaki olaylar olduğu düşüncesini destekliyor. Uzman olmayanlar için temel mesaj, kalsiyum sinyalleri ile mitokondriyal enerji üretimi arasındaki dengenin korunmasının, daha iyi bilinen amiloid plaklara yönelik hedeflemeler kadar hastalığın önlenmesinde merkezi olabileceğidir.
Atıf: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
Anahtar kelimeler: Alzheimer hastalığı, mitokondri, kalsiyum sinyalleşmesi, presenilin-1 mutasyonu, iPSC kaynaklı nöronlar