Clear Sky Science · tr
2,5-disubstitüe-1,3,4-oksadiazol analoğlarının yapısal ve hesaplamalı destekli geliştirilmesi: aktif LOX, üreaz ve α-glukozidaz inhibitörleri olarak
Yaygın Hastalıklarla Mücadele İçin Yeni Kimyasal Araçlar
Ülserlerden böbrek taşlarına, diyabetten kronik iltihaba kadar birçok gündelik sağlık sorunu, vücudumuzdaki aşırı aktif enzimlerin etkisiyle ilerler. Bu çalışma, söz konusu üç enzimi küçük frenler gibi durduran yeni tasarlanmış bir küçük molekül ailesini inceliyor. Araştırmacılar yapıları ayarlayıp onları laboratuvarda ve bilgisayar ortamında test ederek, gelecekte daha etkili ve daha güvenli ilaçlar için zemin hazırlamayı amaçlıyor. 
Bu Enzimlerin Neden Önemli Olduğu
Ekip, sağlıkta çok farklı ama eşit derecede önemli rollere sahip olan üç enzim hedefine odaklandı. Üreaz üreyi parçalamaya yardımcı olur; belirli bakterilerde veya dokularda aşırı aktif hale geldiğinde mide ve idrar yolu ülserlerine, böbrek taşlarına ve hatta yüksek tansiyona katkıda bulunabilir. Alfa‑glukozidaz bağırsak hücrelerinin yüzeyinde yer alır ve karmaşık karbonhidratları glikoza çevirir; bunu engellemek tip 2 diyabette kan şekeri kontrolüne yardımcı olmanın iyi yerleşmiş bir yoludur. Lipooksijenaz (LOX) yağları iltihap, astım ve bazı kanser ilişkili süreçleri tetikleyen işaret moleküllerine dönüştürür. Bu enzimleri diğer sistemlere zarar vermeden azaltabilen ilaçlar bu yüzden oldukça aranan hedeflerdir.
Aday Moleküllerden Oluşan Bir Kütüphane Oluşturmak
Böyle ilaçları aramak için araştırmacılar 1,3,4‑oksadiazol halkasına bağlı bir piperidin birimi içeren 15 ilgili bileşikten oluşan bir dizi derlediler. Bu kimyasal iskelet modern bazı ilaçlarda zaten bulunuyor ve biyolojik hedeflerle iyi etkileşime girdiği biliniyor. Ekip, bu çekirdeğe bağlı “süslemeleri”—metil, etil, metoksi, benzil ve siklohekzil gibi küçük grupları—farklı pozisyonlarda değiştirerek 7a’dan 7o’ya etiketlenen küçük bir aday kütüphanesi oluşturdu. Her bir yapıyı kızılötesi ve nükleer manyetik rezonans spektroskopisi gibi standart analitik araçlarla doğrulayarak yapılan bileşiklerin tasarımlarıyla uyumlu olduğunu garanti ettiler.
Moleküllerin Enzimleri Ne Kadar Engellediğini Test Etmek
Her bileşik daha sonra saf LOX, üreaz ve alfa‑glukozidaz karşısında enzimin aktivitesini ne ölçüde yavaşlatabildiğini görmek için test edildi. Birkaç molekül öne çıktı. Alfa‑glukozidaz karşısında 7a ve 7n bileşikleri özellikle etkiliydi; laboratuvar testlerinde standart diyabet ilacı akarboza kıyasla düşük mikromolar konsantrasyonlarda yüksek inhibisyon yüzdeleri elde ederek daha iyi performans gösterdiler. LOX için 7a, 7h ve 7n çok güçlü aktivite sergiledi; bazı durumlarda doğal referans inhibitör kuersetinden daha iyi sonuçlar verdi. Üreaz testlerinde ise 7a ve özellikle 7l bileşikleri standart inhibitör tiyüreaya rakip oldu ya da hafifçe üstünlük sağladı; bu da gelecekte anti‑ülser veya taş karşıtı tedaviler için başlangıç bileşiği olabileceklerini düşündürüyor. 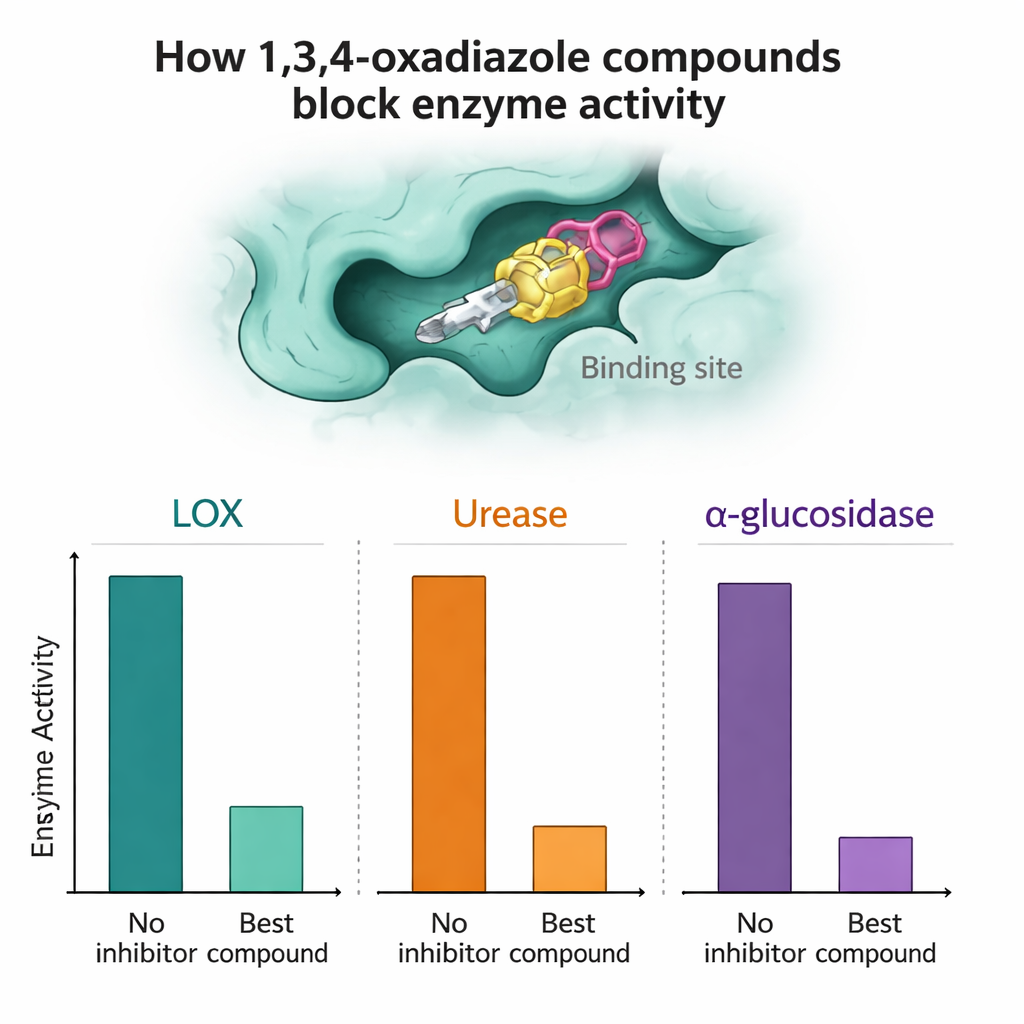
Yapıyı Performansa Bağlamak
7a–7o bileşikleri arasındaki tek farklılıklar çekirdek halka sisteminin etrafındaki küçük değişiklikler olduğundan, araştırmacılar basit yapı‑aktivite ilişkilerini haritalamaya başlayabildiler. Örneğin, bağlı bir halkadaki belirli “orto” pozisyonlara küçük karbojen‑grupların eklenmesi genellikle alfa‑glukozidaz veya LOX’u engelleme yeteneğini artırdı. Daha az uygun konumlara yerleştirilen bazı metoksi veya ester grupları gibi diğer sübsitüsyonlar ise aktiviteyi zayıflatma eğilimindeydi. Nedenini anlamak için ekip bilgisayar simülasyonları kullandı. Kuantum‑kimyasal hesaplamalar tüm moleküllerin termodinamik olarak stabil ve enzim ceplerine uyum sağlayacak kadar esnek olduğunu gösterdi. Docking çalışmaları—her molekülün enzimlerin üç boyutlu modellerine sanal olarak yerleştirilmesi—en aktif bileşiklerin aktif bölgelerde hidrojen bağları ile hidrofobik (yağ‑benzeri) etkileşimlerin karışımı yoluyla daha sıkı temas kurduğunu; zayıf adayların ise daha gevşek oturduğunu veya kritik temas noktalarını kaçırdığını ortaya koydu.
Gelecek İlaçlar İçin Anlamı
Günlük terimlerle, çalışma üç hastalık ilişkili “kilide” iyi uyan birkaç umut verici “anahtar” belirliyor ve bazı anahtarların diğerlerinden neden daha iyi döndüğünü atomik düzeyde açıklamaya başlıyor. Bu moleküllerin hiçbiri henüz ilaç olmaya hazır değil—güvenlik testleri, vücut içindeki davranışlarının optimize edilmesi ve hayvan ile insan çalışmalarına ihtiyaçları var. Ancak çalışma, 1,3,4‑oksadiazol–piperidin çerçevesinin diyabet, enflamatuar durumlar ve üreaz ilişkili bozuklukları hedefleyen gelecekteki tedaviler için verimli bir başlangıç noktası olduğunu gösteriyor. Titiz laboratuvar ölçümleri ile ayrıntılı bilgisayar modellemesinin kombinasyonu, bu adayları daha keskin ve etkili ilaçlara dönüştürmek için bir yol haritası sunuyor.
Atıf: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Anahtar kelimeler: enzim inhibitörleri, ilaç keşfi, oksadiazol bileşikleri, diyabet ve iltihap, üreaz ve lipooksijenaz