Clear Sky Science · tr
Fisyon mayasında lüminesans tamamlanmasıyla protein–protein etkileşimlerini tespit etmek için küresel bir tarama sistemi geliştirilmesi
Proteinlerin Gizli Yaşamını Aydınlatmak
Vücutta her kalp atışı, düşünce ve nefes hücrelerin içindeki proteinlerin bir araya gelmesine bağlıdır. Bu küçük ortaklıklar, protein–protein etkileşimleri, genlerin nasıl okunmasından hücrelerin strese nasıl yanıt verdiğine kadar her şeyi kontrol eder. Ancak bu ortaklıkların birçoğu geçici veya hassastır ve mevcut araçlarla tespit edilmeleri zordur. Bu çalışma, basit bir model organizma olan fisyon mayasında binlerce gizli protein bağlantısını aynı anda ortaya çıkarmak için yeni, yüksek hassasiyetli bir "ışık tabanlı" tarama sistemi tanımlıyor.
Protein Ortaklıklarını Görmeyi Zorlaştıran Nedir
Proteinler nadiren tek başına çalışır. Farklı zamanlarda farklı ortaklara tutunurlar, bazen sadece birkaç saniye için, ve davranışları kimyasal değişikliklerden veya hücre içindeki konumlarından etkilenebilir. Bu etkileşimleri incelemek için kullanılan geleneksel yöntemler ya proteinleri doğal ortamlarından çıkarır ya da her eşleşmeyi yakalamayan genetik numaralara dayanır. Sonuç olarak, hücrede kimlerin kimle etkileştiğine dair mevcut haritalar eksiktir. Yazarlar, canlı hücrelerde neredeyse her fisyon mayası proteinini tarayabilecek daha esnek, daha hassas bir sistem oluşturarak bu resmi iyileştirmeyi amaçladılar.
Dokunmayı Işığa Çevirmek
Yeni yaklaşımın merkezinde ışık yayan bir parçalanmış enzim bulunur. LgBiT adı verilen bir parça, araştırmacıların incelemek istediği "yem" proteine bağlanır. Diğer parça SmBiT ise her maya suşunda birer tane olacak şekilde birçok olası "av" ortağa bağlanır. Tek başlarına bu iki enzim parçası neredeyse etkileşmez. Ancak yem ve av proteinleri hücre içinde birbirine bağlandığında, iki parça birleşerek ışık veren çalışan bir enzim oluşturur; bu enzim bir kimyasal yakıt varlığında parlar. Her maya suşunun ne kadar ışık ürettiğini ölçerek ekip, hangi proteinlerin hücre içinde gerçekten buluştuğunu ve ne kadar güçlü etkileştiklerini belirleyebilir. Etiketin normal işlevi engellediği için ortakları kaçırmamak adına yem proteini iki versiyonda üretilir; LgBiT her iki uca da takılarak en az bir düzenlemenin işe yarama olasılığını önemli ölçüde artırır. 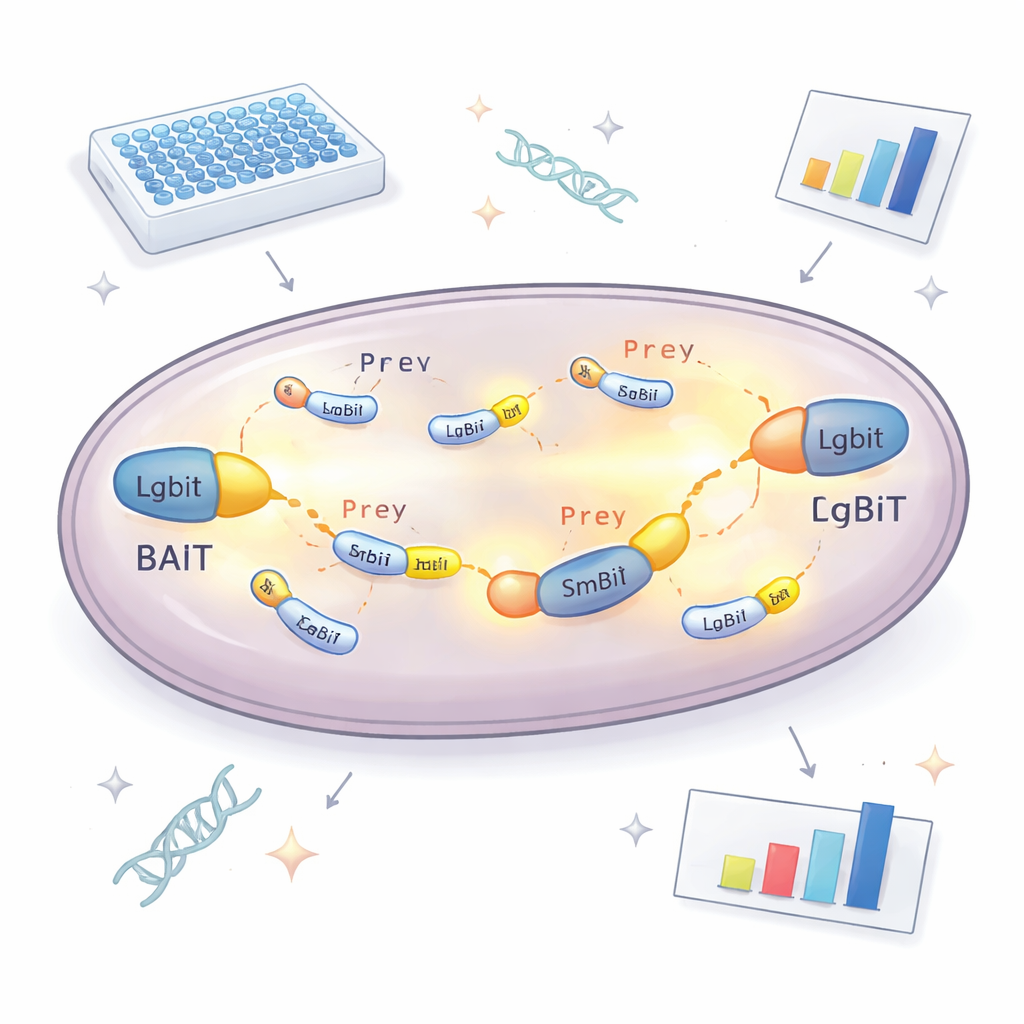
Bir Maya Kütüphanesi ve Suş Sistemi Tasarlamak
Bu platformu kurmak yalnızca zekice bir enzim gerektirmedi. Araştırmacıların ayrıca binlerce av proteinini kontrollü, tek kopyalı bir şekilde mayaya sokmaları gerekti. Av proteinleri için mayanın genomunda tanımlı bir noktaya giren ve kırmızı bir floresan belirteç taşıyan özel bir DNA vektörü tasarladılar. Bu kırmızı sinyalin parlaklığı, kaç kopya yerleştiğinin göstergesidir; ekip böylece güvenilir karşılaştırmalar için tam olarak bir kopyaya sahip kolonileri kolayca seçebilir. Ayrıca LgBiT’i yem proteininin başına veya sonuna yerleştiren, proteinlerin normal şekilde katlanıp hareket edebilmesi için esnek bağlayıcılarla ayrılmış özel yem vektörleri oluşturuldu. İki yem konstrüktu ve bir av konstrüktünü aynı anda barındıracak, yalnızca doğru birleşime sahip hücrelerin hayatta kalmasını sağlayan beslenme belirteçlerini kullanan dikkatle tasarlanmış maya suşları inşa edildi.
Sistemi Sınamaya Koymak
Tasarımın gerçekten algılamayı geliştirip geliştirmediğini kontrol etmek için bilim insanları önce iyi bilinen ortaklara sahip proteinleri inceledi. Sinyal gücünün ışık yayıcı etiketin nereye takıldığına güçlü bir şekilde bağlı olduğunu doğruladılar: bazı etkileşimler yalnızca LgBiT yem proteininin bir ucunda olduğunda ortaya çıkıyor, diğerinde değil. Her iki versiyonun birlikte ifade edilmesi ışık çıkışını artırdı ve bu da çift-yem stratejisinin zayıf veya yönelim duyarlı etkileşimleri yakalamayı kolaylaştırdığını kanıtladı. Sistem ayrıca geleneksel maya iki-hibrit yöntemleri için notoriöz olarak zor olan membrana bağlı proteinlerle olan temasları tespit etti. Bu doğrulamanın ardından ekip, Tfs1 adlı bir transkripsiyon ilişkili proteini yem olarak kullanarak genoma yönelik bir taramaya ölçekledi. 4.600’den fazla av proteini taranarak 31 güçlü aday bulundu; bunların arasında daha önce bilinen ortaklar ve çekirdek dışında mitokondri ve hücre yüzeyi gibi yerlerde bulunan birçok yeni eş bulunuyordu. 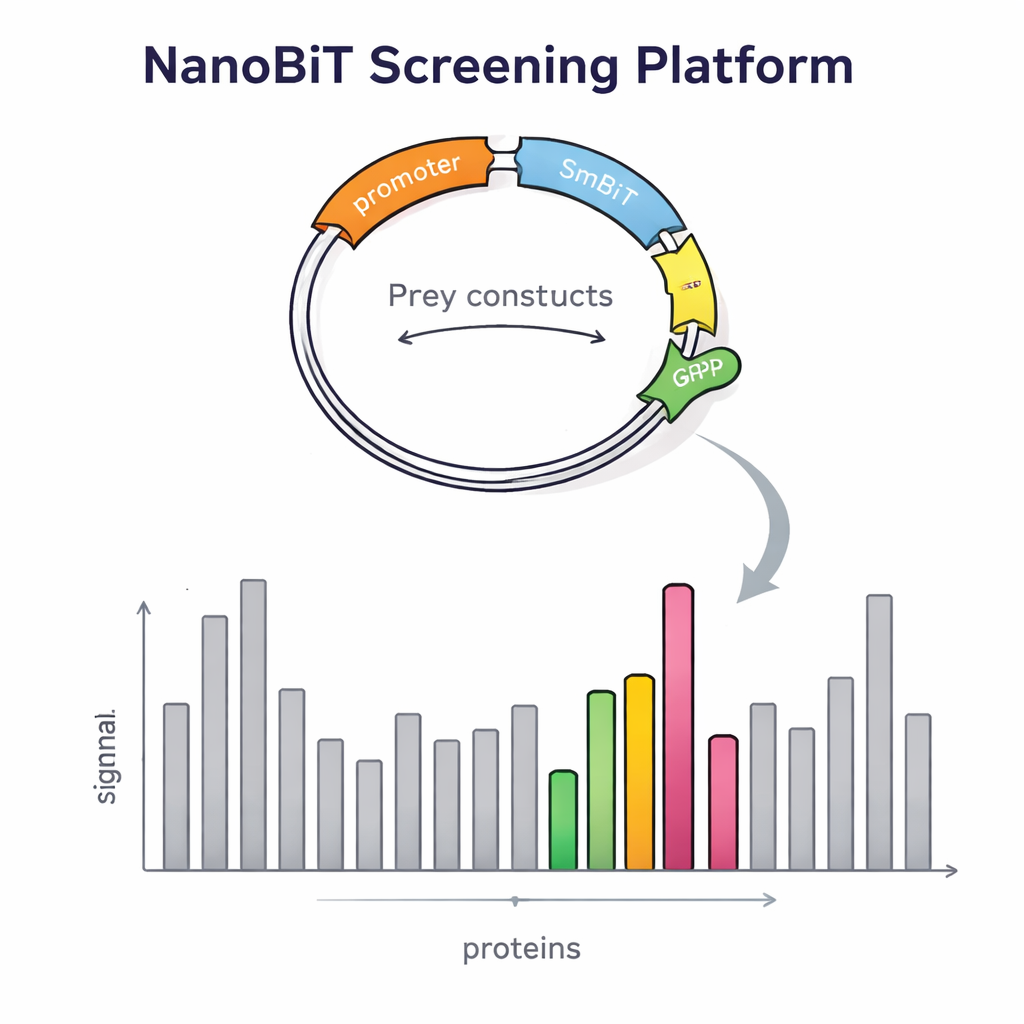
Bu Biyoloji ve İlaç Keşfi İçin Ne Anlama Geliyor
Uzman olmayan biri için ana mesaj, yazarların maya hücreleri içinde daha hassas bir "etkileşim radarı" inşa etmiş olmalarıdır. Kısa protein el sıkışmalarını ölçülebilir ışık patlamalarına çevirerek ve üç etiketli proteinin birlikte ifade edilmesini genetik olarak akıllıca düzenleyerek, sistemleri hem bilinen hem de daha önce görünmez olan protein ortaklarını ortaya çıkarır. Her yeni eşleşmeyi doğrulamak için diğer tekniklerle daha fazla kontrol hâlâ gerekli olsa da bu platform hücresel ağ haritalarımızdaki önemli boşlukları doldurur. Suşlar küçük moleküllere karşı daha hassas olacak şekilde de tasarlandığından, aynı düzenleme zararlı protein ortaklıklarını bozacak veya faydalı olanları stabilize edecek ilaçları aramak için uyarlanabilir; bu da hem temel biyoloji hem de erken aşama ilaç keşfi için güçlü yeni bir araç sunar.
Atıf: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Anahtar kelimeler: protein etkileşimleri, fizyon mayası, lüminesans testi, yüksek verimli tarama, ilaç keşif araçları