Clear Sky Science · tr
Sırayla uygulanan platin ve PARP inhibisyonu, farelerde BRCA2 mutasyonlu pankreas kanserinde PD1 immünoterapisinin etkinliğini artırıyor
Bu araştırma hastalar için neden önemli
Pankreas kanseri en ölümcül kanserlerden biridir ve bir tümörde BRCA2 geninde bir duyarlılık gibi yararlı bir açıklık olsa bile, günümüz tedavileri hastalığı uzun süre kontrol altında tutmakta nadiren başarılı oluyor. Bu çalışma, gerçekçi bir fare modeli kullanarak birçok hastanın ve onkologun şimdi karşılaştığı pratik bir soruyu soruyor: kuvvetli kemoterapi ve ardından PARP inhibitörü uygulandıktan sonra, modern immünoterapi eklemek sağkalımı anlamlı biçimde uzatabilir mi ve tümörler neden bu kadar sık geri dönüyor?
Genetik bir zayıflığı olan inatçı bir kanser
Pankreatik duktal adenokarsinom tedavisiyle ünlü şekilde zordur; beş yıllık sağkalım hâlâ tek hanelerdedir. Hastaların küçük bir kısmı, kırık DNA’yı tamir etmek için gerekli olan BRCA2 geninde kalıtsal veya tümöre özgü kusurlar taşır. Bu tümörler, DNA’ya zarar veren ilaçlara —platin içeren kemoterapilere— ve kanser hücrelerinin DNA tamir yeteneğini daha da bozun PARP inhibitörlerine karşı olağandışı derecede hassastır. İlerlemiş BRCA‑mutasyonlu pankreas kanserinde mevcut standart bakım, aylara yayılan platin kemoterapisi sonrasında PARP inhibitörü ile bakım tedavisidir. Ancak kilit POLO klinik çalışmasında bu strateji genel sağkalımı uzatmadı; bu da direnç mekanizmalarını anlamanın ve daha iyi bakım yaklaşımları tasarlamanın gerekliliğini vurguluyor.
Daha gerçekçi bir fare modeli inşa etmek
Mevcut birçok laboratuvar modeli, gerçek hastalardaki tümörleri çevreleyen bağışıklık ve stroma bileşenlerini yok sayar. Bunu aşmak için yazarlar, tam işlevli bir bağışıklık sistemi bağlamında BRCA2 yetersiz pankreas tümörleri geliştiren fareler tasarladılar. Bu spontan tümörlerden, genetik olarak eşleşik farelere yerleştirilebilen klonal hücre hatları türettiler. Bu Brca2‑mutant tümörler insan pankreas kanserlerine çok benziyordu: yoğun fibrözdü, büyük ölçüde T hücrelerinden arındırılmıştı ve yüksek düzeyde spontan DNA hasarı gösteriyordu. Kritik olarak, tümörler yaygın bir platin kombinasyonuna (gemcitabin artı sisplatin) çok hassastı; oysa PARP inhibitörü tedavisi hayvanda yalnız uygulandığında, aynı hücreler kültürde güçlü etki gösterse bile yalnızca sınırlı ve kısa süreli etkiler sağladı. 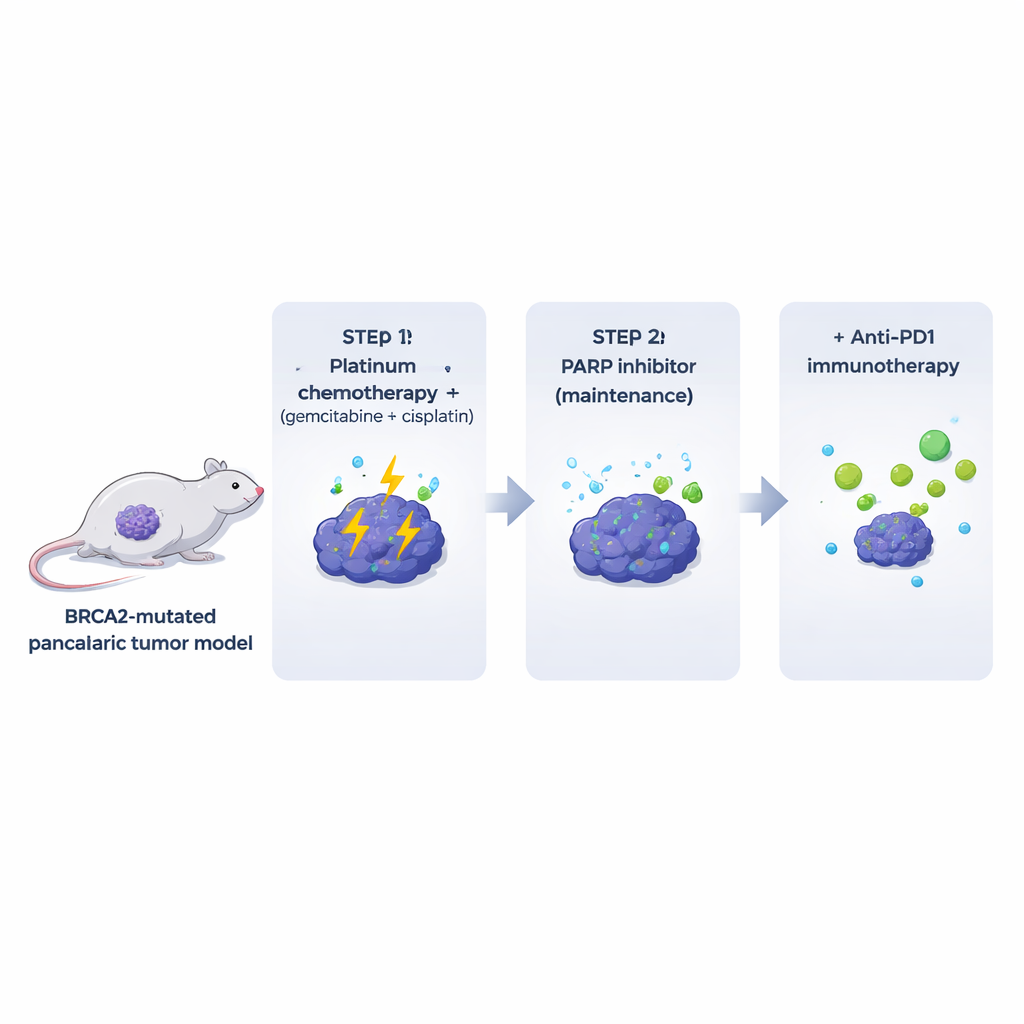
Kemoterapi tümör çevresini yeniden şekillendiriyor
Araştırma ekibi daha sonra platin kemoterapisi sonrası tümör içinde neler olduğunu inceledi. Tedaviden on gün sonra tümörler küçülmüştü fakat tamamen yok olmamıştı. Gen ifade analizleri, bağışıklıkla ilgili aktiviteye doğru çarpıcı bir kayma gösterdi: T hücresi aktivasyonu ve adaptif bağışıklıkla bağlantılı yollar etkinleşmişti. Tedavi edilmiş tümörlerde daha fazla T hücresi bulundu ve bu T hücrelerinin çoğu tükenme belirteçleri taşıyordu—yani aktive olmuş ancak etkisizleşmekte olduklarına işaret eden belirtiler. Benzer artmış T hücresi varlığı desenleri, cerrahi öncesi platin‑bazlı kemoterapi alan BRCA veya ilişkili PALB2 mutasyonlu insan pankreas kanserlerinde de gözlendi. Aynı zamanda, tümör hücreleri PD‑L1 düzeylerini artırdı; bu yüzey proteini PD‑1 reseptörüne bağlanarak T hücrelerini kapatabilir ve tümörlerin bu yeni immün baskıya karşı kendini savunduğuna işaret eder.
Neden PARP tek başına yeterli değil — ve direnç nerede ortaya çıkıyor
Hasta bakımını yansıtarak, araştırmacılar farelere önce gemcitabin ve sisplatinden oluşan bir kür, ardından PARP inhibitörü olaparib ile bakım verdi. Bu sıra, yalnız kemoterapiye kıyasla tümör kontrolünü ve sağkalımı geliştirdi; bu da önceki kemoterapinin tümörleri PARP inhibisyonuna daha duyarlı hale getirebileceğini doğruladı. Ancak hiçbir fare iyileşmedi: tümörler PARP bakım altında eninde sonunda yeniden büyüdü. Dirençli tümörler daha farklılaşmış bir görünüm sergiledi ve gelişim düzenleyicisi CDX2 düzeylerini güçlü şekilde artırmıştı. Bu, en azından bu modelde direncin yalnızca orijinal DNA tamir kusurunu onarmaktan kaynaklanmadığını, tümörün hücresel kimliğinde bir değişimi içerebileceğini düşündürüyor. CDX2, hastalarda ortaya çıkan direncin bir biyobelirteci olarak potansiyel şekilde hizmet edebilir.
Doğru sıra ile immünoterapinin kilidini açmak
Anti‑PD1 antikorları gibi immün kontrol noktası ilaçları bazı kanserlerin tedavisinde devrim yarattı, ancak pankreas kanseri büyük ölçüde yanıtsız kaldı. Buna uygun olarak, tedavi‑naif BRCA2‑mutant tümörlere anti‑PD1 (başka bir kontrol noktası ilacı olan anti‑CTLA4 ile birlikte veya tek başına) verilmesi yardımcı olmadı ve ayrıca sadece PARP inhibitörüne eklenmesi de az bir fayda sağladı. Tam sıra uygulandığında tablo değişti: önce platin kemoterapisi, ardından bakım olarak PARP inhibisyonu artı anti‑PD1. Bu düzenekte tümörler daha derin küçülmeler gösterdi ve fareler kemoterapi artı PARP inhibitörü veya sadece anti‑PD1’e kıyasla daha uzun yaşadı. PARP bakımı üzerine anti‑CTLA4 eklenmesi benzer faydalar sağlamadı; bu da kemoterapiyle hazırlanmış tümör ortamının özellikle PD‑1 blokajına yanıt vermeye uygun hale geldiğini düşündürüyor. 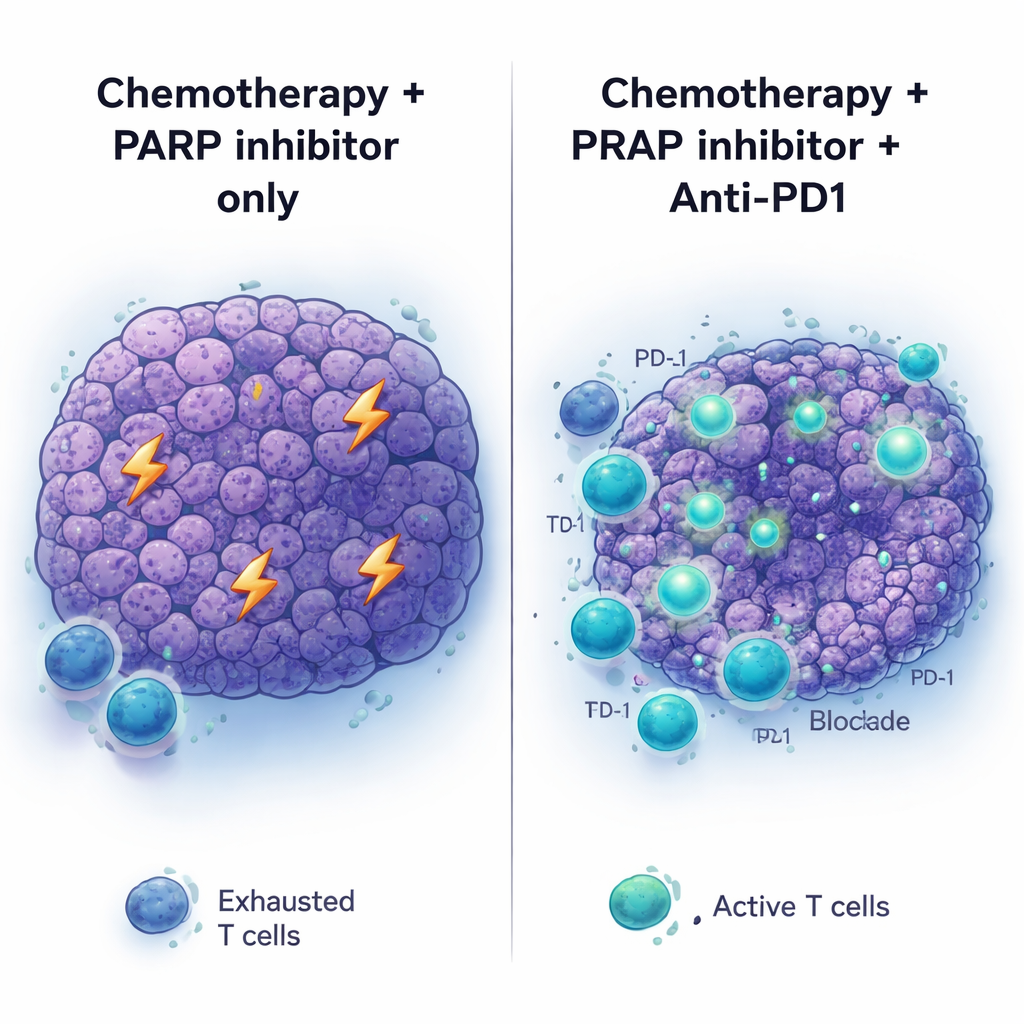
Gelecekteki bakım için bunun anlamı ne olabilir
Bir arada değerlendirildiğinde, çalışma BRCA‑mutasyonlu pankreas kanserinde tedavilerin sırası ve kombinasyonunun büyük önem taşıdığını savunuyor. Güçlü DNA hasarı yapan kemoterapi yalnızca tümör hücrelerini doğrudan hedeflemekle kalmaz, aynı zamanda başlangıçta tükenme ve PD‑L1 savunmalarıyla bastırılmış olsa bile immün yanıtı da canlandırır. PARP inhibitörleri bu faydayı uzatabilir ancak tek başına küratif olması olası değildir ve tümörleri dirençli, CDX2‑yüksek bir duruma itebilir. Platin kemoterapisinden sonra PARP bakımına anti‑PD1 immünoterapisini ekleyerek, kısa süreli inflamasyonlu ve tükenmiş immün manzarayı daha etkili ve kalıcı bir antitümör saldırıya dönüştürmek mümkün olabilir. BRCA ilişkili pankreas kanserinde PARP inhibitörleri ile immünoterapinin kombinasyonunu inceleyen devam eden klinik denemeler, bu dikkatle zamanlanmış stratejinin hastalar için daha uzun ve daha iyi yaşamlara dönüşüp dönüşemeyeceğini öğrenmek açısından belirleyici olacaktır.
Atıf: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Anahtar kelimeler: pankreas kanseri, BRCA2 mutasyonu, platin kemoterapisi, PARP inhibitörü, PD-1 immünoterapisi