Clear Sky Science · tr
Bir enzimin fonksiyonel sıcak nokta kalıntılarının NMR ve hesaplamalı yaklaşımlarla enzimatik reaksiyonun gerçek zamanlı izlenmesiyle incelenmesi
Geleceğin antiviralleri için neden bu önemli
Favipiravir, influenza’ya karşı kullanılan ve COVID-19 için test edilen bir hap formunda mevcut olsa da, yuttuğumuz formda virüslerle doğrudan savaşıyor değildir. Kendi hücrelerimiz onu önce aktif, virüsleri engelleyen bir moleküle dönüştürmelidir. Bu çalışma, insan hücresindeki bir enzimin kritik bir aktivasyon adımını neredeyse atom atom nasıl gerçekleştirdiğini ve enzimin hangi küçük parçalarının ilacın ne kadar hızlı ve ne kadar iyi etkinleştirileceğini kontrol eden “sıcak noktalar” olarak davrandığını ayrıntılı şekilde çözümlüyor. Bu ayrıntıların anlaşılması, hem daha güçlü hem de hastalarda daha öngörülebilir yeni nesil antivirallerin tasarımını yönlendirebilir.
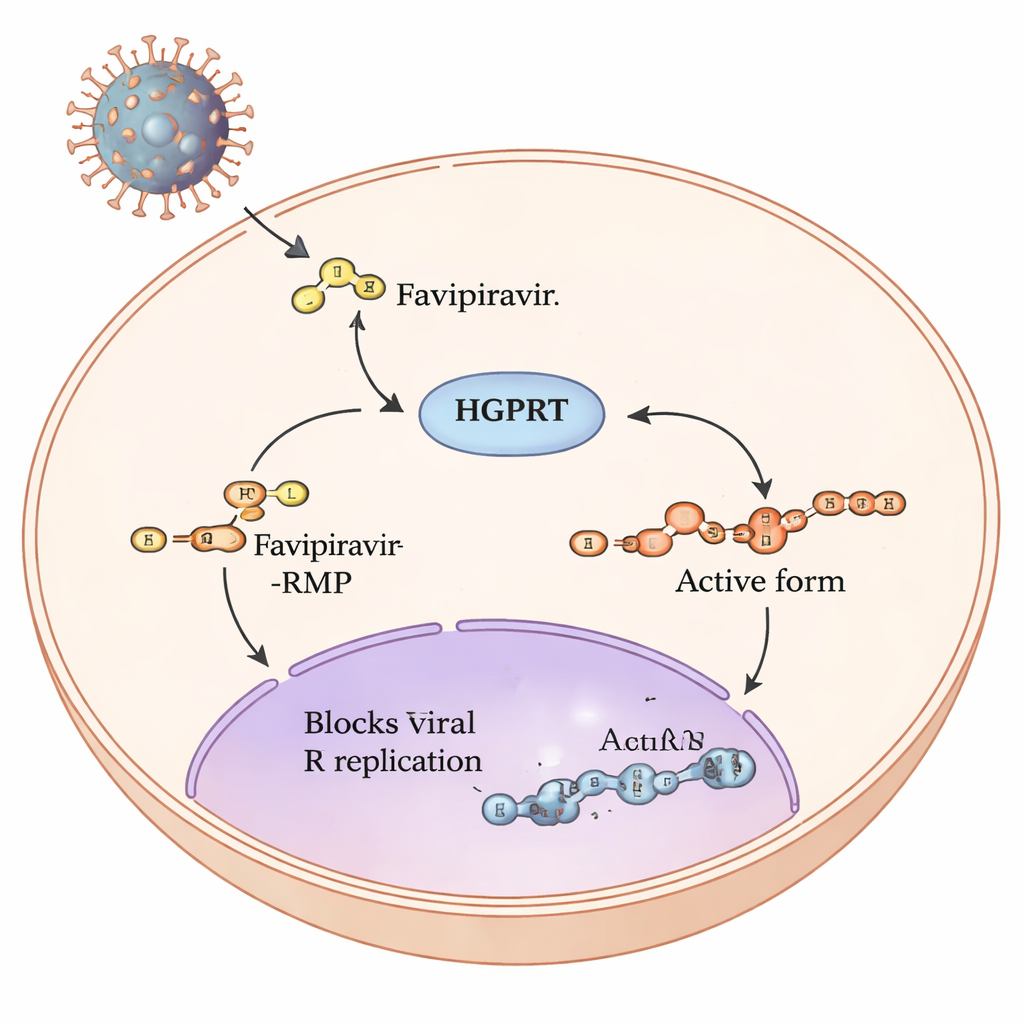
Proilacın hücrelerimiz içindeki yolculuğu
Favipiravir, sözde bir proilaçtır: insan hücrelerine girdikten sonra bir dizi kimyasal adım onu influenza ve SARS‑CoV‑2 gibi RNA virüslerinin kopyalama mekanizmasını kilitleyebilecek bir forma dönüştürür. Bu yolun ilk ve en yavaş adımı, hipoksantin‑guanin fosforibosiltransferaz olarak adlandırılan insan bir enzim tarafından yürütülür (HGPRT). HGPRT, favipiravir’e küçük bir şeker‑fosfat grubu ekleyerek favipiravir‑RMP üretir. Ancak bu adımdan sonra diğer enzimler, viral RNA polimerazına doğrudan müdahale eden tam aktif trifosfat formunu oluşturabilir. İlk HGPRT kaynaklı adım, ne kadar aktif ilacın yapıldığında bir darboğaz gibi davrandığı için yazarlar HGPRT’nin favipiraviri işlemede en önemli hangi bölgelerine odaklanacaklarını belirlemeye giriştiler.
Kimyayı gerçek zamanlı NMR ile izlemek
Favipiravir, manyetik alanda küçük bir radyo vericisi gibi davranan bir flor atomu içerir; bu özellik benzersizdir. Ekip bunu, flor‑19 nükleer manyetik rezonans (NMR) spektroskopisini kullanarak tüpte reaksiyon ilerledikçe ne kadar favipiravir ve ne kadar favipiravir‑RMP bulunduğunu gerçek zamanlı izlemek için değerlendirdi. Sadece ilacın flor taşıması nedeniyle NMR sinyalleri temiz ve izlemesi kolaydı. Ara sıra 12 saat boyunca alınan spektrumlarla araştırmacılar başlangıç ilacının azalmasını ve modifiye ürünün yükselmesini takip ederek, reaksiyonun ne kadar hızlı ilerlediği ve enzimin ilacı ne kadar sıkı tuttuğu gibi standart kinetik ölçümleri çıkarabildiler.
Enzimde kilit pozisyonları ayarlamak
Favipiravir‑RMP’ye bağlı HGPRT’nin önceki X‑ray görüntüleri, ilacı bir ceplerde kavrayan birkaç amino asit önermişti. Yeni çalışma bu pozisyonlardan üçünü, proteinde hassas tek harf değişiklikleri yaparak test ediyor ve her mutant enzimi doğal olanla karşılaştırıyor. T138A adını verdikleri bir değişiklik, ilacı tutmaya yardımcı olduğu düşünülen bir kimyasal grubu kaldırmasına rağmen, beklenmedik şekilde enzimin favipiraviri yaklaşık dört ila altı kat daha hızlı dönüştürmesini sağladı. İkinci değişiklik K140M, reaksiyonu ölçülü şekilde yavaşlattı ve görünür bağlanmayı biraz zayıflattı. Üçüncü değişiklik D193N ise, değiştirilmiş protein hâlâ ürünü üretebiliyor ve ürüne bağlanabiliyor olsa da, enzimin favipiravir‑RMP yapabilme yeteneğini tamamen ortadan kaldırdı. Bu sonuçlar birlikte gösteriyor ki tüm temas noktaları eşit değil: bazıları ince hız düzenleyicileri olarak davranırken, diğerleri temel anahtarlar niteliğinde.
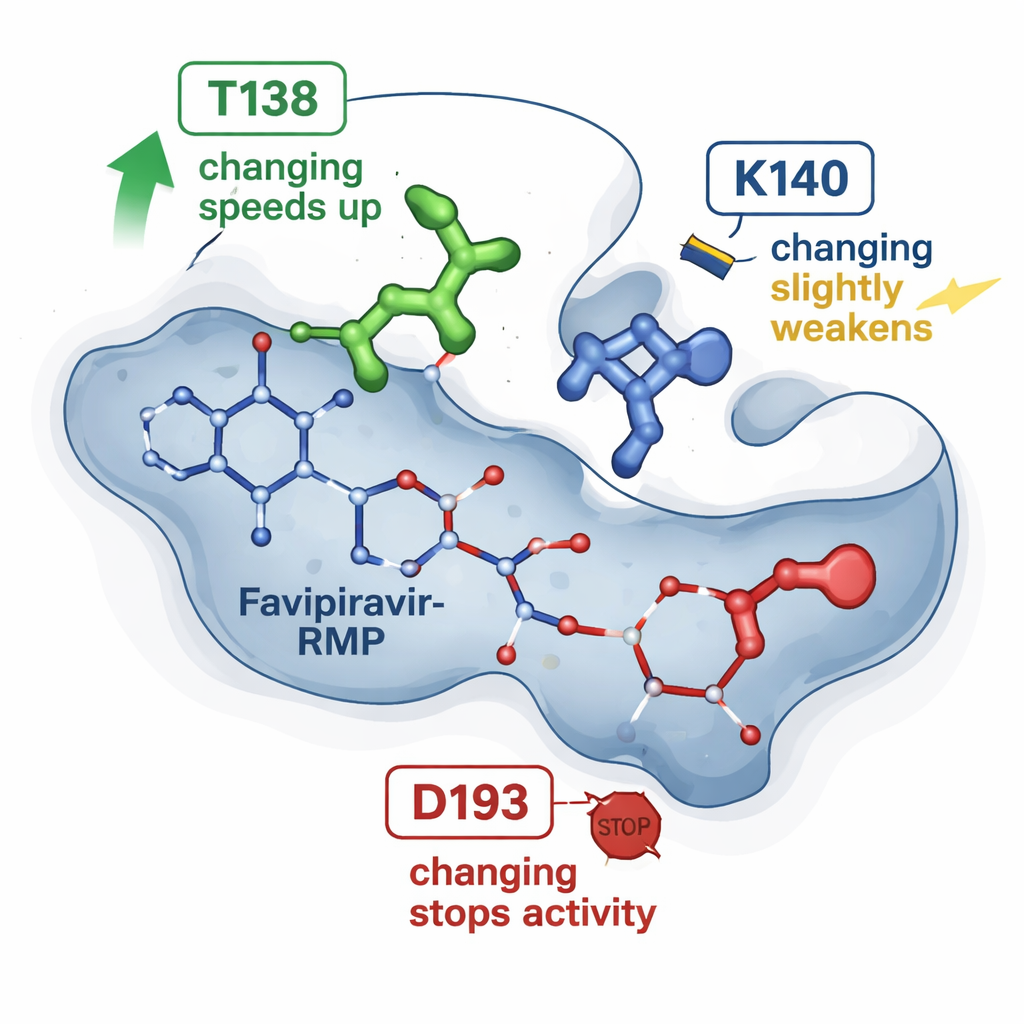
Bilgisayarda hareketli parçaları simüle etmek
Statik yapıların ötesini görmek için araştırmacılar moleküler simülasyonlara yöneldiler. Favipiravir‑RMP ile birlikte bilinen üç boyutlu HGPRT yapısından başlayarak, ilacın her mutanttaki bağlanma gücünü tahmin etmek ve çok sayıda kısa moleküler dinamik simülasyonu çalıştırmak için yerleşik hesaplamalı araçlar kullandılar. Bu simülasyonlar atomların onlarca nanosaneye nasıl sallanıp etkileştiğini izliyor. Hesaplamalar NMR’den elde edilen eğilimlerle uyum gösterdi: T138A varyantı favipiravir‑RMP’yi genellikle daha elverişli tutma eğilimindeydi ancak ilaçın başka bir kalıntı (K140) tarafından fosfat grubu kısa süreliğine demirlenerek serbest bırakılmadan önce bir “kaçış” yoluna doğru hareket ettiği dönemler de gösterdi. Buna karşılık D193N varyantı ürünü hâlâ kavrıyordu, ancak magnezyum iyonu gerektiren daha erken bir katalitik adımda muhtemelen başarısız oldu; bu da stabil bağlanma olmasına rağmen aktivitesini neden kaybettiğini açıklıyor.
Daha akıllı antiviral tasarım için bir yol haritası
Gerçek zamanlı NMR ölçümleri ile ayrıntılı bilgisayar modellerini birleştirerek bu çalışma, favipiravir’in nasıl etkinleştirildiğini yöneten HGPRT içindeki fonksiyonel sıcak noktaları haritalıyor. Uzman olmayanlar için çıkarım şudur: Kendi enzimlerimiz, hücre içinde ne kadar aktif antiviral ilacın biriktiğini büyük ölçüde etkileyebilir ve ilacın şeklini veya enzimin cebini değiştirerek bu sonucu dramatik biçimde değiştirmek mümkündür. Yazarların hibrit stratejisi, diğer ilaçların hedef proteinleriyle nasıl etkileştiğini incelemek için genel bir plan sunuyor ve böylece vücudun aktivasyon mekanizmasına daha iyi uyumlu yeni antiviral bileşiklerin geliştirilmesini hızlandırabilir.
Atıf: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Anahtar kelimeler: favipiravir, antiviral aktivasyon, HGPRT enzimi, NMR spektroskopisi, ilaç tasarımı