Clear Sky Science · tr
Multiplex immünofloresan verileri için bilgilendirilmiş mekânsal farkındalıklı desenler
Tümör Hücrelerinin Mahallesi Neden Önemli
Pankreas kanseri, kısmen tümörlerin bağışıklık ve destek hücrelerinden oluşan karmaşık bir “mahalle” içinde yaşaması nedeniyle en ölümcül kanserlerden biridir; bu hücreler kanserle savaşabilir veya onun saklanmasına yardım edebilir. Bu çalışma, mikroskop görüntülerindeki bu hücrelerin mekânsal düzenini okumaya yönelik yeni bir yaklaşım sunar ve agresif pankreatik duktal adenokarsinom (PDAC) ile onun kanser öncesi komşusu intraductal papillary mucinous neoplasm (IPMN) arasında bağışıklık sisteminin nasıl farklı davrandığını ortaya koyar. Bu gizli desenleri anlamak daha iyi tanı yöntemlerine ve daha akıllı, hedefe yönelik tedavilere işaret edebilir.
Dokuya Sadece Resim Gibi Değil, Harita Gibi Bakmak
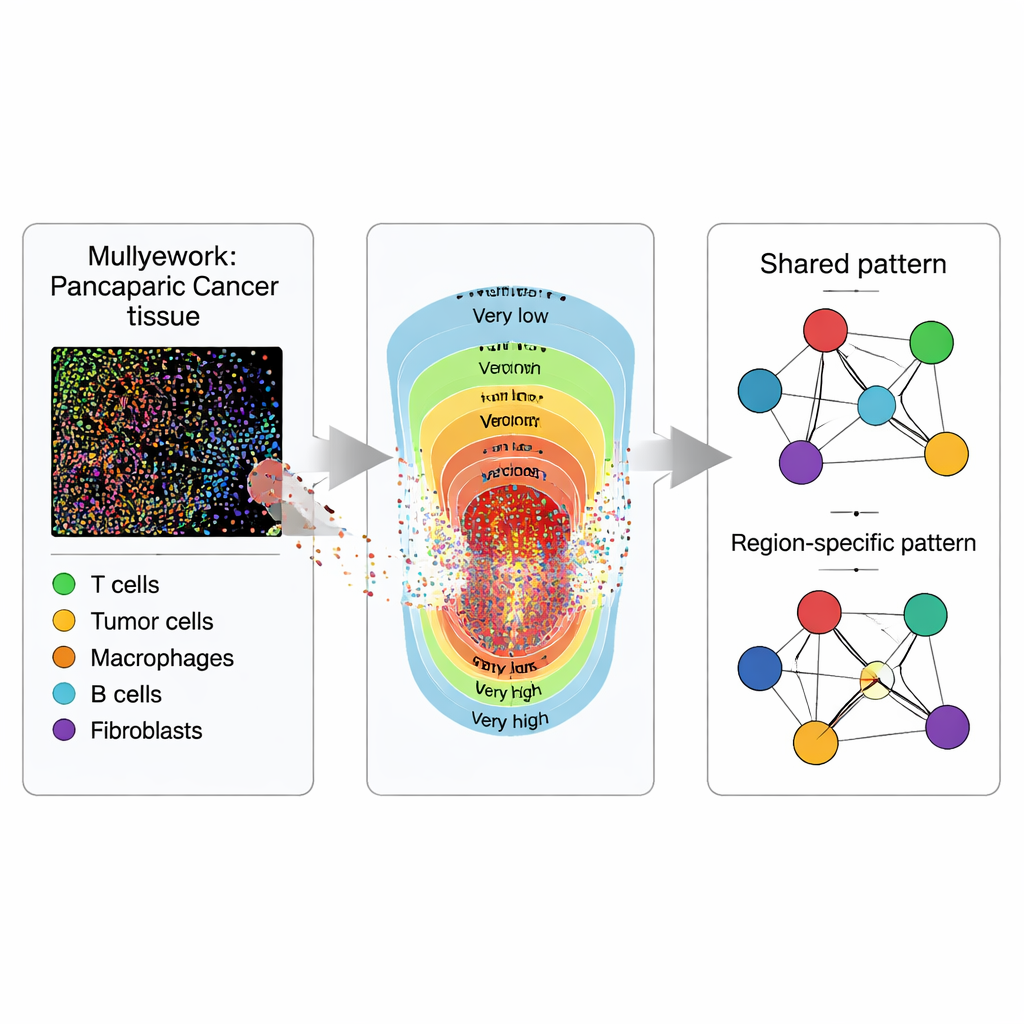
Araştırmacılar, tümör dilimini düz bir görüntü olarak ele almak yerine onu noktalardan oluşan bir harita gibi ele alıyor. Multiplex immünofloresan görüntüleme kullanarak 119 PDAC ve 53 IPMN hastasından alınan doku örneklerini, farklı hücre tiplerinin farklı renklerde parlamasını sağlayacak şekilde boyuyorlar. Özel yazılım, görünen her hücreyi koordinatları ve etiketi olan bir nokta hâline çeviriyor: tümör (epitelyal) hücreleri, bağışıklık tepkisini saldırgan ya da düzenleyici yönde etkileyebilen çeşitli T hücresi türleri ve tümör parçalarını T hücrelerine gösteren antijen sunan hücreler. Önemli soru yalnızca her hücre tipinin ne kadar bulunduğu değil, aynı zamanda doku boyunca birbirlerine göre nerede yer aldıklarıdır.
Tümörü Bölgelere Ayırmak
Tümörün merkezinden dışa doğru nasıl değiştiğini yakalamak için her doku örneği, tümör hücrelerinin yoğunluğuna göre “çok düşük”den “çok yüksek”e beş bölgeye ayrılıyor. Bu bölgeler, patolojistler tarafından mikroskopta sıklıkla görülen ancak nadiren nicelendirilen bir tümör yükü ve hücresel yoğunluk gradyanını temsil ediyor. Her bölgede ekip, her hücre tipi için düzleştirilmiş “yoğunluk haritaları” tahmin ediyor; temelde dağınık noktaları her hücre tipinin kümelendiği yerlerin sürekli ısı haritalarına çeviriyorlar. Bu bölgeleme, hücrelerin genel olarak nasıl etkileştiğini karşılaştırmanın yanı sıra, bu etkileşimlerin seyrekten yoğun tümör bölgelerine nasıl kaydığını da incelemelerini sağlıyor.
Hücre Mahallelerini Ağlara Dönüştürmek
Sonraki adımda araştırmacılar mekânsal desenleri ağlara çeviriyor; burada her hücre tipi bir düğüm ve bağlantılar iki hücre tipinin diğer tüm hücreleri hesaba kattıktan sonra birlikte görünme eğiliminin gücünü temsil ediyor. ISPat (Informed Spatially aware Patterns) adını verdikleri Bayesyen istatistik çerçevesini kullanarak, tüm bölgelerde ortak olan özellikleri bölgeye özgü olanlardan ayırıyorlar. ISPat, mevcut olduğunda önceden bilinen biyolojik bilgiyi de entegre edebiliyor ve karmaşık verilerde kestirimleri stabilize etmeye yardımcı oluyor. Simülasyon deneyleri, ISPat’ın bilinen desenleri güvenilir şekilde geri kazanabildiğini ve geleneksel yöntemlerden çok daha hızlı çalıştığını gösteriyor; bu da büyük görüntüleme çalışmalarında pratik olmasını sağlıyor.
İki Hastalık, İki Bağışıklık Mimarisi
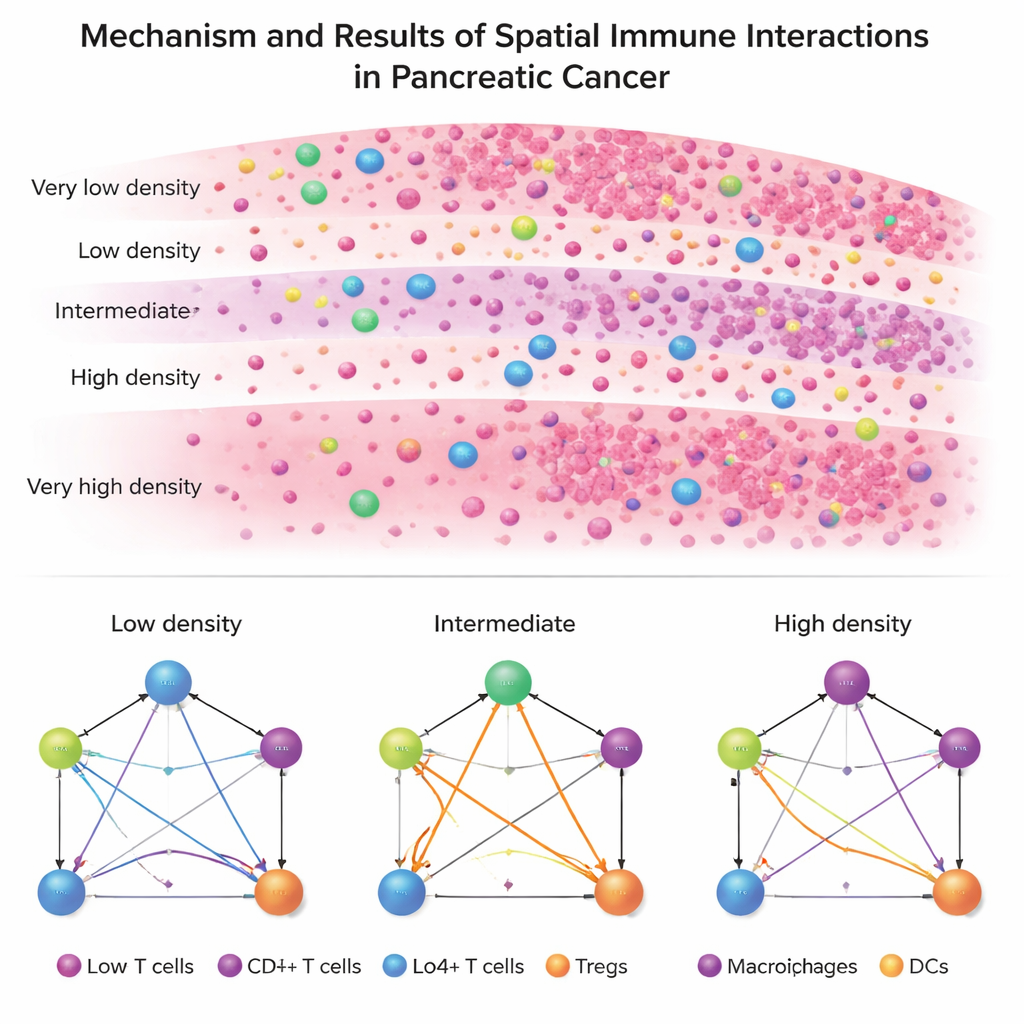
ISPat’ı gerçek hasta verilerine uyguladıklarında PDAC ile IPMN arasında çarpıcı bir tezat ortaya çıkıyor. PDAC, katı ve tekdüze bir bağışıklık mimarisi gösteriyor: neredeyse tüm bölgelerde tümör hücreleri, yardımcı T hücreleri, öldürücü (sitotoksik) T hücreleri, düzenleyici T hücreleri ve antijen sunan hücreler hemen hemen aynı ilişki düzenini koruyor. Bu, yerinden edilmesi zor, kalıcı bir immünsüpresif ortamı işaret ediyor. Buna karşılık IPMN, özellikle düzenleyici T hücrelerinin diğer bağışıklık hücreleriyle bağlantısında bölgeden bölgeye çok daha fazla değişkenlik gösteriyor. IPMN’de, ne tamamen tümör hücreleriyle dolu ne de neredeyse tümörden arınmış olan ara yoğunluklu bölgeler, bağışıklık etkileşimlerinin en dramatik biçimde yeniden şekillendiği alanlar olarak öne çıkıyor.
Bağışıklıktan Kaçış ve Tedavi İçin Sıcak Noktalar
Daha derine inildiğinde, çalışma özellikle ara yoğunluklu bölgelerde PDAC ile IPMN arasında etkileşimleri tutarlı biçimde farklı olan bazı hücre çifti ilişkilerini tanımlıyor. Bunların birçoğu bağışıklık saldırılarını azaltabilen düzenleyici T hücrelerini, antijen sunan hücreleri ve anti-tümör yanıtları başlatıp icra eden öldürücü T hücrelerini içeriyor. Özellikle antijen sunumunu ve doğrudan tümör öldürmeyi yönlendiren etkileşimler ile immün baskıyı pekiştiren etkileşimler, en uç tümör bölgelerinde değil, bu ara gradyent alanlarında en belirgin şekilde farklılaşıyor. Bu desen, bağışıklık kontrolü için kritik mücadelenin tümör ile bağışıklık sistemi hâlâ aktif olarak pazarlık yaptığı geçiş bölgelerinde olduğunu öne sürüyor.
Bu Hastalar İçin Ne Anlama Geliyor
Uzman olmayan bir okuyucu için çıkarım şudur: hücrelerin tümör içindeki konumu, hangi hücrelerin orada olduğuna en az onun kadar önemlidir. PDAC, baskılayıcı bir immün “yerleşimi” sabitlemiş gibi görünürken, IPMN’in immün peyzajı daha esnek ve bölgeye dayalı kalmaya devam ediyor. Bu mekânsal parmak izleri, tehlikeli tümörleri kanser öncesi lezyonlardan ayırt etmek ve hangi hastaların belirli immünoterapilerden yararlanabileceğini tahmin etmek için biyobelirteçler haline gelebilir. ISPat çerçevesi, birçok hastalıkta bu tür mekânsal kodları okumak için genel bir araç sunarak, kanser tedavisinin yalnızca genetikler ve hücre tipleriyle değil, aynı zamanda her hastanın tümöründeki hücrelerin ince ölçekli coğrafyasıyla yönlendirildiği bir geleceği destekliyor.
Atıf: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Anahtar kelimeler: pankreas kanseri, tümör mikroçevresi, mekânsal görüntüleme, immün etkileşimler, kesin onkoloji