Clear Sky Science · tr
Proksimite-biotinilasyon uygulamaları için lizin içermeyen bir REC etiket sistemi
Proteinlerde küçük etiketlerin önemi
Her hücrenin içinde proteinler nadiren tek başına çalışır—sağlık ve hastalığı yönlendiren değişken ortaklıklar halinde bir araya gelirler. Bu ortaklıkları incelemek için bilim insanları sıklıkla proteinlere izlenebilmeleri, karışımdan çekilebilmeleri veya mikroskopta görülebilmeleri için küçük “isim etiketleri” takarlar. Proksimite biotinilasyon adı verilen yaygın bir yöntem, hücre içindeki kimlerin kimlere yakın olduğunu haritalamaya olanak tanır, ancak bunun gizli bir sorunu vardır: bu isim etiketlerinin birçoğu kimyasal olarak modifiye olur ve tam ihtiyaç duyulduğunda etkili bir şekilde kaybolur. Bu çalışma, zorlu koşullar altında görünür kalmak üzere tasarlanmış yeni bir etiket türünü, REC etiketini tanıtıyor.
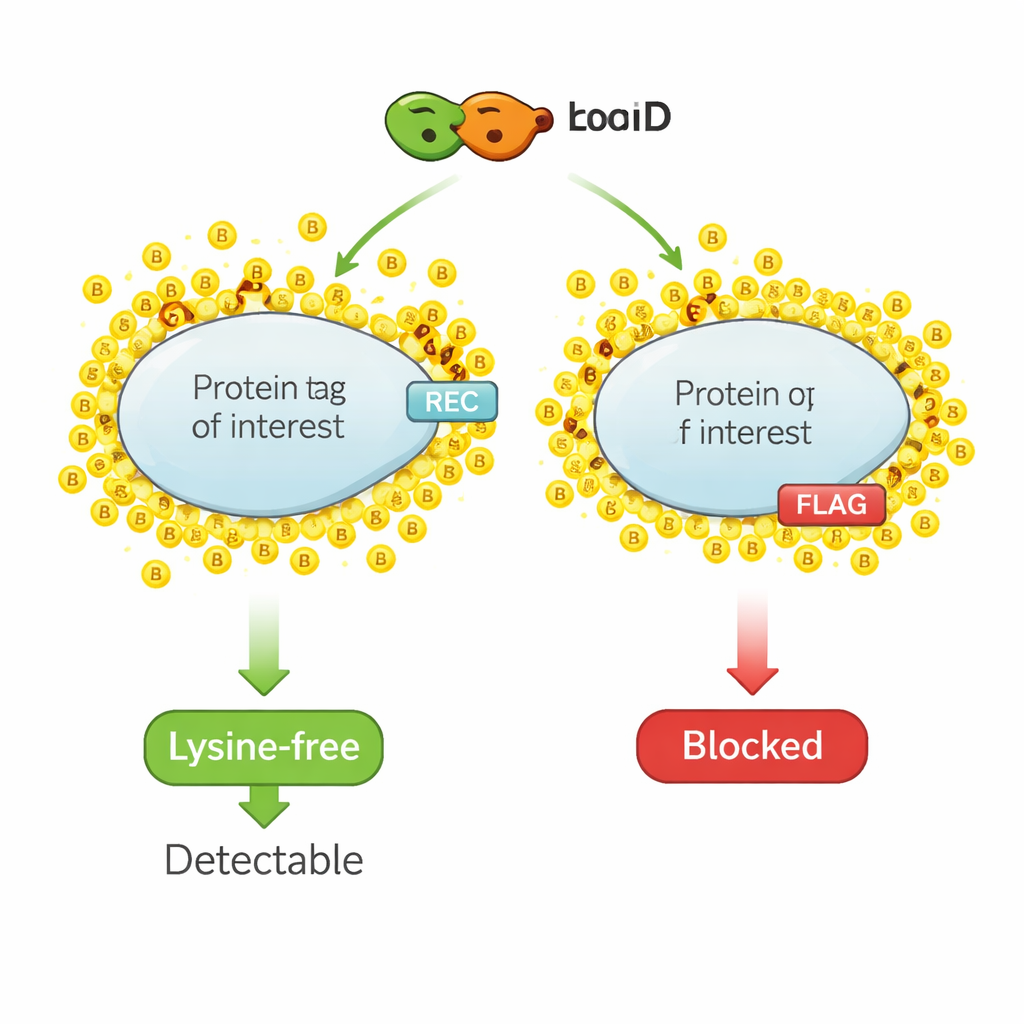
Protein komşuları için kimyasal bir fosforlu kalem
Proksimite biotinilasyon bir moleküler fosforlu kalem gibi çalışır. TurboID gibi mühendislik yapılmış bir enzim, ilgi proteinine füzyonlanır. Biotin—küçük bir vitamin—eklendiğinde TurboID hızla yakınlardaki proteinlere biotin molekülleri bağlar. Araştırmacılar daha sonra tüm biotin işaretli proteinleri çıkarır ve bunları tanımlayarak proteinin yerel komşuluğunun bir anlık görüntüsünü elde ederler. Ancak, yakın proteinleri etiketleyen aynı kimya, tespit için yaygın olarak kullanılan küçük epitop etiketlerini de hedef alır; çünkü bu etiketler genellikle biotinin ana bağlanma yeri olan lizin aminoasitini içerir. Etiketteki lizinin biotinle kaplanması durumunda antikorlar etiketi tanıyamaz ve standart tespit yöntemlerindeki sinyal düşer veya yok olur.
Modifikasyona dirençli bir etiket tasarlamak
Bunu çözmek için yazarlar tamamen lizin içermeyen yeni bir etiket yaratmaya karar verdiler. İnsan proteinleriyle benzerliği az olan ve istenmeyen çapraz tepkime riskini azaltan PfRipr5 adlı bir sıtma paraziti protein fragmentinden başladılar. Tavşanlarda mikroçip tabanlı bir tarama yöntemi kullanarak PfRipr5'e karşı 22 monoklonal antikor ürettiler ve özellikle güçlü ve özgül bağlanma gösteren bir tanesini, klon No. 6 olarak adlandırdılar. PfRipr5 fragmentini sistematik olarak budayıp mutasyona uğratarak antikorun hedefini 11 amino asitlik bir diziye daralttılar. Bu minimal dizide yalnızca bir lizin vardı ve bunu benzer bir aminoasit olan argininle değiştirdiler. İlginç bir şekilde, antikor hâlâ aynı şekilde bağlanmaya devam etti. Bu optimize edilmiş, lizinsiz dizi REC etiketi olarak adlandırıldı ve ona karşılık gelen antikor REC antikoru olarak adlandırıldı.
REC etiketini sınama
Ekip daha sonra REC etiketinin, laboratuvarda yaygın olarak kullanılan FLAG gibi etiketlerin yerini alıp alamayacağını test etti. Floresan veya sinyal proteinlerine füzyonlanıp hücresiz sistemlerde ve memeli hücrelerinde üretildiğinde, REC etiketli proteinler immünoblotlama, AlphaScreen adı verilen yüksek duyarlıklı ışık tabanlı bir plaka testi ve hücre içi immün boyama ile kolayca tespit edildi. Tespit gücü FLAG etiketi ve başka bir lizinsiz etiket sistemi (AGIA) ile benzerdi ve REC antikoru çeşitli insan ve maymun hücre hatlarında çok az arka plan gürültüsü gösterdi. Önemli olarak, etiket proteinin başında veya sonunda yerleştirildiğinde ve çekirdek, mitokondri, endoplazmik retikulum ve hücre zarı dahil olmak üzere farklı hücresel bölgelerde bulunan proteinlerde çalıştı.
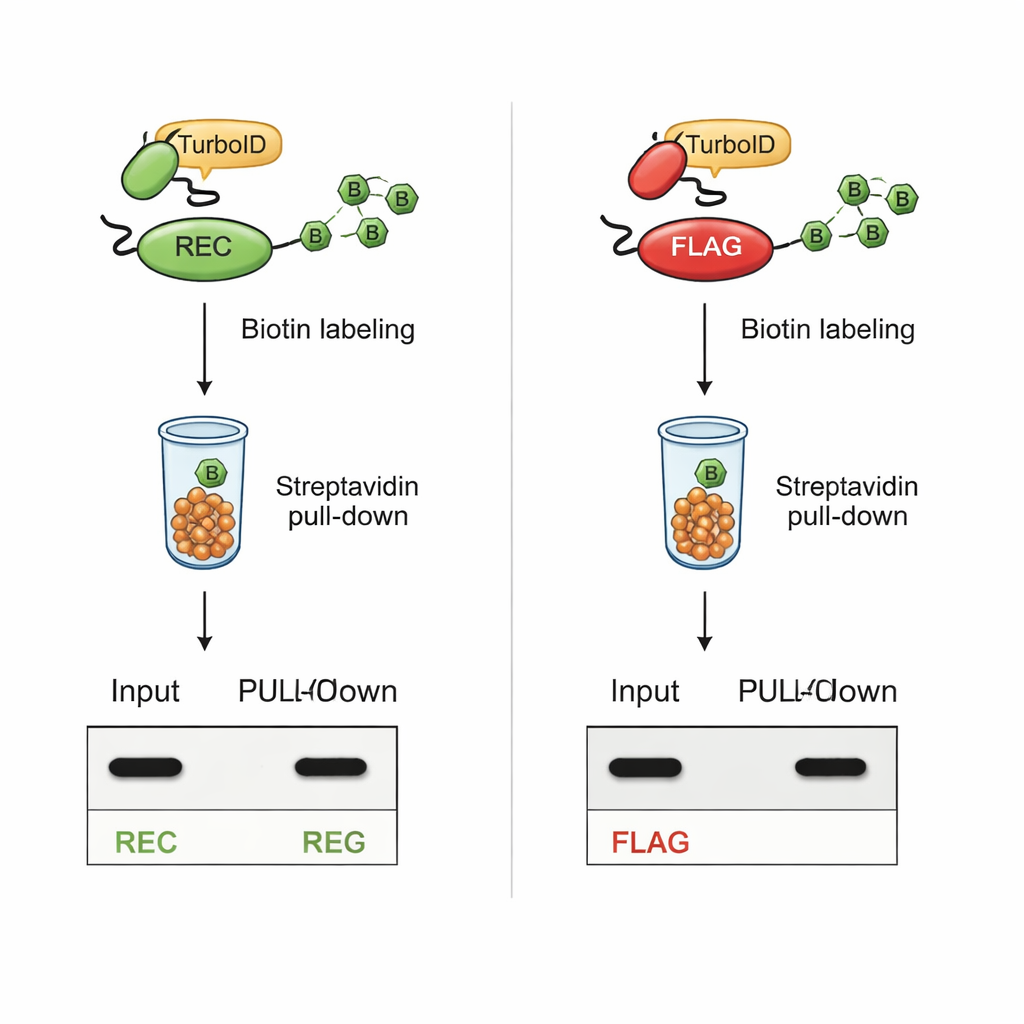
Yoğun etiketleme sırasında görünür kalma
Kritik test, TurboID tabanlı biotinilasyon sonrası REC’in tespit edilebilir kalıp kalmayacağıydı. TurboID bilinen etkileşim partnerlerine füzyonlandığında, REC taşıyan proteinler hem tüm hücre özütlerinde hem de saflaştırılmış, biotinle işaretlenmiş fraksiyonda net şekilde görünmeye devam etti. Buna karşılık, klasik FLAG taşıyan proteinler TurboID etkin hale geldiğinde FLAG sinyalini kaybetti; oysa proteinlerin kendileri hâlâ mevcuttu. Sentetik peptitlerle yapılan ek deneyler, TurboID’nin doğrudan FLAG dizisindeki lizini biotinileştirdiğini ve böylece antikor erişimini fiziksel olarak engellediğini gösterdi. Lizin içermeyen REC etiketi ise TurboID tarafından dokunulmadan kaldı ve tespit edilmesi kolay oldu.
Gelecek deneyler için anlamı
Canlı hücrelerde protein ağlarını araştıran araştırmacılar için REC etiketi pratik bir yeni araç sunuyor: günlük deneylerde tanıdık etiketler gibi davranıyor ama güçlü proksimite-etiketleme enzimleri etkin olduğunda bile çalışmaya devam ediyor. Bu, bilim insanlarının etiketli proteinlerinin var olduğunu ve doğru şekilde yakalandığını daha güvenilir bir şekilde doğrulamalarına olanak sağlar ve etiketin kendisi müdahale etmeden ubiquitinasyon ve asetilasyon gibi diğer lizin-temelli modifikasyonları incelemelerini mümkün kılar. Kısacası, REC küçük bir tasarım değişikliği ama büyük bir etki; karmaşık protein haritalama deneylerini daha net ve güvenilir hale getirmeye yardımcı oluyor.
Atıf: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Anahtar kelimeler: protein etiketleme, proksimite biotinilasyon, TurboID, protein etkileşimleri, epitop etiketleri