Clear Sky Science · tr
Sistemik amiloidoza karşı dirençteki biyokimyasal temelin değerlendirilmesi
Çok Küçük Protein Değişiklikleri Ölümcül Bir Birikimi Nasıl Engelliyor
Romatoid artritten tüberküloza kadar birçok kronik inflamatuar hastalık, nadir ama sıklıkla ölümcül olabilen sistemik AA amiloidozu tetikleyebilir. Bu durumda normal bir kan proteini, organları tıkayan sert lifler olarak birikir. Bu çalışma şaşırtıcı derecede umut verici bir soruyu soruyor: bu proteindeki küçük, doğal değişiklikler bazı hayvanları hastalığa karşı büyük ölçüde bağışık kılabilir mi—ve eğer öyleyse nasıl?
Protein Birikimlerinin Gizli Tehdidi
AA amiloidozu, kanda serum amiloid A (SAA) adı verilen bir inflamatuar alarm sinyaliyle başlar. Şiddetli veya uzun süren inflamasyon sırasında SAA seviyeleri normalin birkaç bin katına çıkabilir. Bazı insanlarda ve hayvanlarda bu proteinin bir bölümü yanlış katlanır ve dalak ile böbrek gibi organlara yayılan uzun lifler, yani amiloid fibrilleri halinde istiflenir. Zamanla bu lifler organ fonksiyonunu bozar. Ancak yüksek SAA seviyesine sahip herkes amiloidoz geliştirmez ve belirli fare soyları laboratuvarda hastalığa zorlanmış olsalar bile şaşırtıcı şekilde dirençli kalır. Bunun nedenini anlamak, insanlarda amiloid birikimini önlemeye yönelik yeni stratejilere işaret edebilir.
Dirençli Fareler ve Özel Protein Versiyonları
Farelere ait AA amiloid fibrillerinin çoğu, hastalıkla güçlü ilişki gösteren SAA1.1 adlı bir SAA versiyonundan kaynaklanır. Ancak bazı fare soyları esas olarak SAA1.5 ve SAA2.2 adlarıyla anılan hafifçe değiştirilmiş versiyonları üretir ve bu soylar nadiren sistemik AA amiloidozu geliştirir. Proteinler yalnızca birkaç yapı taşı (amino asit) ile farklılık gösterir, fakat bu değişiklikler hastalığa neden olan liflerin iç çekirdeğini oluşturan sıkışık bir bölgede kümelenir. Araştırmacılar bu küçük farklılıkların proteinlerin tamamen toplanmasını engellemediğini, bunun yerine onları zararlı olan çok özel lif şekline girmelerini önlediğini öne sürdü.
Proteinleri Laboratuvarda Test Etmek
Bu fikri araştırmak için ekip, üç fare SAA varyantının tamamını bakterilerde üretti ve bunların test tüpü deneylerinde nasıl davrandığını izledi. Amiloid oluştuğunda ışıldayan bir floresan boya kullanarak lif oluşumunu izlediler ve yapıları elektron mikroskoplarıyla doğruladılar. Hastalıkla ilişkilendirilen SAA1.1 hızla uzun, düz lifler oluşturdu. SAA2.2 de lif oluşturabiliyordu, ancak onlar daha kalın, daha burulmuş ve yapısal olarak daha çeşitliydi ve aynı güçlü boya sinyalini tetiklemedi. Buna karşın SAA1.5, test edilen koşullar altında lif oluşturmayı başaramadı. Bilim insanları hasta fare dalaklarından alınan gerçek hastalık liflerinden çok küçük örnekleri “tohum” olarak eklediklerinde, SAA1.1 orijinal yapıyı yakından taklit eden yeni lifler hızla büyüttü; bu, prion benzeri bir etkiydi. Çarpıcı biçimde, SAA1.5 ve SAA2.2 bu tohumlara hiç eklenmedi; ex vivo lifler onları patojenik şekle çekemedi.
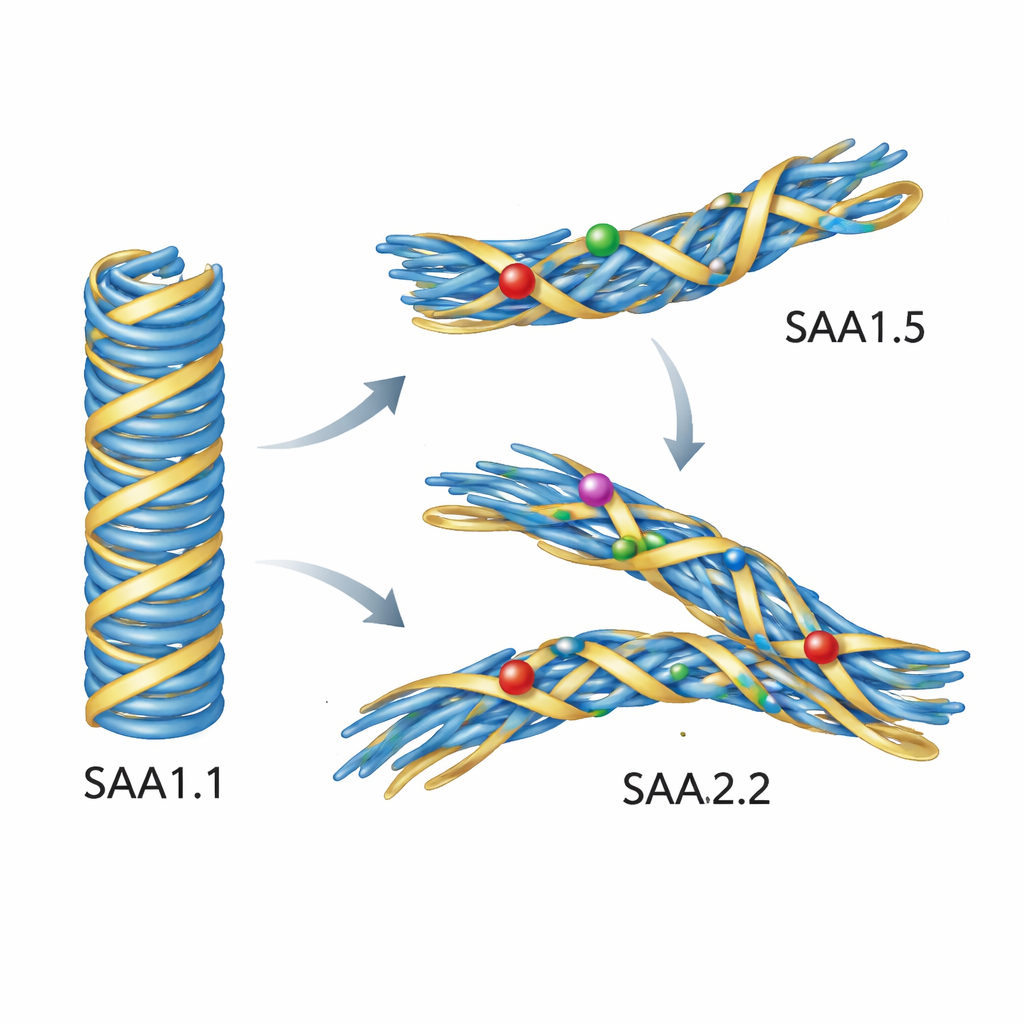
Simülasyonlar Neden Mutant Proteinlerin Kötü Şekli Reddedildiğini Gösteriyor
Deneyler atomik düzeyde tam olarak neyin yanlış gittiğini gösteremediği için yazarlar ayrıntılı bilgisayar simülasyonlarına başvurdu. Patolojik bir fare AA fibrilinin yüksek çözünürlüklü yapısından başladılar (SAA1.1 tabanlı) ve sonra hesaplamalı olarak SAA1.5 ile SAA2.2 dizilerini yerleştirdiler. Bu fibrilleri vücut sıcaklığında suda simüle ettiklerinde, SAA1.1 tabanlı model dikkat çekici şekilde kararlı kaldı. Buna karşılık, SAA1.5 veya SAA2.2’den yapılan fibriller kaydı ve bozuldu. Çekirdekteki önemli bir döngü bölgesi dışarı doğru hareket etti ve proteinin başlangıç segmentiyle temasını gevşetti; birkaç yan zincir yeni yönelimlere geçti. Bu ince yeniden düzenlemeler, hastalıkla ilişkili katlanmayı tanımlayan sıkı sıkıştırmayı bozdu. Başka bir deyişle, varyant diziler genel olarak lif oluşturmaktan rahatsız değil—ancak patojenik AA fibrilinin planına rahatça uyamıyorlardı.
Doğanın Tasarımı Gelecekteki Tedavilere Nasıl İpucu Veriyor
Birlikte ele alındığında çalışma, “amiloide dirençli” fare soylarının korunmasının nedeninin SAA’larının hiç birikememesi olmadığını gösteriyor. Bunun yerine onların SAA versiyonları, sistemik AA amiloidoza yol açan o tekil lif şekliyle yapısal olarak uyumsuz. Proteinler hâlâ kümelenebiliyor, ancak bunu alternatif ve görünüşe göre zararsız formlarda yapıyorlar. Benzer koruyucu mutasyonlar prion ve Alzheimer dahil diğer protein yanlış katlanması hastalıklarında da biliniyor. Bu, daha geniş bir ilkeye işaret ediyor: hastalığa yatkın bir proteini işlevini normal biçimde sürdürürken toksik mimarisini alamayacak şekilde değiştirmek—yeterli düzeyde hastalığı önleyebilir. Uzun vadede, bu doğal “dirençli” varyantlardan ya da bunlardan türetilen kısa parçacıklardan esinlenen tedaviler, proteinleri zararlı katlanmalardan çıkarıp zararsız biçimlere yönlendirmede yardımcı olabilir.
Atıf: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Anahtar kelimeler: AA amiloidozu, serum amiloid A, protein yanlış katlanması, amiloid direnci, fare modelleri