Clear Sky Science · tr
Polikaprolakton nanoparçacık çökeltiminin modellenmesi ve deneysel doğrulanması
Tıp için neden küçük plastik küreler önemli
Etkili bir ilacı, kan damarlarından geçebilecek kadar küçük ve yükünü tam gerektiği yerde bırakabilecek bir zerrecik içine koyduğunuzu hayal edin. Polimer nanoparçacıklar olarak adlandırılan bu zerrecikler, birçok yeni tedavi ve görüntüleme aracının merkezinde yer alır. Ancak bunları doğru ve tekrarlanabilir boyutta üretmek şaşırtıcı derecede zordur. Bu çalışma, basit bir fizik-temelli bilgisayar modelinin yaygın kullanılan biyobozunur bir nanoparçacık olan polikaprolaktonun boyutunu tahmin edip ayarlayabileceğini gösteriyor; bu da yeni nanoterapilerin geliştirilmesinde yıllarca sürebilecek deneme‑yanılma süreçlerini kısaltabilir.
Mutfak karıştırmasından laboratuvar hassasiyetine
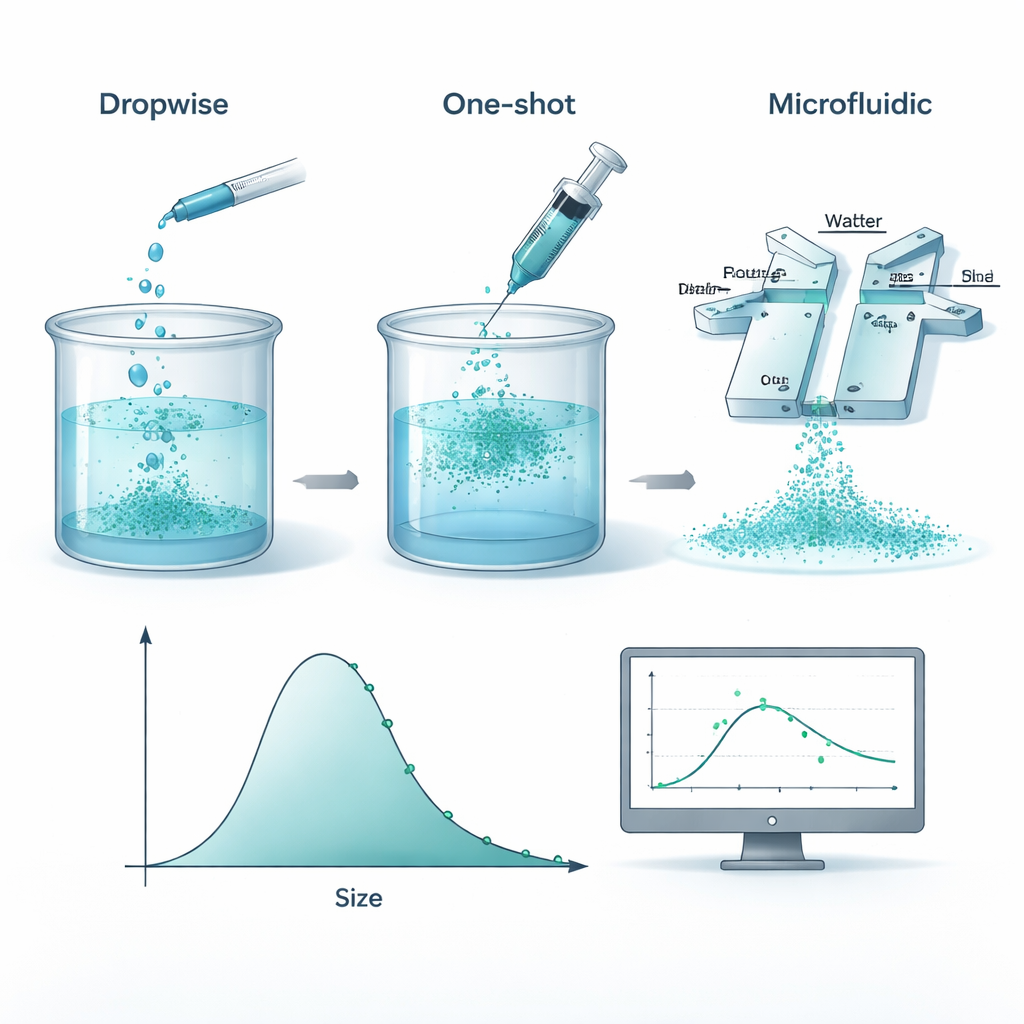
Bu nanoparçacıkları oluşturmak için araştırmacılar, polikaprolakton (PCL) adlı biyobozunur bir plastik maddesini organik bir çözücüde çözüyor ve sonra polimerin çözeltiden “çökmesini” ve küçük küreler oluşturmasını sağlamak için su ile karıştırıyorlar. Ekip üç pratik yöntemi karşılaştırdı: polimer çözeltisini damla damla yavaşça eklemek, bir kerede dökmek ve her iki sıvıyı dar kanallarda buluştuğu küçük bir mikroakışkan çipe sıkıştırmak. Dikkatle kontrol edilen koşullar altında, bu üç yaklaşımın tümü benzer ortalama boyutlar ve boyut dağılımı genişlikleri üretti. Bu da, incelenen aralıklarda, hangi karıştırma aletini kullandığınızdan ziyade hangi malzemeyi koyduğunuzun—polimer ve stabilizatör miktarının—daha önemli olduğunu gösteriyor.
Kalınlık ve yardımcı moleküller parçacıkları nasıl şekillendirir
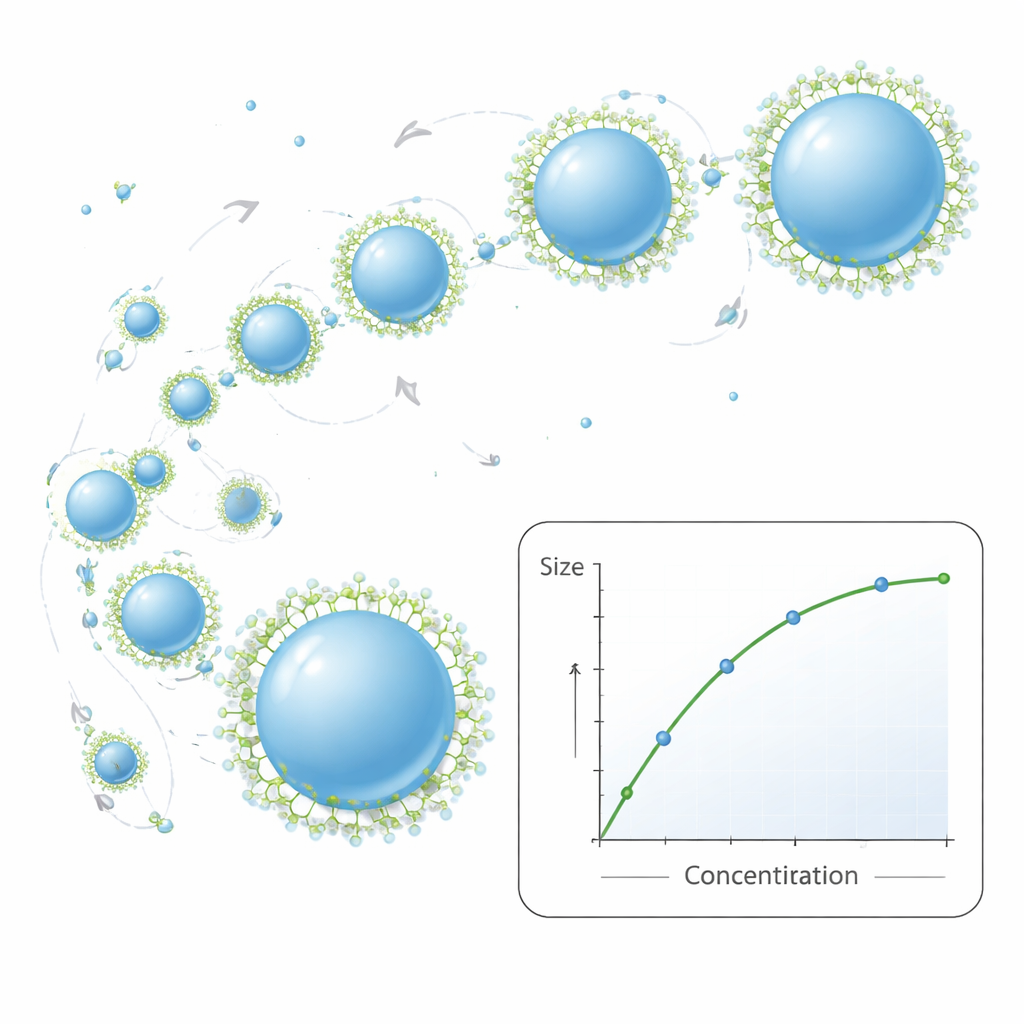
Araştırmacılar daha sonra tarif bileşenlerinin nihai parçacık boyutunu nasıl kontrol ettiğini inceledi. Organik fazdaki PCL miktarının artırılması, o sıvıyı daha kalın yani daha viskoz hale getirir. Şurubu suya karıştırmaya çalışmak yerine meyve suyuna karıştırmaya çalışmayı düşünün: daha yoğun şurup daha büyük damlacıklara ayrılır. Burada daha yoğun polimer çözeltileri daha büyük nanoparçacıklara ve biraz daha geniş boyut dağılımlarına yol açtı. İkinci bir çözücü olan etanol eklemek, çok yüksek polimer düzeylerinde süreci kararlı tutmaya yardımcı oldu, ancak üst konsantrasyon aralığında parçacıkları daha büyük hale getirme maliyetiyle oldu. İkinci bir bileşen olan Pluronic F‑127 adlı yüzey aktif madde ise moleküler bir yapışmayı önleyici ajan gibi davranır. Düşük yüzey aktif düzeylerinde parçacıklar birbirine çarpıp yapışma eğilimindedir, bu da daha büyük ve daha düzensiz parçacıklar oluşturur. Yüzey aktif konsantrasyonu arttıkça parçacık yüzeylerini kaplar, birleşmelerini önler ve daha küçük, daha stabil nanoparçacıklar verir—ancak belli bir noktadan sonra ek faydalar sınırlıdır ve boyut dağılımı daha karışık hale gelebilir.
Gerçeklikle uyumlu basit bir büyüme kuralı
Çalışmanın özünde, nanoparçacıkların ilk ortaya çıkışlarından sonra nasıl büyüdüklerini tanımlayan kompakt bir matematiksel model bulunuyor. Model, hareketlerini sıvı içindeki rastgele titreşimler olarak ele alıyor; burada çarpışmalar bazen iki parçacığın birleşip daha büyük bir parçacık oluşturmasına yol açıyor. Önceki modeller, parçacıklar her karşılaştığında anında birleşip kusursuz küreler haline geldiğini varsayıyordu. Yeni model iki gerçekçi öğe ekliyor: birincisi, iki temas eden parçacığın uzun bir şekilden tek bir küreye gevşemesi için sonlu bir süreye izin veriyor; ikincisi, yüzey aktif moleküllerin yüzeyi kademeli olarak “engellemesine”, böylece daha fazla birleşmeyi yavaşlatmasına veya durdurmasına imkan tanıyor. Sıcaklık, sıvı viskozitesi ve başlangıç polimer konsantrasyonu gibi yalnızca birkaç ölçülebilir girdiyle model, tarif koşullarına göre ortalama parçacık boyutunun nasıl değişmesi gerektiğini öngörüyor. Birçok deneyde, öngörülen boyutlar ışık saçılma ile ölçülenlere yakın çıktı ve aynı zamanda boyut dağılımının nasıl genişlediğine dair genel eğilimleri de yakaladı.
Modeli bir tasarım aracı olarak kullanmak
Bu yaklaşımın gerçekten işe yarayıp yaramadığı test etmek için ekip sorunu tersine çevirdi: modeli geçmiş verileri açıklaması için kullanmak yerine üç belirli nanoparçacık boyutu ve birimlilik derecesi verecek tarifleri önermesini istedi. Ardından bu “tasarlanmış” formülasyonları laboratuvarda hazırladılar. Ölçülen parçacık çapları hedeflerden yalnızca yüzde 1–7 aralığında farklıydı—tipik deneysel değişkenlik içinde—ve bu da modelin formülasyon seçimlerini güvenilir şekilde yönlendirebildiğini gösteriyor. Boyut dağılımının ne kadar dar veya geniş olacağına dair öngörüler daha az kesin olsa da, nispeten sıkı ile daha yaygın nüfusları ayırt edecek kadar iyiydi. Her molekülü veya her akış girdabını izleyen ağır simülasyon yöntemleriyle kıyaslandığında, bu sadeleştirilmiş model mütevazı bilgisayarlarda hızlı çalışıyor ve diğer polimerlere ve işlem düzeneklerine kolayca uyarlanabiliyor.
Geleceğin nanoterapileri için anlamı
Uzman olmayanlar için ana mesaj, yararlı nanoparçacıklar üretmenin artık yalnızca laboratuvarda sabır gerektiren deneme‑yanılmaya dayanmak zorunda olmadığıdır. Küçük plastik damlacıkların nasıl hareket ettiğini, çarpıştığını ve yüzey aktiflerle nasıl korunduklarını tanımlayan temel fiziği yakalayarak, bu çalışma formülasyon seçimlerinden—ne kadar polimer, hangi çözücü karışımı, ne kadar stabilizatör—nihai parçacık boyutuna pratik bir “harita” sunuyor. PCL, ilaç taşıma, implantlar ve görüntüleme ajanlarında yaygın kullanılan bir biyobozunur malzeme olduğundan, bu model araştırmacıların daha güvenli, daha etkili nanoterapileri daha hızlı ve daha az malzeme israfıyla tasarlamasına yardımcı olabilir. Aynı ilkeler diğer polimerlere de genişletilebilir ve nanoskopik terapiler dünyasına daha fazla öngörülebilirlik ve verimlilik kazandırabilir.
Atıf: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Anahtar kelimeler: polimer nanoparçacıklar, nanopresipitasyon, ilaç taşıma, sayısal modelleme, polikaprolakton